Pytanie 1
Jakie jest stężenie roztworu HNO3, który powstał w wyniku połączenia 50 cm3 roztworu HNO3 o stężeniu 0,2 mol/dm3 oraz 25 cm3 roztworu HNO3 o stężeniu 0,5 mol/dm3?
Wynik: 18/40 punktów (45,0%)
Wymagane minimum: 20 punktów (50%)
Jakie jest stężenie roztworu HNO3, który powstał w wyniku połączenia 50 cm3 roztworu HNO3 o stężeniu 0,2 mol/dm3 oraz 25 cm3 roztworu HNO3 o stężeniu 0,5 mol/dm3?
W próbkach obecne są składniki, które znacznie różnią się pod względem zawartości. Składnik, którego procentowy udział w próbce jest niższy od 0,01%, nazywamy
W wyniku reakcji 20 g tlenku magnezu z wodą uzyskano 20 g wodorotlenku magnezu. Oblicz efektywność reakcji.
MMg = 24 g/mol, MO = 16 g/mol, MH = 1 g/mol?
Brak odpowiedzi na to pytanie.
Metoda oczyszczania substancji oparta na różnicach w rozpuszczalności poszczególnych składników w określonym rozpuszczalniku to
50 cm3 alkoholu etylowego zmieszano w kolbie miarowej z 50 cm3 wody. W wyniku zjawiska kontrakcji objętość otrzymanego roztworu wyniosła 97,5 cm3. Ile wynosi stężenie procentowe (v/v) roztworu alkoholu w wodzie po zmieszaniu i stężenie procentowe roztworu alkoholu (v/v) po uzupełnieniu kolby wodą do 100 cm3?
| Stężenie procentowe (v/v) roztworu alkoholu w wodzie po zmieszaniu | Stężenie procentowe (v/v) roztworu alkoholu po uzupełnieniu kolby wodą do 100 cm3 | |
|---|---|---|
| A. | 49,2% | 48,0% |
| B. | 50,0% | 49,7% |
| C. | 51,3%, | 50,0% |
| D. | 53,3% | 50,2% |
Brak odpowiedzi na to pytanie.
Ekstrakcję w trybie ciągłym przeprowadza się
Podstawowy zestaw do filtracji składa się ze statywu oraz
Aby oddzielić galaretowaty osad typu Fe(OH)3 od roztworu, jaki sączek należy zastosować?
Substancje pomocnicze wykorzystywane do realizacji podstawowych analiz jakościowych i ilościowych, które nie wymagają wysokiej czystości, są oznaczane na opakowaniach symbolem
Przedstawiony sposób dotyczy pobierania próbki wody do przeprowadzenia badań
| Sposób pobierania próbki wody do przeprowadzenia badań: - próbki pobrać do sterylnych butelek; - przed przystąpieniem do pobierania wody zdjąć z kurka wszelkie urządzenia, zeskrobać zanieczyszczenia, następnie całkowicie otwierając i zamykając zawór, wielokrotnie płukać; - metalowy kurek wysterylizować płomieniem, a kurek z tworzywa sztucznego alkoholem etylowym; - kurek otworzyć do połowy przepływu i spuszczać wodę przez około 2-3 minuty do osiągnięcia stałej temperatury; - pobrać próbkę wody napełniając butelkę do około ¾ objętości i natychmiast zamknąć korkiem. |
Na podstawie danych w tabeli określ, jaką masę próbki należy pobrać, jeżeli wielkość ziarna wynosi 1·10-5 m.
| Wielkość ziaren lub kawałków [mm] | Poniżej 1 | 1-10 | 11-50 | Ponad 50 |
|---|---|---|---|---|
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
Rozpuszczalniki organiczne powinny być składowane
Odlanie cieczy z nad osadu to
Wybór lokalizacji do poboru próbek wody z rzeki nie jest uzależniony od
Jaką objętość zasady sodowej o stężeniu 1,0 mol/dm3 należy dodać do 56,8 g kwasu stearynowego, aby otrzymać mydło sodowe (stearynian sodu)?
| C17H35COOH + NaOH → C17H35COONa + H2O |
| (MC17H35COOH = 284 g/mol, MC17H35COONa = 306 g/mol, MNaOH = 40 g/mol, MH2O= 18 g/mol) |
Średnia masa wody wypływająca z pipety o deklarowanej pojemności 25 cm3, w temperaturze 25°C wynosi 24,80 g. Korzystając z danych zamieszczonych w tabeli wskaż wartość poprawki kalibracyjnej dla tej pipety.
| Masa wody zajmującej objętość 1 dm3 w zależności od temperatury pomiaru | |
|---|---|
| Temperatura °C | Masa wody g |
| 20 | 997,17 |
| 21 | 997,00 |
| 22 | 996,80 |
| 23 | 996,59 |
| 24 | 996,38 |
| 25 | 996,16 |
| 26 | 995,93 |
| 27 | 995,69 |
| 28 | 995,45 |
| 29 | 995,18 |
| 30 | 994,92 |
Losowo należy pobierać próbki z opakowań
Na rysunku przedstawiono przyrząd do pobierania próbek

Który symbol literowy umieszczany na naczyniach miarowych wskazuje na kalibrację do "wlewu"?
Aby przygotować 250 cm3 0,2-molowego roztworu wodorotlenku sodu, należy odważyć
| MNaOH = 40g / mol |
Podczas przygotowywania roztworów buforowych do analizy pH w laboratorium istotne jest, aby:
Metoda oczyszczania substancji, która opiera się na różnicy w rozpuszczalności substancji docelowej oraz zanieczyszczeń w zastosowanym rozpuszczalniku, nosi nazwę
Do szklanych narzędzi laboratoryjnych wielomiarowych używanych w analizach ilościowych należy
Aby uzyskać wodorotlenek wapnia, odważono 30 g węglanu wapnia, który następnie wyprażono. Powstały tlenek wapnia dodano do 100 cm3 wody, a otrzymany osad wysuszono i zważono, uzyskując 18,5 g wodorotlenku wapnia. Jaką wydajność miała ta reakcja?
Ca – 40 g/mol; O – 16 g/mol; C – 12 g/mol; H – 1 g/mol
Brak odpowiedzi na to pytanie.
Komora przeszklona w formie dużej szafy, wyposażona w wentylator, która zapobiega wydostawaniu się szkodliwych substancji do atmosfery laboratorium oraz chroni przed pożarami i eksplozjami, to
Brak odpowiedzi na to pytanie.
Ustalanie miana roztworu polega na
Brak odpowiedzi na to pytanie.
Proces oddzielania cieczy od osadu nazywa się
Brak odpowiedzi na to pytanie.
Na ilustracji przedstawiono sprzęt stosowany do sączenia osadu
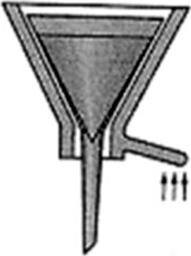
Brak odpowiedzi na to pytanie.
Aby odróżnić urządzenia w laboratorium chemicznym, rury do próżni maluje się w kolorze
Brak odpowiedzi na to pytanie.
Oblicz stężenie molowe 250 cm3 roztworu NaOH, w którym znajduje się 0,5 g substancji. Masa molowa NaOH wynosi 40 g/mol
Brak odpowiedzi na to pytanie.
Jakim narzędziem dokonuje się poboru próbki wody?
Brak odpowiedzi na to pytanie.
Deminimalizowaną wodę można uzyskać przez
Brak odpowiedzi na to pytanie.
Wybierz poprawny zapis jonowy spośród podanych reakcji, w których otrzymywany jest siarczan(VI) baru.
Brak odpowiedzi na to pytanie.
Nie należy używać gorącej wody do mycia
Brak odpowiedzi na to pytanie.
Jak przebiega procedura unieszkodliwiania rozlanego kwasu siarkowego(VI)?
Brak odpowiedzi na to pytanie.
Ilustracja przedstawia fragment szklanej pipety wielomiarowej

Brak odpowiedzi na to pytanie.
Jeżeli partia towaru składa się z 10 dużych opakowań, wtedy z jednego opakowania pobiera się kilka próbek, które następnie łączy, uzyskując próbkę
Brak odpowiedzi na to pytanie.
Zastosowanie łaźni wodnej nie jest zalecane w trakcie prac, w których stosuje się
Brak odpowiedzi na to pytanie.
Jakie oznaczenie znajduje się na naczyniach szklanych kalibrowanych do wlewu?
Brak odpowiedzi na to pytanie.
Na rysunku przedstawiono palnik Bunsena. Którym numerem oznaczono element do regulowania dopływu powietrza?

Brak odpowiedzi na to pytanie.