Pytanie 1
SPECT to
Wynik: 32/40 punktów (80,0%)
Wymagane minimum: 20 punktów (50%)
SPECT to
Na przedstawionym scyntygramie ukazano duży obszar
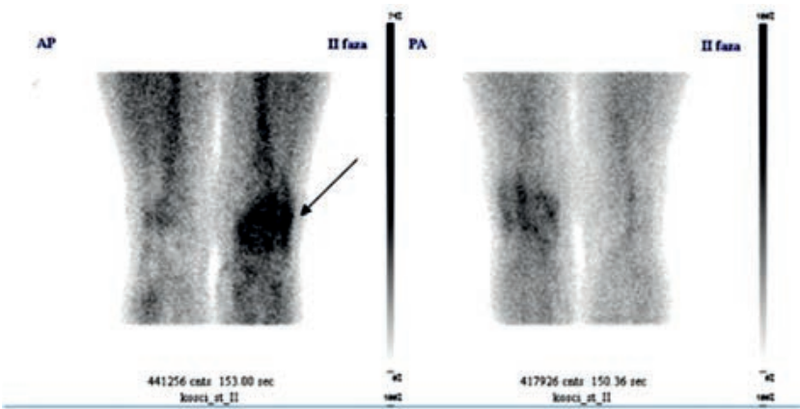
Czas połowicznego zaniku jest wykorzystywany
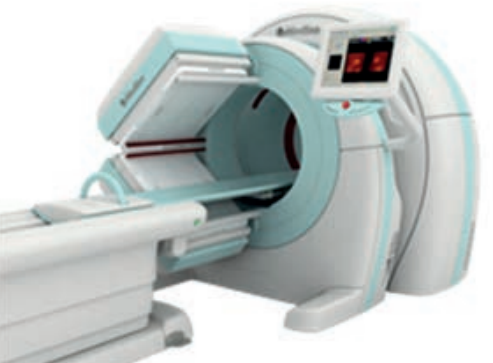
Które urządzenie zostało przedstawione na fotografii i w jakiej pracowni znajduje zastosowanie?
Podczas którego badania zostały zarejestrowane przedstawione obrazy?
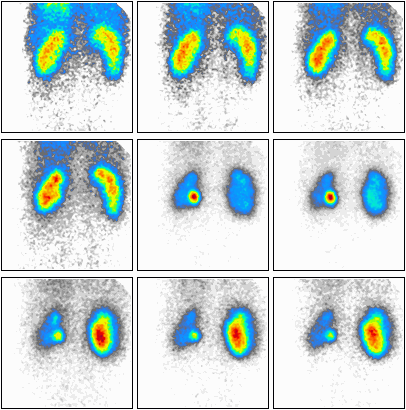
W badaniu PET CT wykorzystuje się radioizotopy emitujące promieniowanie
W leczeniu izotopowym tarczycy podaje się
Na scyntygramie strzałką oznaczono
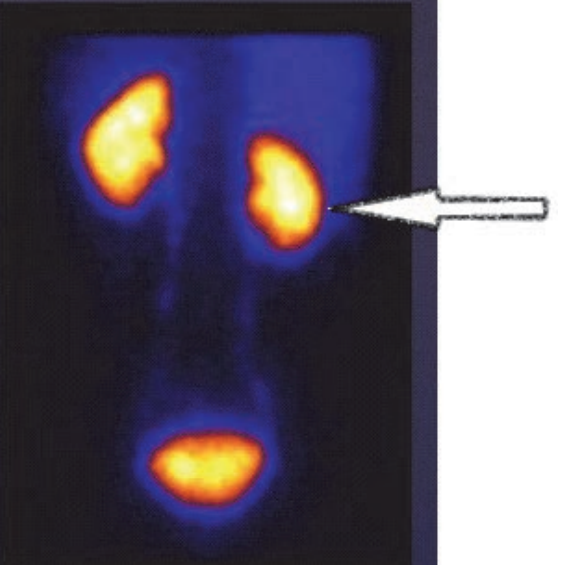
Radiofarmaceutyki stosowane w medycynie nuklearnej powstają dzięki połączeniu radioizotopu
Który radioizotop stosuje się do badania scyntygraficznego kości?
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Na zarejestrowanych obrazach badania renoscyntygraficznego widać, że prawa nerka pacjenta
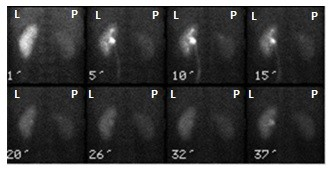
Podczas badania gammakamerą źródłem promieniowania jest
W celu wykonania badania scyntygraficznego układu kostnego radiofarmaceutyk należy podać pacjentowi
Który radioizotop jest stosowany w scyntygrafii perfuzyjnej mózgu?
W medycynie nuklearnej wykorzystuje się:
Kto jest odpowiedzialny za wykonywanie testów podstawowych kontroli jakości gammakamery w Zakładzie Medycyny Nuklearnej?
Które znaczniki są wykorzystywane w scyntygrafii tarczycy?
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
Który radioizotop jest emiterem promieniowania alfa?
Na scyntygramie tarczycy został uwidoczniony guzek
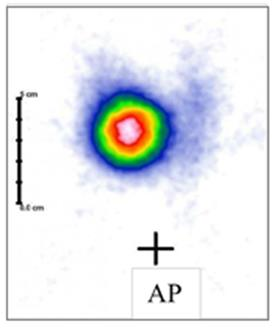
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Przedstawiony obraz został zarejestrowany podczas wykonania
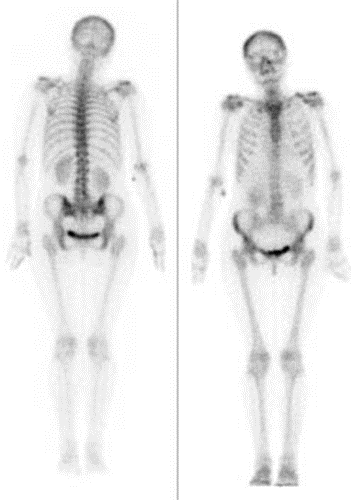
W badaniu PET stosuje się tylko radioizotopy emitujące
Ligand stosuje się
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?
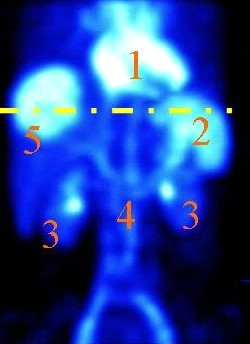
Przemiana promieniotwórcza radu w ren opisana wzorem \( {}_{88}^{226}\text{Ra} \to {}_{86}^{222}\text{Rn} + {}_{2}^{4}\text{He} \) jest rozpadem
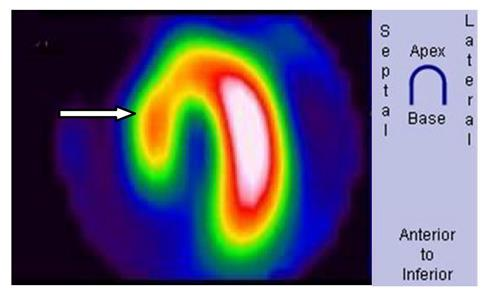
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę
Na scyntygramie tarczycy uwidoczniono guzek
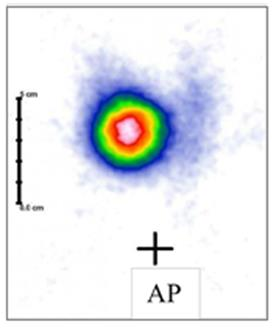
W której technice obrazowania zostają zarejestrowane jednocześnie dwa przeciwbieżne kwanty promieniowania gamma o równej energii 511 keV?
Który radiofarmaceutyk należy podać pacjentowi w scyntygrafii perfuzyjnej mózgu?
Na obrazie uwidoczniono
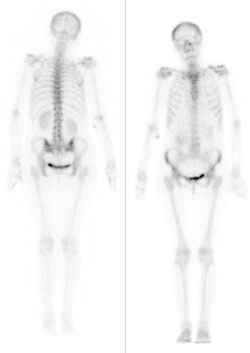
Diagnozowanie metodą PET oparte jest na zjawisku
Radioizotopowa terapia medycyny nuklearnej polega na wprowadzeniu do tkanek lub narządów radiofarmaceutyku
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
Glukoza podawana pacjentowi w badaniu PET jest znakowana radioaktywnym
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
W badaniu PETCT radioizotop ulega
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki