Pytanie 1
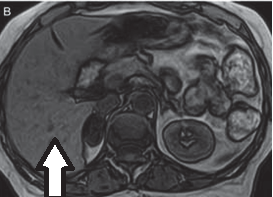
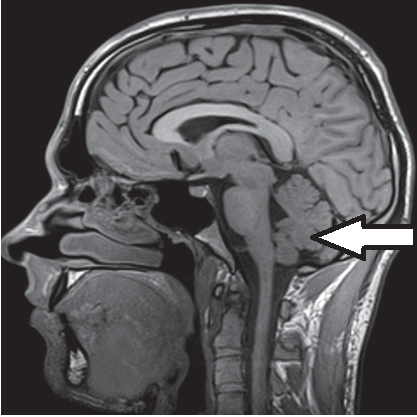
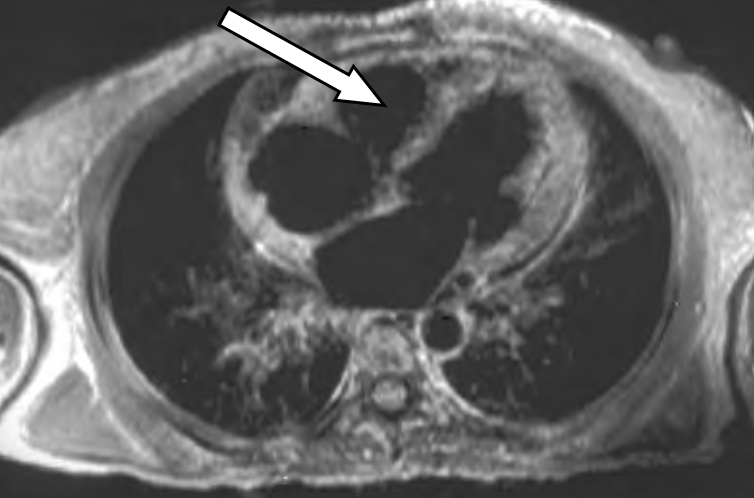
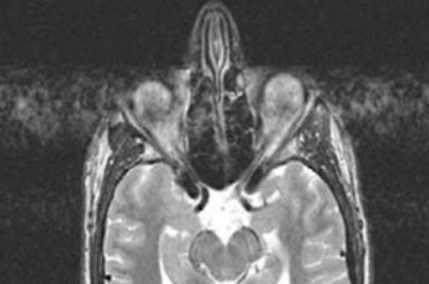
Którą strukturę anatomiczną oznaczono strzałką na obrazie rezonansu magnetycznego?
Wynik: 37/40 punktów (92,5%)
Wymagane minimum: 20 punktów (50%)
Którą strukturę anatomiczną oznaczono strzałką na obrazie rezonansu magnetycznego?

Nieostrość geometryczna obrazu rentgenowskiego zależy od
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
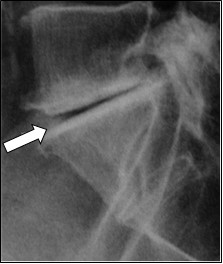
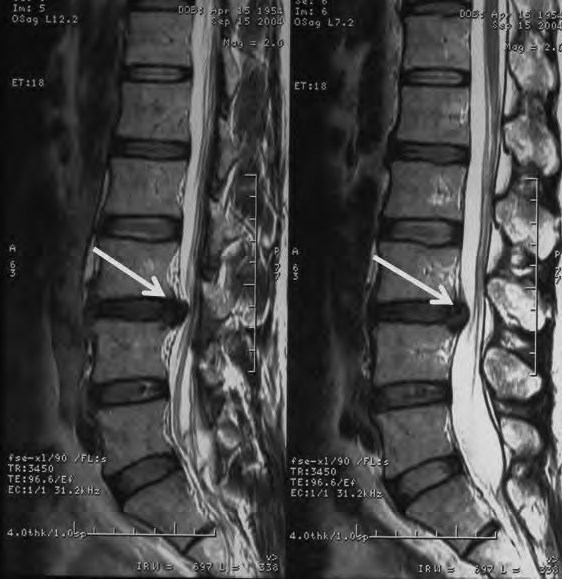
Na rentgenogramie strzałką zaznaczono
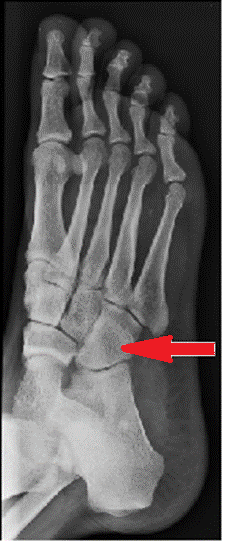
Na radiogramie stopy strzałką wskazano kość
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
Brachyterapia polega na napromieniowaniu pacjenta promieniowaniem
Na skanie rezonansu magnetycznego serca oznaczono
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
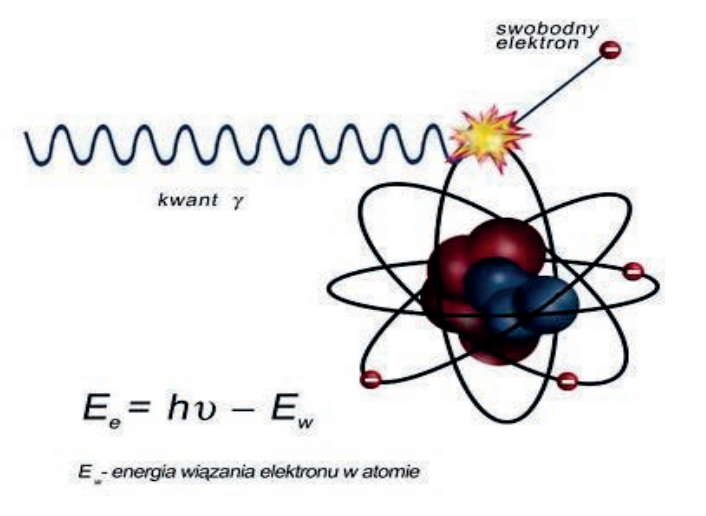
Na zamieszczonej rycinie przedstawiono
Wskazaniem do wykonania przesiewowego badania densytometrycznego jest
Ligand stosuje się
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

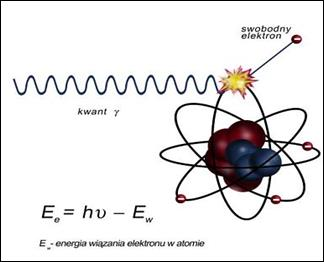
Rozpraszanie promieniowania X, w wyniku którego następuje zwiększenie długości fali promieniowania, to zjawisko
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Teleterapia polega na napromienowaniu
Zamieszczone badanie elektrokardiograficzne wykazało u pacjenta
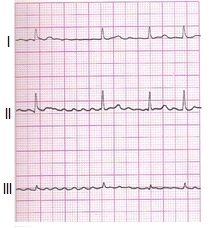
Artefakty zarejestrowane na elektrokardiogramie zostały wywołane przez
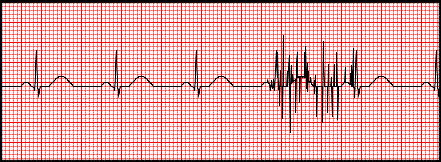
Jakie wymagania techniczne muszą spełniać aparaty terapeutyczne stosowane w zakładach brachyterapii, służące bezpośrednio do napromieniania pacjenta metodą zdalnego wprowadzania źródeł promieniotwórczych?
Fotostymulacja wykonywana jest podczas badania
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
W których projekcjach wykonuje się standardowe badanie mammograficzne?
Co jest przyczyną artefaktu widocznego na obrazie MR?
Standardowe badanie urografii polega na podaniu pacjentowi środka kontrastującego
Do pomiaru dawek indywidualnych u osób narażonych zawodowo na promieniowanie rentgenowskie są stosowane
Radioizotopowa terapia medycyny nuklearnej polega na wprowadzeniu do tkanek lub narządów radiofarmaceutyku
W trakcie obrazowania metodą rezonansu magnetycznego wykorzystywane jest zjawisko wysyłania sygnału emitowanego przez
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?
Jaki jest cel stosowania bolusa w radioterapii?
Na ilustracji przedstawiono zjawisko
Podczas badania EEG otwarcie oczu powoduje
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
W którym miejscu, zgodnie z zasadami wykonywania badania EKG, należy umocować żółtą elektrodę przedsercową V2?
W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
W standardowym badaniu elektrokardiograficznym elektrodę C4 należy umieścić
Na obrazie RM uwidoczniono odcinek kręgosłupa
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono