Pytanie 1
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Podczas rozkładu chloranu(V) potasu powstają chlorek potasu oraz tlen. Ile gramów tlenu zostanie wydzielonych w trakcie rozkładu 24,5 g chloranu(V) potasu, jeśli jednocześnie uzyskano 14,9 g chlorku potasu? Masy molowe pierwiastków: K = 39 g/mol, Cl = 35,5 g/mol, O=16 g/mol?
Podstawowy zestaw do filtracji składa się ze statywu oraz
Zamieszczony fragment procedury opisuje sposób otrzymywania
| „W zlewce o pojemności 250 cm3 rozpuść w 50 cm3 wody destylowanej 5 g uwodnionego siarczanu(VI) miedzi(II). Do roztworu dodaj 16,7 cm3 roztworu NaOH o stężeniu 6 mol/dm3. Następnie dodaj 10 g glukozy w celu przeprowadzenia reakcji redukcji jonów miedzi(II) do miedzi(I). Ostrożnie ogrzewaj zlewkę z mieszaniną reakcyjną do otrzymania czerwonego osadu (...)Osad odsącz, przemyj alkoholem i susz na bibule na powietrzu." |
Na podstawie informacji zawartych w tabeli wskaż mieszaninę oziębiającą o temperaturze -21 °C.
| Temperatura mieszaniny | Skład mieszaniny | Stosunek masowy |
| -15 °C | lód + octan sodu | 10:9 |
| -18 °C | lód + chlorek amonu | 10:3 |
| -21 °C | lód + chlorek sodu | 3:1 |
| -25 °C | lód + azotan amonu | 1:9 |
Która część małej partii materiału jest najczęściej pobierana w celu przygotowania próbki ogólnej?
Jaka minimalna pojemność powinna mieć miarka, aby jednorazowo zmierzyć 60,0 cm3 wody?
W tabeli zamieszczono temperatury wrzenia niektórych składników powietrza. Na podstawie tych danych podaj, który ze składników oddestyluje jako ostatni.
| Temperatura wrzenia °C | Składniki |
|---|---|
| -245,9 | Neon |
| -182,96 | Tlen |
| -195,8 | Azot |
| -185,7 | Argon |
Aby uzyskać wodorotlenek wapnia, odważono 30 g węglanu wapnia, który następnie wyprażono. Powstały tlenek wapnia dodano do 100 cm3 wody, a otrzymany osad wysuszono i zważono, uzyskując 18,5 g wodorotlenku wapnia. Jaką wydajność miała ta reakcja?
Ca – 40 g/mol; O – 16 g/mol; C – 12 g/mol; H – 1 g/mol
Przedstawiony na ilustracji zestaw służy do

To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Który sposób przechowywania próbek żywności jest niezgodny z Rozporządzeniem Ministra Zdrowia?
| Fragment Rozporządzenia Ministra Zdrowia w sprawie pobierania i przechowywania próbek żywności przez zakłady żywienia zbiorowego typu zamkniętego |
| (...) Zakład przechowuje próbki, przez co najmniej 3 dni, licząc od chwili, kiedy cała partia została spożyta w miejscu wyłącznym właściwym do tego celu oraz w warunkach zapewniających utrzymanie temperatury +4°C lub niższej, w zależności od przechowywanego produktu. Miejsce przechowywania próbek musi być tak zabezpieczone, aby dostęp do niego posiadał tylko kierujący zakładem lub osoba przez niego upoważniona. |
Roztwory, które wykorzystuje się do kalibracji pehametrów, to
Wskaź zestaw reagentów oraz przyrządów wymaganych do przygotowania 0,5 dm3 roztworu HCl o stężeniu 0,2 mol/dm3?
Reakcja miedzi metalicznej z stężonym kwasem azotowym(V) prowadzi do powstania azotanu(V) miedzi(II) oraz jakiego związku?
Na rysunku przedstawiono urządzenie stosowane do pobierania próbek
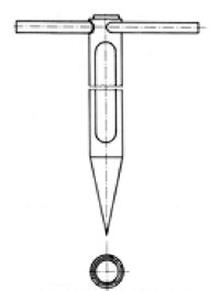
Zapis "20°C" umieszczony na pipecie oznacza, że

Na rysunku numerami 1 i 4 oznaczono:
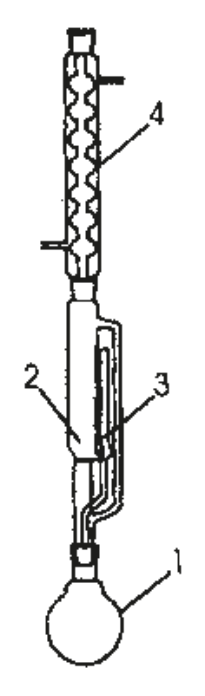
Aby przygotować miano kwasu solnego, konieczne jest odważenie węglanu sodu o masie wynoszącej około 400 mg. Jaką precyzję powinna mieć waga używana do odważenia węglanu sodu?
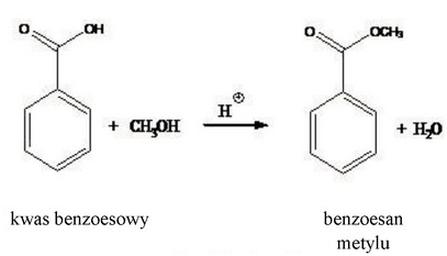
Do reakcji estryfikacji użyto 150 g kwasu benzoesowego (M = 122,12 g/mol), w wyniku której otrzymano czysty preparat benzoesanu metylu (M = 136,2 g/mol). Ile gramów benzoesanu metylu otrzymano, jeżeli reakcja przebiegała z wydajnością 92%?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Użycie płuczek jest konieczne w trakcie procesu
Czułość bezwzględna wagi definiuje się jako
W wyniku rozkładu 100 g węglanu wapnia, otrzymano 25 g tlenku wapnia. Wydajność procentowa reakcji wynosi
| MCaCO3 = 100g / mol | MCaO = 56g / mol |
Który z wskaźników nie jest używany w alkacymetrii?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Ile gramów chlorku baru powinno się rozpuścić w wodzie, aby uzyskać 200 cm3 roztworu o stężeniu 10% i gęstości 1,203 g/cm3?
Resztki szkła, osadników czy inne odpady stałe powstałe w laboratorium analitycznym powinny być umieszczone
W celu sprawdzenia stężenia kwasu siarkowego(VI) odważono 1 g badanego kwasu i przeprowadzono analizę miareczkową, w której zużyto 20,4 \( \text{cm}^3 \) roztworu NaOH.
Stężenie procentowe badanego kwasu, obliczone na podstawie wzoru wynosi
$$ C_p = \frac{0,02452 \cdot V_{NaOH}}{mp} \cdot 100\% $$gdzie:
\( C_p \) – stężenie procentowe badanego kwasu; \( \% \)
\( 0,02452 \) – współczynnik przeliczeniowy; \( \text{g/cm}^3 \)
\( V_{NaOH} \) – objętość roztworu NaOH, zużyta w miareczkowaniu; \( \text{cm}^3 \)
\( mp \) – odważka badanego kwasu; g
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Między wodorotlenkiem baru a chlorkiem amonu dochodzi do spontanicznej reakcji, która powoduje silne schłodzenie mieszaniny oraz wydobycie się charakterystycznego zapachu amoniaku.
Ba(OH)2(s) + 2 NH4Cl(s) → BaCl2(aq) + 2 H2O(c) + 2 NH3(g) Wskaź, które sformułowanie właściwie wyjaśnia to zjawisko.
nieodwracalnie jej równowagę.
Na rysunku przedstawiono palnik
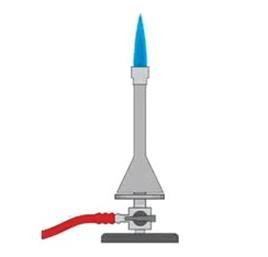
W laboratoriach roztwór potasu dichromianu(VI) w stężonym kwasie siarkowym(VI) wykorzystuje się do
W którym z podanych równań reakcji dochodzi do zmiany stopni utlenienia atomów?
Jakim przyrządem nie jest możliwe określenie gęstości cieczy?
Czy próbkę laboratoryjną przechowuje się w lodówce, gdy występuje w niej
Oblicz, ile moli gazu można zebrać w pipecie gazowej o pojemności 500 cm3, jeśli gaz będzie gromadzony w warunkach normalnych. (W normalnych warunkach jeden mol gazu ma objętość 22,4 dm3)
Który z wymienionych roztworów NaOH, o określonych stężeniach, nie jest roztworem mianowanym?
Podczas oznaczania kwasu siarkowego zachodzi reakcja:
H2SO4 + 2NaOH → Na2SO4 + 2H2OZgodnie z zamieszczoną instrukcją, roztwór poreakcyjny należy
| Fragmenty instrukcji zbierania, utylizacji i eliminacji odpadów chemicznych | |
|---|---|
| Lista substancji, które mogą być usunięte z odpadami komunalnymi w postaci stałej, lub wprowadzone do systemu kanalizacyjnego w postaci rozcieńczonych roztworów wodnych, o ile ich ilość nie przekracza jednorazowo 100 g. | |
| Związki nieorganiczne Siarczany sodu, potasu, magnezu, wapnia, amonu | |
| Kwasy nieorganiczne Stężone kwasy ostrożnie rozcieńczyć przez wkroplenie z równoczesnym mieszaniem do wody z lodem, a następnie zneutralizować roztworem wodorotlenku sodowego. Po neutralizacji doprowadzić pH roztworu do zakresu 6-8 przelać do pojemnika S. Małe ilości kwasów takich jak siarkowy, solny, azotowy czy fosforowy (nie więcej niż 10 g) po rozcieńczeniu wodą i neutralizacji roztworem wodorotlenku sodowego oraz doprowadzeniu pH takiego roztworu do zakresu 6-8 można wylać do zlewu i obficie spłukać wodą. | |
| Sole nieorganiczne Stałe sole nieorganiczne – pojemnik N. Obojętne roztwory soli nieorganicznych pojemnik S. Sole metali ciężkich, sole o właściwościach toksycznych – pojemnik TN. |