Pytanie 1
W obrazowaniu MR wykorzystuje się moment magnetyczny
Wynik: 22/40 punktów (55,0%)
Wymagane minimum: 20 punktów (50%)
W obrazowaniu MR wykorzystuje się moment magnetyczny
Gdzie znajduje się węzeł zatokowo-przedsionkowy wywołujący rytmiczne skurcze mięśnia serca?
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
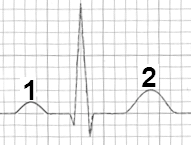
Na schemacie oznaczono
Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
W zapisie EKG linia izoelektryczna obrazuje
Wskazaniem do wykonania badania spirometrycznego jest
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
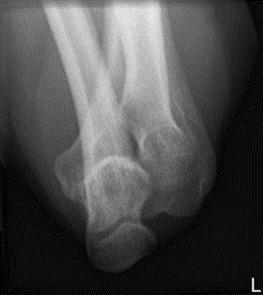
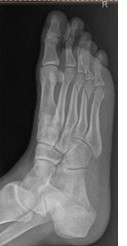
Na rentgenogramie stopy uwidocznione jest złamanie
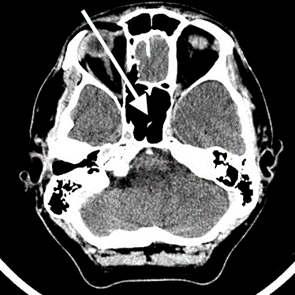
Na przedstawionym radiogramie TK głowy strzałką zaznaczono
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Do zdjęcia prawych otworów międzykręgowych kręgosłupa szyjnego pacjent stoi w skosie
Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
Parametr SNR w obrazowaniu MR oznacza
Czas połowicznego zaniku jest wykorzystywany
Teleterapia polega na napromienowaniu
Na scyntygramie tarczycy został uwidoczniony guzek
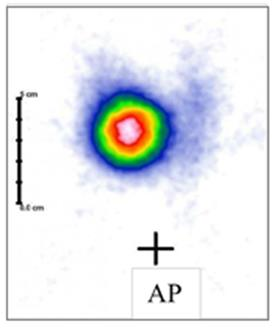
Na radiogramie TK głowy strzałką wskazano
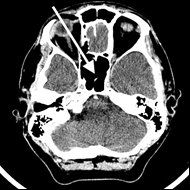
Kiedy w procesie terapii wykonuje się badanie CBCT (cone beam computed tomography)?
Przy ułożeniu do zdjęcia AP czaszki płaszczyzna
Podstawowym elementem diagnostycznym aparatury izotopowej wykorzystującej emisyjne metody pomiaru jest
Zdjęcie zatok przynosowych wykonuje się w pozycji
Które urządzenie zostało przedstawione na fotografii i w jakiej pracowni znajduje zastosowanie?
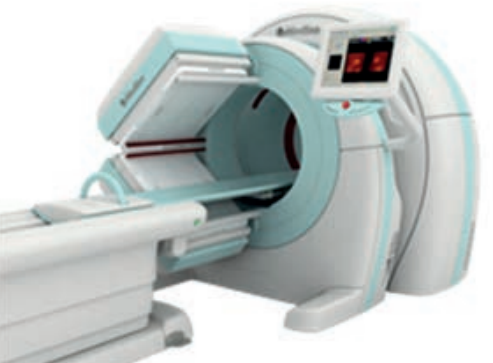
Skrótem CTV w radioterapii oznacza się
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
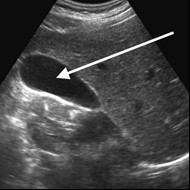
Podczas teleradioterapii piersi lewej narządem krytycznym jest
W radiologii analogowej lampy rentgenowskiej z tubusem używa się do wykonania zdjęcia
W scyntygrafii perfuzyjnej płuc pacjentowi podawany jest radioizotop
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce
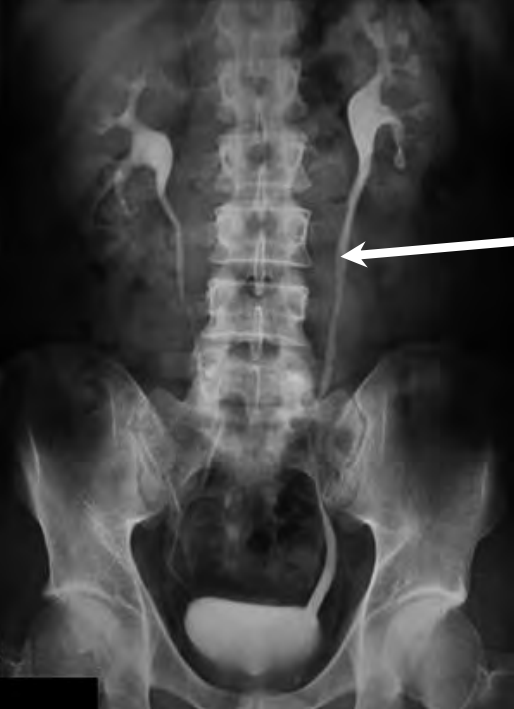
Na prawidłowo przedstawionym radiogramie badania kontrastowego strzałką zaznaczono
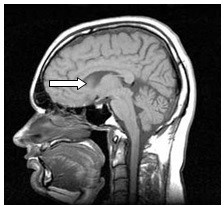
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
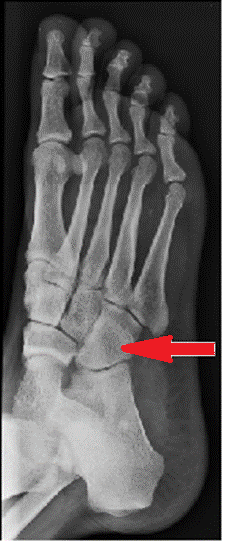
Na radiogramie stopy strzałką wskazano kość
Która właściwość promieniowania X pozwala na skierowanie promienia centralnego na wybrany punkt topograficzny podczas wykonywania badania radiologicznego?
Które znaczniki są wykorzystywane w scyntygrafii tarczycy?
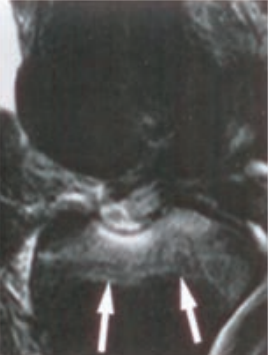
Obraz stawu kolanowego otrzymano metodą
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
W celu unieruchomienia okolicy badanej podczas wykonywania zdjęcia nadgarstka u osoby dorosłej należy zastosować
Czym charakteryzuje się późny odczyn popromienny?
Diagnozowanie metodą PET oparte jest na zjawisku