Pytanie 1
Który radioizotop jest emiterem promieniowania alfa?
Wynik: 29/40 punktów (72,5%)
Wymagane minimum: 20 punktów (50%)
Który radioizotop jest emiterem promieniowania alfa?
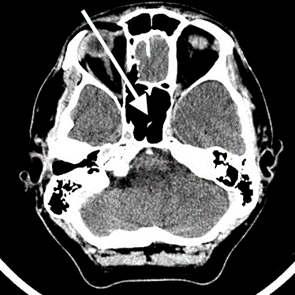
Na przedstawionym radiogramie TK głowy strzałką zaznaczono
W badaniu EKG elektrodę przedsercową V4 należy umocować
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Podstawowym elementem diagnostycznym aparatury izotopowej wykorzystującej emisyjne metody pomiaru jest
W zapisie EKG załamki P dodatnie w odprowadzeniu I i II, a ujemne w aVR oraz częstotliwość rytmu mniejsza niż 60/min wskazują na
W celu wykonania badania scyntygraficznego układu kostnego radiofarmaceutyk należy podać pacjentowi
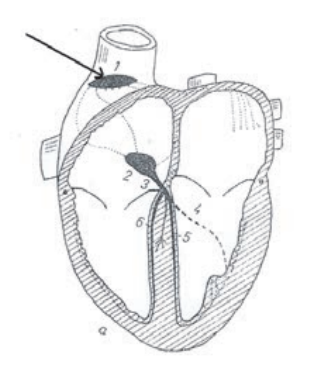
Strzałką na schemacie oznaczono
Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
Jakie źródła promieniowania stosowane są w brachyterapii?
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
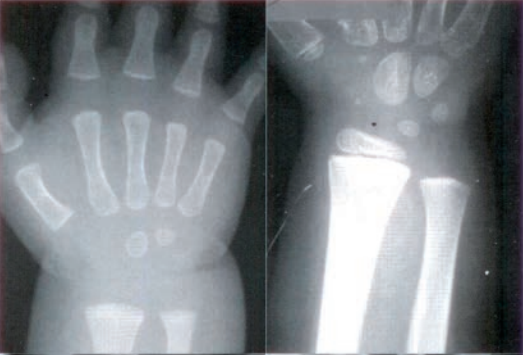
Zestaw rentgenogramów przedstawia
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
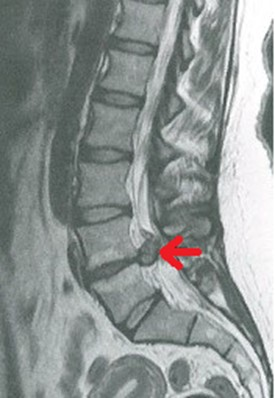
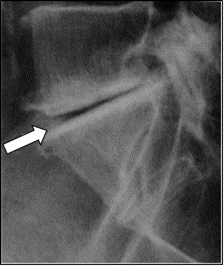
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
Jaka jest standardowa odległość OF do wykonania rentgenowskich zdjęć kości i stawów kończyny górnej?
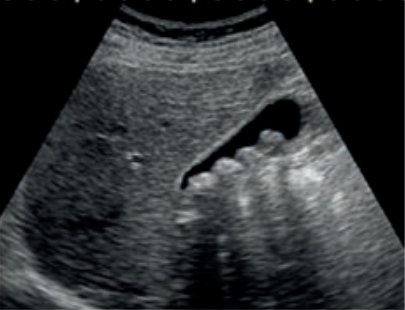
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
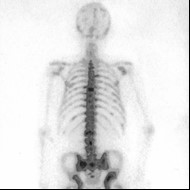
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
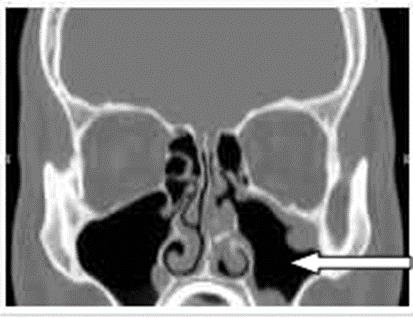
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
Szczytowy przepływ wydechowy zarejestrowany w trakcie badania maksymalnie natężonego wydechu jest oznaczany skrótem
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
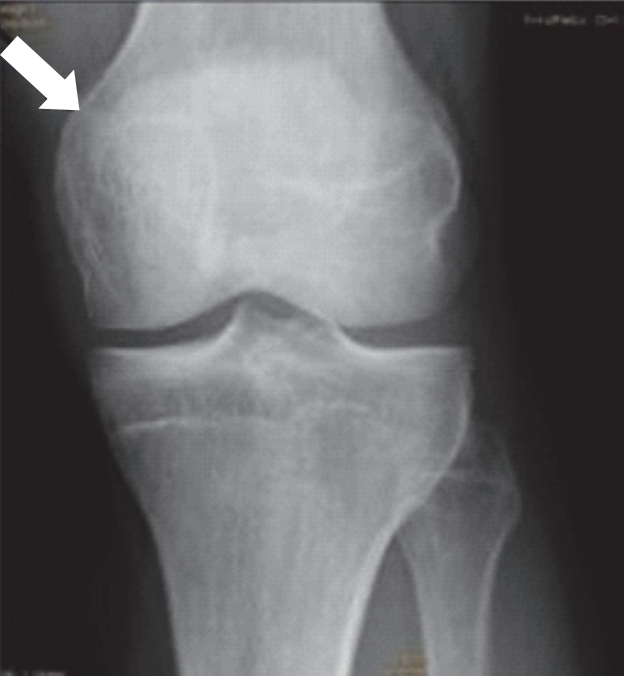
Którą strukturę anatomiczną zaznaczono na radiogramie stawu kolanowego?
Na zamieszczonym rentgenogramie strzałką zaznaczono
Podczas wykonywania badania EKG czarną elektrodę kończynową należy umieścić na kończynie dolnej
Który radiofarmaceutyk należy podać pacjentowi w scyntygrafii perfuzyjnej mózgu?
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Przedstawiony obraz został zarejestrowany podczas wykonywania
Do zdjęcia lewobocznego kręgosłupa lędźwiowo-krzyżowego pacjenta należy ułożyć na boku
Zgodnie z obowiązującą procedurą radiologiczną zdjęcie jamy brzusznej przy podejrzeniu zapalenia nerek zostanie wykonane w projekcji
Która metoda diagnostyczna służy do określenia gęstości minerału kostnego w ujęciu objętościowym g/cm³?
Urografia polega na
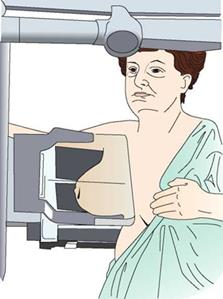
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
W pracowni ultrasonograficznej technik elektroradiolog nie korzysta z przepisów dotyczących
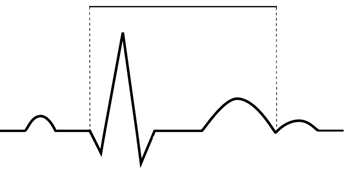
Na wykresie EKG zaznaczono
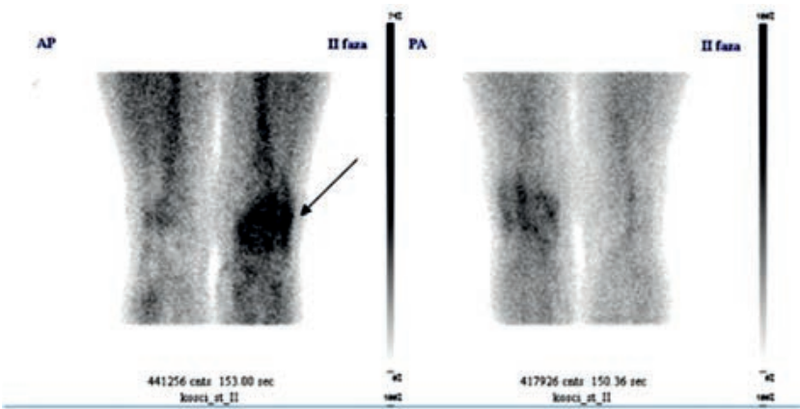
Na przedstawionym scyntygramie ukazano duży obszar
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Rumień skóry pojawiający się podczas radioterapii jest objawem