Pytanie 1
Na radiogramie żuchwy uwidoczniono złamanie w okolicy
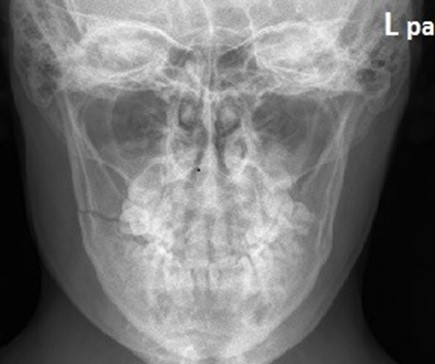
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Na radiogramie żuchwy uwidoczniono złamanie w okolicy

Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
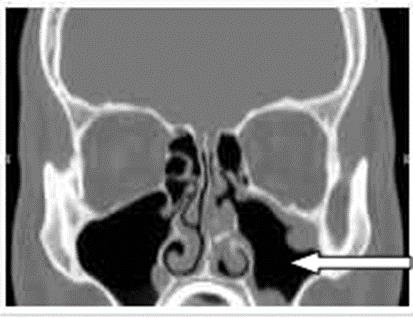
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?
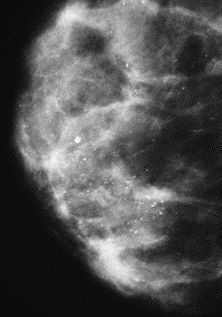
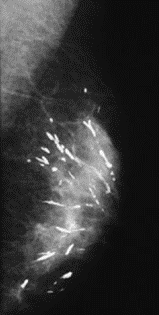
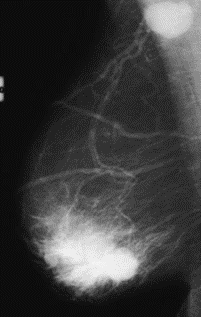
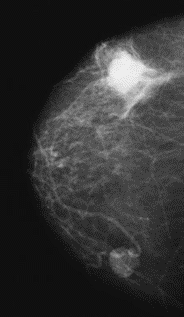
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Która składowa prawidłowej krzywej EKG odpowiada powolnej repolaryzacji komór mięśnia sercowego?
Fala głosowa rozchodzi się
Pojawienie się w zapisie EKG patologicznego załamka Q lub QS może wskazywać na
Jak konwencjonalnie frakcjonuje się dawkę w teleradioterapii?
W sekwencji echa spinowego obraz T2-zależny uzyskuje się przy czasie repetycji TR
Na ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
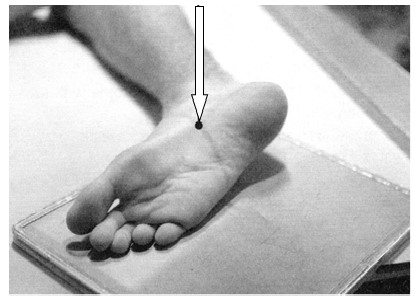
Na radiogramie stawu barkowego strzałką wskazano
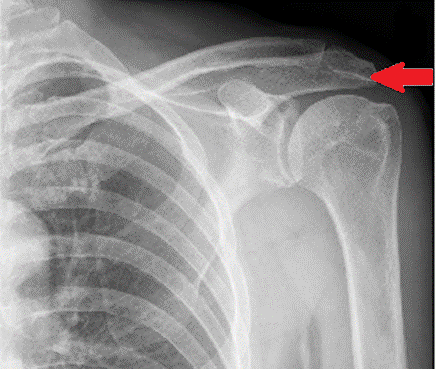
W zapisie EKG zespół QRS odzwierciedla
Radioizotopowa terapia medycyny nuklearnej polega na wprowadzeniu do tkanek lub narządów radiofarmaceutyku
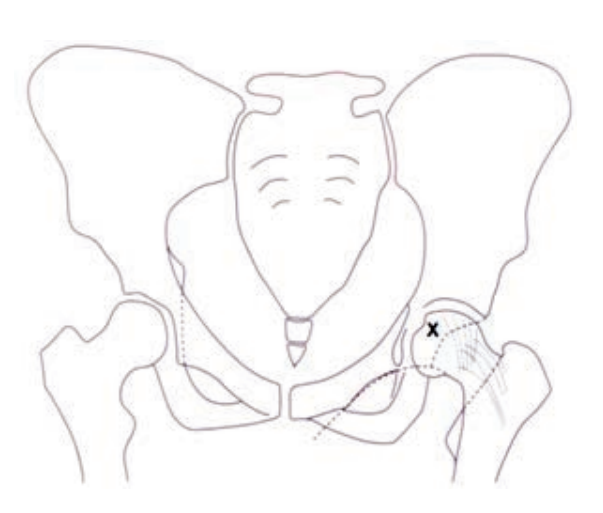
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
Który radioizotop jest stosowany w diagnostyce i terapii raka tarczycy?
Zadaniem technika elektroradiologii w pracowni badań naczyniowych jest
Kiedy w procesie terapii wykonuje się badanie CBCT (cone beam computed tomography)?
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
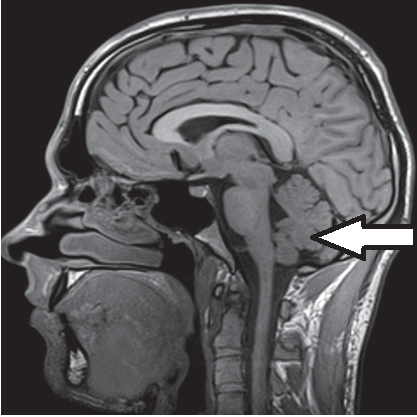
Którą strukturę anatomiczną oznaczono strzałką na obrazie rezonansu magnetycznego?
Jaki jest cel stosowania bolusa w radioterapii?
W badaniu EKG elektrodę przedsercową V4 należy umocować
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
Na zamieszczonej ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
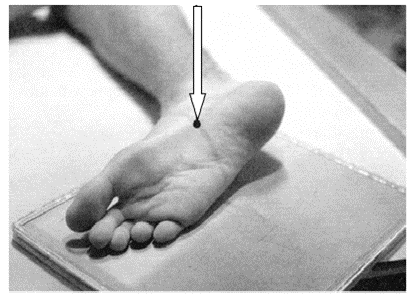
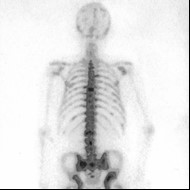
Przedstawiony obraz został zarejestrowany podczas wykonywania
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
W badaniu EKG elektrodę przedsercową V4 należy umocować
Rozpraszanie promieniowania X, w wyniku którego następuje zwiększenie długości fali promieniowania, to zjawisko
Gdzie znajduje się węzeł zatokowo-przedsionkowy wywołujący rytmiczne skurcze mięśnia serca?
Do środków kontrastujących negatywnych należą
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
Który zestaw zdjęć narządów klatki piersiowej należy wykonać u pacjenta z podejrzeniem lewostronnego zapalenia płuc?
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
W obrazowaniu MR do uwidocznienia naczyń krwionośnych jest stosowana sekwencja
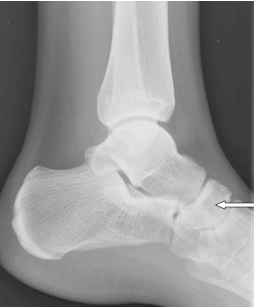
Na radiogramie strzałką oznaczono
W jakich jednostkach mierzy się natężenie dźwięku?
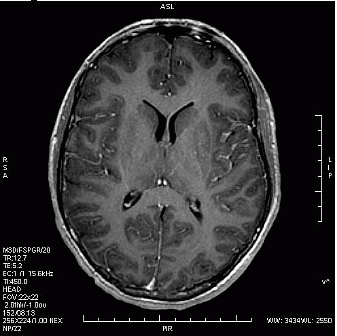
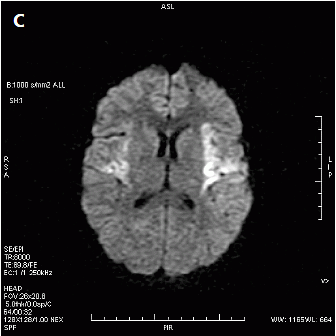
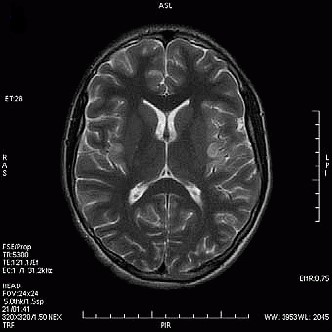
Który obraz MR mózgu został wykonany w sekwencji DWI?
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Warstwa półchłonna (WP) służy do obliczania