Pytanie 1
Strzykawka automatyczna do podawania kontrastu jest stosowana przy wykonywaniu
Wynik: 38/40 punktów (95,0%)
Wymagane minimum: 20 punktów (50%)
Strzykawka automatyczna do podawania kontrastu jest stosowana przy wykonywaniu
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
W standardowym badaniu elektrokardiograficznym elektrodę C4 należy umieścić
Na którym obrazie MR jest widoczne pasmo saturacji?

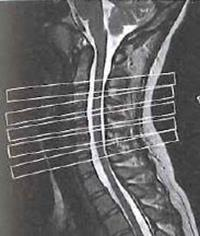
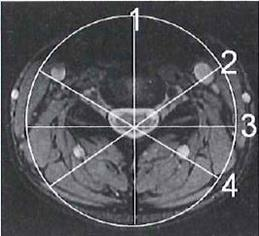
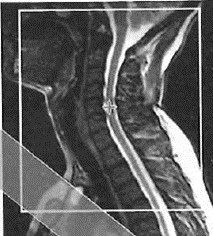
W których projekcjach wykonuje się standardowe badanie mammograficzne?
Radiogram jamy brzusznej uwidacznia
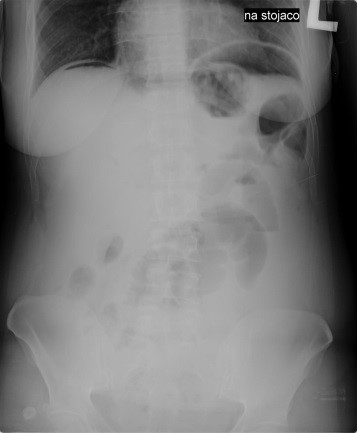
W ułożeniu do rentgenografii AP stawu kolanowego promień główny pada
Który obszar napromieniania wskazano na ilustracji strzałką?
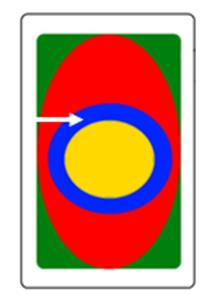
Którą strukturę anatomiczną oznaczono na skanie TK głowy?
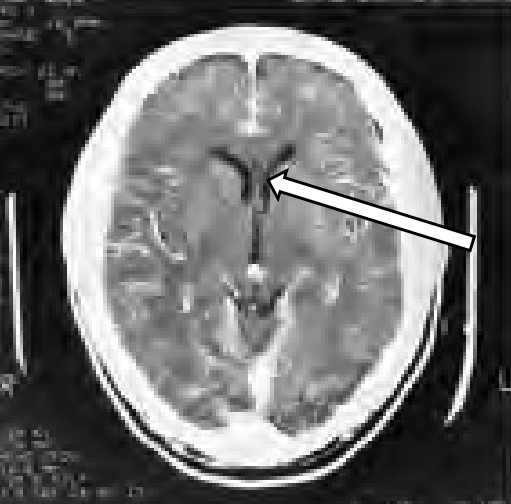
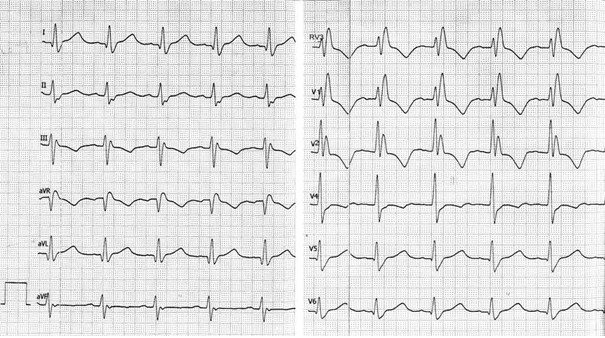
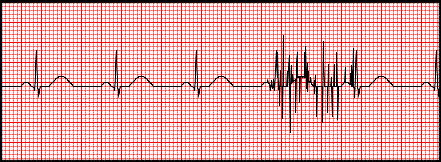
Przedstawiony zapis elektrokardiograficzny może wskazywać na
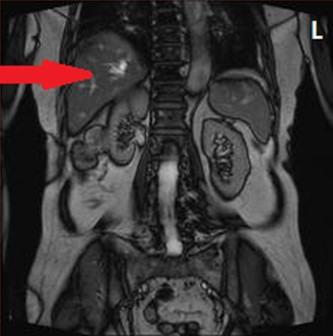
Na obrazie MR jamy brzusznej strzałką wskazano
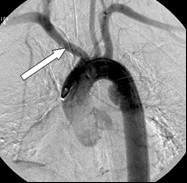
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
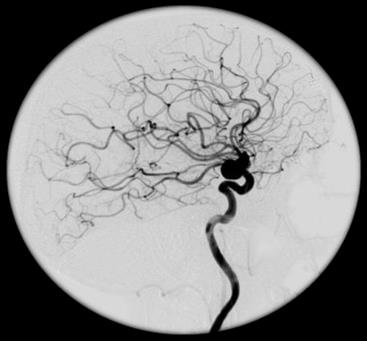
Na zamieszczonym obrazie RM nadgarstka lewego strzałką wskazano kość
W radioterapii hadronowej leczenie odbywa się przy użyciu
Na ilustracji przedstawiono ułożenie pacjenta do zdjęcia rentgenowskiego
Który z nowotworów jest hormonozależny?
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Cholangiografia to badanie radiologiczne
Podczas wykonywania zdjęć wewnątrzustnych zębów górnych linia Campera powinna przebiegać w stosunku do płaszczyzny podłogi
W scyntygrafii kośćca „ogniska gorące” oznaczają miejsca
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Rutynowe badanie koronarografii prawej tętnicy wieńcowej wykonywane jest w rzucie skośnym przednim
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
Jednostką indukcji magnetycznej jest
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
W badaniu PETCT radioizotop ulega
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
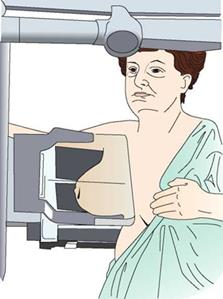
Na obrazie cyfrowej angiografii subtrakcyjnej strzałką zaznaczono
Pielografia to badanie układu
Do prób aktywacyjnych stosowanych w badaniu EEG zalicza się
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |
W którym miejscu, zgodnie z zasadami wykonywania badania EKG, należy umocować żółtą elektrodę przedsercową V2?
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną
Celem radioterapii paliatywnej nie jest
Artefakty zarejestrowane na elektrokardiogramie zostały wywołane przez
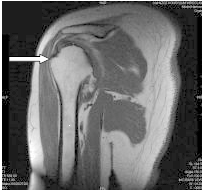
Którą strukturę anatomiczną oznaczono na obrazie rezonansu magnetycznego?
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do