Pytanie 1
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Wynik: 37/40 punktów (92,5%)
Wymagane minimum: 20 punktów (50%)
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?
SPECT to
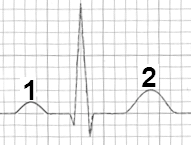
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
W badaniu PET CT wykorzystuje się radioizotopy emitujące promieniowanie
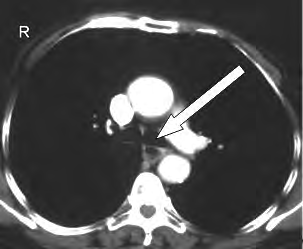
Zamieszczone na ilustracji obrazy dotyczą badania
Na prawidłowo wykonanym zdjęciu zatok w projekcji PA górny zarys piramid rzutuje się
Elementem pomocniczym w radioterapii, zapewniającym powtarzalność ułożenia w pozycji terapeutycznej, a także unieruchomienie pacjenta, jest
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Rytm alfa i beta rejestruje się podczas badania
Fistulografia to badanie kontrastowe
Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
Brachyterapia wewnątrzprzewodowa jest stosowana w leczeniu
W badaniu EKG elektrodę przedsercową V4 należy umocować
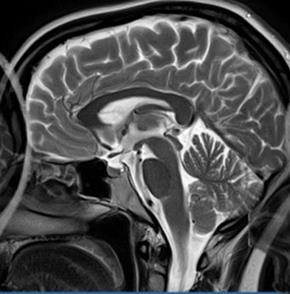
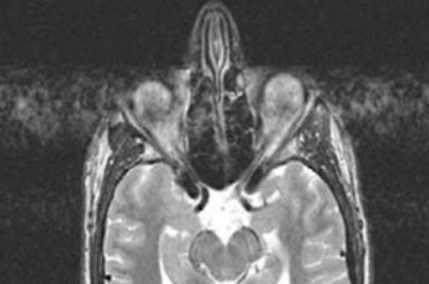
Która przyczyna spowodowała powstanie artefaktu widocznego na zamieszczonym obrazie MR?
Które informacje należy zamieścić na strzykawce z radiofarmaceutykiem przygotowanym przez technika elektroradiologa?
W radiologii analogowej lampy rentgenowskiej z tubusem używa się do wykonania zdjęcia
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
W którym miejscu, zgodnie z zasadami wykonywania badania EKG, należy umocować żółtą elektrodę przedsercową V2?
W metodzie RM (rezonansu magnetycznego) po umieszczeniu pacjenta w silnym, stałym polu magnetycznym dochodzi do oddziaływania
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
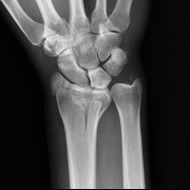
Na schemacie oznaczono
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
Przemiana promieniotwórcza radu w ren opisana wzorem \( {}_{88}^{226}\text{Ra} \to {}_{86}^{222}\text{Rn} + {}_{2}^{4}\text{He} \) jest rozpadem
Co jest przyczyną artefaktu widocznego na obrazie MR?
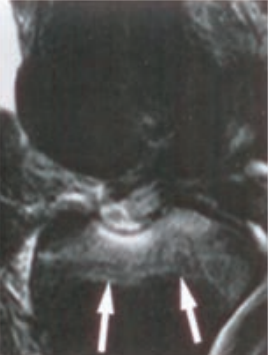
Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
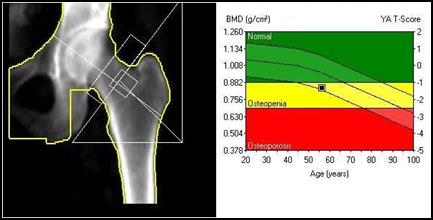
Obraz stawu kolanowego otrzymano metodą
W badaniu EKG odprowadzenie I rejestruje różnicę potencjałów między
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
Przy ułożeniu do zdjęcia AP czaszki płaszczyzna
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Standardowe badanie urografii polega na podaniu pacjentowi środka kontrastującego
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
Odprowadzenie II rejestruje różnicę potencjałów między
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
Na obrazie TK klatki piersiowej w przekroju poprzecznym strzałką oznaczono