Pytanie 1
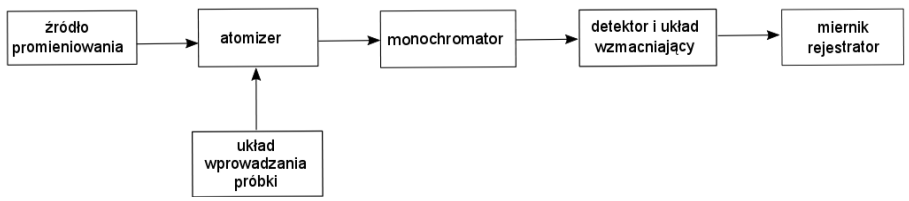
Na rysunku przedstawiono schemat blokowy
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Na rysunku przedstawiono schemat blokowy

Z analizy danych zawartych w tabeli wynika, że
| Tabela. Rodzaj paliwa stałego, zawartość węgla pierwiastkowego i wartość opałowa | ||||
|---|---|---|---|---|
| Rodzaj paliwa | Torf | Węgiel brunatny | Węgiel kamienny | Antracyt |
| Zawartość C, % | 55 – 63 | 63 – 76 | 80 – 90 | 93 – 98 |
| Wartość opałowa, MJ/kg | 21 – 24 | 26 – 32 | 30 – 35 | 36 |
Obecność wiązań podwójnych w cząsteczkach nienasyconych kwasów tłuszczowych powoduje, że zazwyczaj mają one
Proces kondensacji i osuszania substancji termolabilnych, takich jak białka oraz kwasy nukleinowe, za pomocą suszenia zamrożonego materiału w obniżonym ciśnieniu poprzez sublimację lodu, określany jest jako
Jakie składniki odżywcze w żywności są identyfikowane za pomocą odczynników Fehlinga I i II?
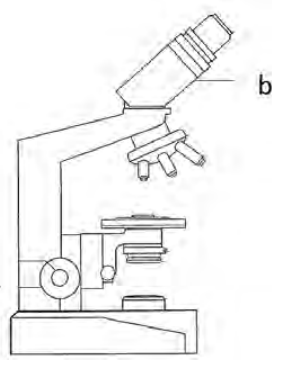
Na rysunku przedstawiającym schemat mikroskopu optycznego literą b oznaczono
W zamieszczonym opisie przedstawiono fragment instrukcji obsługi
| Umieść probówki w adapterach. Zawsze umieszczaj probówki symetrycznie celem prawidłowego wyważenia rotora. W przypadku użycia tylko jednej probówki niezbędne jest umieszczenie przeciwwagi po stronie przeciwnej. Po zamknięciu pokrywy zostaje ona automatycznie zablokowana ... |
Aby przygotować podłoże do badań mikrobiologicznych, należy
Przed każdym pomiarem pryzmaty refraktometru powinny być starannie oczyszczone
Jakie jest zastosowanie psychrometru aspiracyjnego?
Metoda obrączkowa jest wykorzystywana do rozpoznawania jonu
Jaki wskaźnik jest używany do oceny kontaktu między wodami naturalnymi a fekaliami?
Woda obecna w cząsteczce Ca(OH)2 określana jest jako woda
Reakcja jonów SCN- z jonami o krwistoczerwonym zabarwieniu prowadzi do powstawania związków kompleksowych
Ile wynosi mnożnik analityczny żelaza oznaczanego wagowo w postaci Fe2O3?
| MFe = 55,845 g/mol | MFe2O3 = 159,687 g/mol |
Część opisu skutków analizy
(...) generuje kation jednowartościowy, a sole powstałe z tym kationem to w przeważającej mierze substancje trudnorozpuszczalne. Większość jego soli jest bezbarwna. Ten bezbarwny jon ma zdolność do tworzenia jonów kompleksowych, na przykład z tiosiarczanem sodowym. Związki tego kationu są wrażliwe na światło (ciemnieją pod jego działaniem), dlatego powinny być przechowywane w pojemnikach z ciemnego szkła (...) Z opisu wynika, że w analizowanym surowcu jakościowo oznaczano kation
Przeprowadzono elektrolizę wodnych roztworów elektrolitów, a wyniki zapisano w zamieszczonej tabeli.
Elektrolizie poddano roztwory oznaczone numerami:
| Produkt wydzielający się na katodzie | wodór | wodór | wodór |
| Produkt wydzielający się na anodzie | chlor | tlen | tlen |
| Odczyn roztworu w elektrolizerze | stał się zasadowy | pozostał zasadowy | pozostał kwasowy |
| 1 | 2 | 3 | 4 | 5 | 6 |
| CuSO4 | Na2SO4 | H2SO4 | HCl | NaCl | NaOH |
Który sprzęt laboratoryjny przedstawiono na ilustracji?

Dostanie się do środowiska pałeczek Salmonella, hodowanych na podłożach mikrobiologicznych, skutkuje
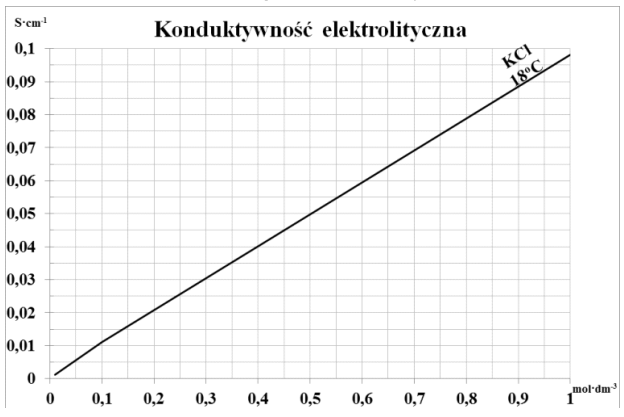
W celu wyznaczenia stężenia badanej próbki chlorku potasu, wykonano krzywą wzorcową zależności konduktywności elektrolitycznej od stężenia. Przewodność badanego roztworu wyniosła 0,045 S∙cm-1. Stężenie badanego roztworu KCl wynosi
Iloczyn rozpuszczalności trudno rozpuszczalnego związku Ca3(PO4)2 wyrażony jest równaniem:
| A. | KSO = [Ca2+] · [PO43-] |
| B. | KSO = [Ca3+]2 · [PO42-]3 |
| C. | KSO = [Ca2+]3 · [PO43-]2 |
| D. | KSO = 3[Ca2+] · 2[PO43-] |
Jaką objętość rozcieńczalnika zużyto na przygotowanie wskazanego w opisie rozcieńczenia próbki mleka?
| Wykonać dziesiętne rozcieńczenia mleka z 10 cm3 próbki. Pierwsze rozcieńczenie wykonać w kolbie o pojemności 250 cm3: do 90 cm3 rozcieńczalnika dodać 10 cm3 próby, dokładnie wymieszać; z tego rozcieńczenia pobrać 0,5 cm3 i przenieść do 4,5 cm3 rozcieńczalnika. Postępować w ten sam sposób, aż do uzyskania rozcieńczenia 1:100000. |
W celu identyfikacji cukru przeprowadzono następujące doświadczenia:
Identyfikowanym cukrem jest
| Doświadczenie | Wynik doświadczenia |
|---|---|
| Próba Trommera | pozytywna |
| Próba Tollensa | pozytywna |
| Hydroliza | nie zachodzi |
Aby utrzymać stałe pH roztworu miareczkowanego w analizach kompleksometrycznych, należy zastosować roztwory buforowe, które charakteryzują się
W wodzie do picia identyfikacja stężenia jonów Fe3+ może być zrealizowana
Czym są lipidy złożone?
Na podstawie informacji zawartych w tabeli wskaż, który adsorbent należy zastosować podczas oznaczania karotenów.
| Podział adsorbentów według zastosowania | |
|---|---|
| Adsorbent | Przykłady zastosowania |
| Tlenek glinu zasadowy | aminy, węglowodory, alkaloidy, zasady heterocykliczne |
| Tlenek glinu obojętny | aminy, amidy, alkaloidy, glikozydy |
| Tlenek glinu kwasowy | barwniki, związki kwasowe |
| Żel krzemionkowy | aminy, kwasy karboksylowe, amidy, węglowodory, inne związki obojętne |
W jakiej proporcji molowej EDTA reaguje z jonami Zn²⁺?
Przewodnictwo właściwe roztworu \( \text{KNO}_3 \) wynosi \( 8{,}9 \cdot 10^{-3} \, \text{S} \cdot \text{cm}^{-1} \). W jakiej odległości powinny być ustawione elektrody o powierzchni \( 5 \, \text{cm}^2 \), aby przewodnictwo roztworu wynosiło \( 5 \, \text{mS} \)?
Wzór do obliczeń:$$ \frac{1}{R} = G = \frac{\kappa \cdot S}{l} $$gdzie:
\( R \) – oznacza opór przewodnika
\( G \) – przewodnictwo elektryczne
\( \kappa \) – przewodnictwo właściwe
\( S \) – powierzchnia elektrod
\( l \) – odległość elektrod względem siebie
Na ilustracji przedstawiono schemat doświadczenia pozwalającego na zbadanie właściwości
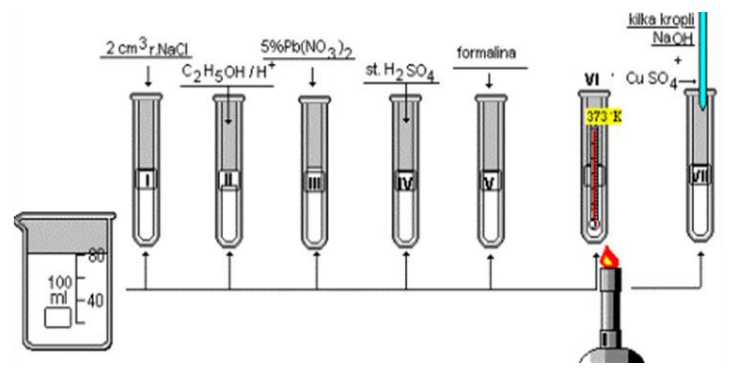
Metodą, którą można oznaczyć całkowitą zawartość siarki w paliwach stałych, jest
Jakie jednostki stosuje się do określenia tzw. indeksu nadmanganianowego, który symbolicznie reprezentuje ilość związków organicznych w wodzie pitnej?
Na podstawie zamieszczonych w tabeli informacji wskaż związek chemiczny, którego należy użyć w celu oddzielenia kationu Pb2+ z mieszaniny kationów grupy pierwszej.
| Pb2+ | Hg22+ | Ag+ |
| + rozc. HCl | ||
| PbCl2↓ | Hg2Cl2↓ | AgCl↓ |
| Dodać kilka kropli H2O, ogrzać na łaźni, odsączyć na gorąco | ||
| Pb2+ | Hg2Cl2↓ | AgCl↓ |
| + K2CrO4 | + NH3 aq | +stęż. NH3 aq |
Reakcja, na której opiera się oznaczenie liczby zmydlania (LZ) tłuszczów, to
W zamieszczonej ramce przedstawiono procedurę oznaczania
| Powierzchnię - suchą próbkę rozetrzeć w moździerzu, przesiać przez sito o średnicy oczek 1,25 mm i odważyć z niej 10 g w zlewce poj. 50 cm3. Do zlewki z próbką dodać 25 cm3 1-molowego roztworu KCl i energicznie mieszać, aż całość przejdzie w zawiesinę. Włączyć pH-metr, zanurzyć elektrody w zawiesinie i odczytać wartość na skali urządzenia. Pomiaru dokonać 3-krotnie, po każdym pomiarze przepłukując elektrody wodą destylowaną. Za wynik uznać średnią z trzech pomiarów obliczoną z dokładnością 0,05 pH. |
Czym charakteryzuje się barwa roztworu zawierającego jony Cr2O72-?
Na podstawie danych zawartych w tabeli, wskaż zestaw substancji uporządkowanych według rosnącej temperatury topnienia.
| Substancja | pirydyna | benzen | etanol |
|---|---|---|---|
| Temperatura wrzenia [°C] | 115,5 | 80,1 | 78,3 |
| Temperatura topnienia [°C] | -41,6 | 5,5 | -114,1 |
Wyznacz refrakcję molową (Rm) dla kwasu octowego korzystając z danych zawartych w tabeli.
Rm = ∑a ∙ Ra gdzie: a – liczba atomów jednego rodzaju, Ra – refrakcja atomowa

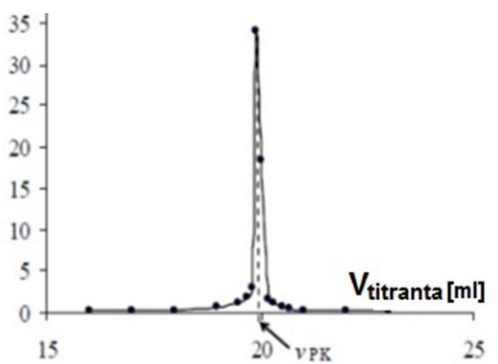
Na wykresie przedstawiono krzywą miareczkowania
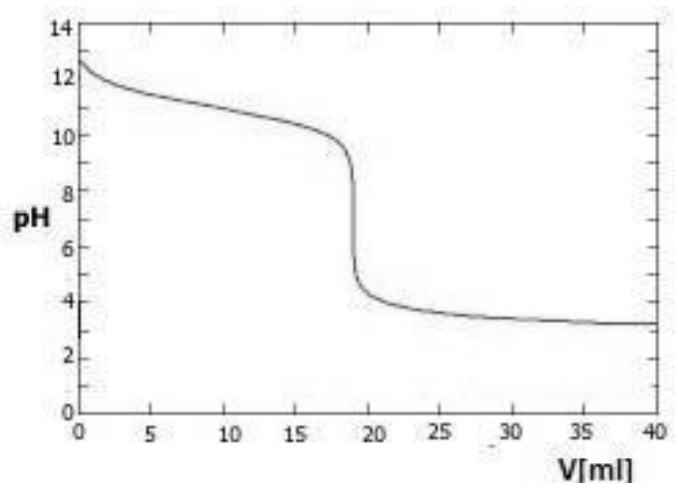
Sporządzono wykres potencjometrycznego miareczkowania alkacymetrycznego. W jaki sposób należy opisać oś Y?
| A. | ΔpH/ΔVtitranta |
| B. | ΔSEM/ΔVtitranta |
| C. | pH/ΔVtitranta |
| D. | SEM/ΔVtitranta |