Pytanie 1
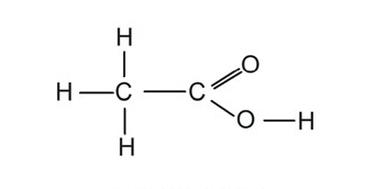
Związek o podanym wzorze to kwas
Wynik: 22/40 punktów (55,0%)
Wymagane minimum: 20 punktów (50%)
Związek o podanym wzorze to kwas

Zbiór próbek pierwotnych tworzy próbkę
Aby oczyścić zwęglone osady w probówce, należy zastosować
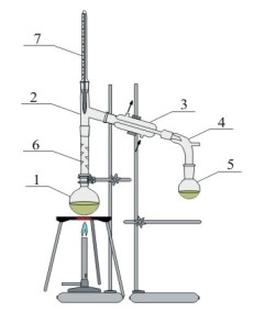
Oddzielanie płynnej mieszaniny wieloskładnikowej poprzez odparowanie, a następnie skraplanie jej komponentów, to proces
Jak nazywa się naczynie o płaskim dnie, które wykorzystuje się do pozyskiwania substancji stałej poprzez stopniowe odparowanie rozpuszczalnika z roztworu?
Odpady z rozpuszczalników organicznych, takich jak benzen czy aceton, zawierające co najmniej 80% danego rozpuszczalnika, należy
Poniżej jest równanie reakcji prażenia węglanu wapnia. 200 g węglanu wapnia zawierającego 10% zanieczyszczeń poddano prażeniu. Masa otrzymanego tlenku wapnia wyniosła
| CaCO3 → CaO + CO2 |
| (MCaCO3 = 100 g/mol, MCaO = 56 g/mol, MCO2 = 44 g/mol) |
Wody pobrane ze studni powinny być przewożone w szczelnie zamkniętych butelkach z przezroczystego materiału
Reagenty o czystości na poziomie 99,999% — 99,9999% to reagenty
Co oznacza zapis cz.d.a. na etykiecie opakowania odczynnika chemicznego?
Aby poprawić efektywność reakcji opisanej równaniem: HCOOH + C2H5OH ⇄ HCOOC2H5 + H2O, należy
Jakie jest stężenie molowe kwasu siarkowego(VI) o zawartości 96% i gęstości 1,84 g/cm3?
Jakie jest znaczenie skrótu: cz. na etykiecie reagentu chemicznego?
Która część małej partii materiału jest najczęściej pobierana w celu przygotowania próbki ogólnej?
Laboratoryjny stół powinien być zaopatrzony w instalację gazową oraz
Podczas przygotowywania roztworu mianowanego kwasu solnego o określonym stężeniu należy:
Jakie substancje są potrzebne do uzyskania nierozpuszczalnego wodorotlenku cynku?
Jaką objętość powinna mieć kolba miarowa, aby przygotować mianowany roztwór NaOH o stężeniu 0,050 M z analitycznej odważki, która zawiera 0,1 mola NaOH?
Ogólna próbka, jednostkowa lub pierwotna powinna
Na rysunku numerem 3 oznaczono
W którym z podanych równań reakcji dochodzi do zmiany stopni utlenienia atomów?
Które z wymienionych reakcji chemicznych stanowi reakcję redoks?
Aby uzyskać drobnokrystaliczny osad BaSO4, należy wykonać poniższe kroki:
Do zlewki wlać 20 cm3 roztworu BaCl2, następnie dodać 100 cm3 wody destylowanej oraz kilka kropli roztworu HCl. Zawartość zlewki podgrzać na łaźni wodnej, a potem, ciągle mieszając, dodać 35 cm3 roztworu H2SO4.
Mieszaninę ogrzewać na łaźni wodnej przez 1 godzinę. Osad odsączyć i przepłukać kilkakrotnie gorącą wodą zakwaszoną kilkoma kroplami roztworu H2SO4.
Według przedstawionej procedury, do uzyskania osadu BaSO4 potrzebne są:
Jakie procesy towarzyszy efekt egzotermiczny?
Który zestaw zawiera niezbędne urządzenia laboratoryjne do przygotowania 10% (m/m) roztworu NaCl?
Który z wskaźników nie jest używany w alkacymetrii?
Na rysunku przedstawiono wagę

Osoba pracująca z lotnym rozpuszczalnikiem straciła przytomność. Jakie działania należy podjąć, aby udzielić pierwszej pomocy?
W trakcie korzystania z odczynnika opisanego na etykiecie, należy szczególnie zwrócić uwagę na zagrożenia związane
Podczas pobierania skoncentrowanego roztworu kwasu solnego konieczne jest pracowanie w włączonym dygestorium oraz zastosowanie
Maksymalna średnica ziaren w partii substancji stałej wynosi 0,5 cm. Zgodnie z danymi zawartymi w tabeli próbka pierwotna tej substancji powinna mieć masę minimum
| Tabela. Masa próbki pierwotnej w zależności od wielkości ziaren lub kawałków | ||||
| Średnica ziaren lub kawałków [mm] | do 1 | 1 - 10 | 11 - 50 | ponad 50 |
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
Do wykrywania pierwiastków w niskich stężeniach w badaniach spektrograficznych należy używać reagentów
Roztwór amoniaku o stężeniu 25% nie powinien być trzymany
W karcie charakterystyki pewnej substancji znajduje się piktogram dotyczący transportu. Jest to substancja z grupy szkodliwych dla zdrowia

Do 200 g roztworu NaOH (M = 40 g/mol) o stężeniu 10 % dodano wodę destylowaną w kolbie miarowej o pojemności 500 cm3 do znaku. Jakie jest stężenie molowe powstałego roztworu?
300 cm3 zanieczyszczonego benzenu poddano procesowi destylacji. Uzyskano 270 cm3 czystej substancji. Jaką wydajność miało oczyszczanie?
W celu przeprowadzenia opisanego doświadczenia, należy przygotować:
| Opis procesu wydzielenia kwasu acetylosalicylowego z tabletek |
|---|
| Pięć rozgniecionych tabletek aspiryny (polopiryny) umieszcza się w kolbie stożkowej o pojemności 100 ml, dodaje 10 ml etanolu i ogrzewa na łaźni wodnej, aż do momentu rozpadnięcia się tabletek. W roztworze znajduje się kwas acetylosalicylowy, natomiast masa tabletkowa pozostaje w osadzie. Osad ten odsącza się na ogrzanym lejku szklanym zaopatrzonym w sączek karbowany. Do odebiornego przesączu dodaje się 20-30 ml zimnej wody destylowanej. Dodatek wody powoduje wypadanie osadu aspiryny z roztworu (zmniejsza się rozpuszczalność aspiryny w roztworze wodno-alkoholowym). Wydzielone kryształy odsączyć na lejku sitowym i suszyć na powietrzu. |
W próbkach obecne są składniki, które znacznie różnią się pod względem zawartości. Składnik, którego procentowy udział w próbce jest niższy od 0,01%, nazywamy
Metoda przygotowania próbki do badania, która nie jest
Z uwagi na higroskopijne właściwości tlenku fosforu(V) powinien on być przechowywany w warunkach bez dostępu