Pytanie 1
Proces wydobywania składnika z cieczy lub ciała stałego w mieszance wieloskładnikowej poprzez jego rozpuszczenie w odpowiednim rozpuszczalniku to
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Proces wydobywania składnika z cieczy lub ciała stałego w mieszance wieloskładnikowej poprzez jego rozpuszczenie w odpowiednim rozpuszczalniku to
Które z poniższych działań należy wykonać przed rozpoczęciem pracy z nowym szkłem laboratoryjnym?
Który z wymienionych roztworów NaOH, o określonych stężeniach, nie jest roztworem mianowanym?
Jak nazywa się naczynie o płaskim dnie, które wykorzystuje się do pozyskiwania substancji stałej poprzez stopniowe odparowanie rozpuszczalnika z roztworu?
Wskaż metodę rozdzielenia układu, w którym fazą rozproszoną jest ciało stałe, a fazą rozpraszającą gaz.
| faza rozproszona | faza rozpraszająca | ||
|---|---|---|---|
| gaz | ciecz | ciało stałe | |
| gaz | - | piana | piana stała |
| ciecz | aerozol ciekły | emulsja | emulsja stała |
| ciało stałe | aerozol stały | zol | zol stały |
Próbka wzorcowa to próbka
200 g soli zostało poddane procesowi oczyszczania poprzez krystalizację. Uzyskano 125 g czystego produktu. Jaką wydajność miała krystalizacja?
Wskaż zbiór substancji, które po rozpuszczeniu w wodzie stają się elektrolitami?
Jakie jest stężenie molowe kwasu siarkowego(VI) o zawartości 96% i gęstości 1,84 g/cm3?
Proces mineralizacji próbki, który polega na jej spopieleniu w piecu muflowym w temperaturze 300-500°C i rozpuszczeniu pozostałych resztek w kwasach w celu oznaczenia zawartości metali ciężkich, to mineralizacja
Substancja oznakowana za pomocą przedstawionych na rysunku piktogramów jest

Aby oddzielić mieszankę etanolu i wody, konieczne jest przeprowadzenie procesu
Stosunek masowy miedzi do siarki w siarczku miedzi(I) wynosi
| 16S Siarka 32 | 29Cu Miedź 63,55 |
Aby uzyskać roztwór 25 gramów CuSO4 w 50 gramach wody, konieczne jest podgrzanie mieszanki do temperatury w przybliżeniu
Podstawowy zestaw do filtracji, oprócz statywu i sączka, obejmuje
Aby przygotować mianowany roztwór KMnO4, należy odważyć wysuszone Na2C2O4 o masie zbliżonej do 250 mg, z dokładnością wynoszącą 1 mg. Jaką masę powinna mieć prawidłowo przygotowana odważka?
Różnica pomiędzy średnim wynikiem pomiaru a wartością rzeczywistą stanowi błąd
Metodą, która nie służy do utrwalania próbek wody, jest
Aby uzyskać Cr2O3, dichromian(VI) amonu został poddany rozkładowi. Po rozpoczęciu, egzotermiczna reakcja rozkładu przebiega samorzutnie.
(NH4)2Cr2O7 → Cr2O3 + 4 H2O + N2 Jak oceniasz zakończenie tej reakcji?
Jakie substancje wykorzystuje się do wykrywania obecności jonów chlorkowych w wodzie mineralnej?
Działanie podejmowane po pobraniu próbki wody, mające na celu zachowanie jej składu chemicznego podczas transportu, określa się mianem
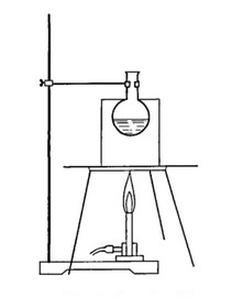
Jakie urządzenie jest wykorzystywane do procesu ekstrakcji?
Laboratoryjny stół powinien być zaopatrzony w instalację gazową oraz
Jakie roztwory chemiczne powinny być stanowczo pobierane przy włączonym dygestorium?
W jakiej standardowej temperaturze są kalibrowane szklane naczynia pomiarowe?
Oddzielanie płynnej mieszanki poprzez jej odparowanie, a potem skroplenie poszczególnych składników to
Skrót "cz." na etykiecie odczynnika chemicznego wskazuje, że
W próbkach obecne są składniki, które znacznie różnią się pod względem zawartości. Składnik, którego procentowy udział w próbce jest niższy od 0,01%, nazywamy
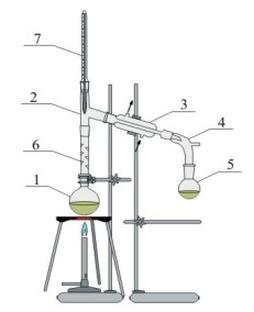
Zestaw przedstawiony na rysunku służy do
Substancje pomocnicze wykorzystywane do realizacji podstawowych analiz jakościowych i ilościowych, które nie wymagają wysokiej czystości, są oznaczane na opakowaniach symbolem
Maksymalna średnica ziaren w partii substancji stałej wynosi 0,5 cm. Zgodnie z danymi zawartymi w tabeli próbka pierwotna tej substancji powinna mieć masę minimum
| Tabela. Masa próbki pierwotnej w zależności od wielkości ziaren lub kawałków | ||||
| Średnica ziaren lub kawałków [mm] | do 1 | 1 - 10 | 11 - 50 | ponad 50 |
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
W parownicy porcelanowej, w której znajduje się 2,5 g naftalenu, umieść krążek bibuły z niewielkimi otworami oraz odwrócony lejek szklany. Zatyczkę lejka zrób z korka z waty. Parownicę umieść w płaszczu grzejnym. Po delikatnym ogrzaniu parownicy, pary substancji przechodzą przez otwory w bibule i kondensują na wewnętrznych ściankach lejka... Powyższy opis dotyczy metody oczyszczania naftalenu przez
Podczas pobierania próby wody do oznaczania metali ciężkich zaleca się stosowanie butelek wykonanych z:
Z 250 g benzenu (M = 78 g/mol) uzyskano 350 g nitrobenzenu (M = 123 g/mol). Jaka jest wydajność reakcji nitrowania?
Metoda oczyszczania substancji, która opiera się na różnicy w rozpuszczalności substancji docelowej oraz zanieczyszczeń w zastosowanym rozpuszczalniku, nosi nazwę
Roztwór, który jest dodawany z biurety w formie kropli do roztworu substancji, którą analizujemy, określamy mianem
Wagi laboratoryjne można klasyfikować według nośności oraz precyzji na
W jakim celu używa się kamyczków wrzenne w trakcie długotrwałego podgrzewania cieczy?
Do filtracji osadów drobnokrystalicznych wykorzystuje się filtry
Na rysunku przedstawiono ogrzewanie kolby z cieczą w łaźni