Pytanie 1
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
W medycynie nuklearnej wykorzystuje się:
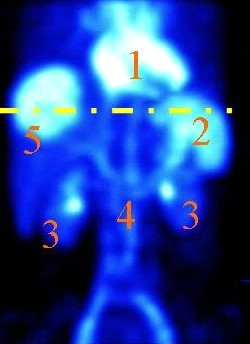
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?
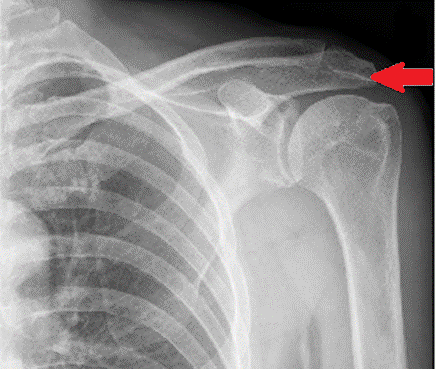
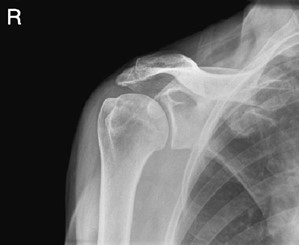
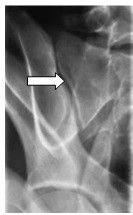
Na radiogramie stawu barkowego strzałką wskazano
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
W systemie międzynarodowym ząb pierwszy przedtrzonowy po stronie lewej oznacza się symbolem
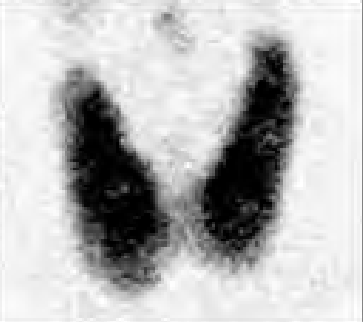
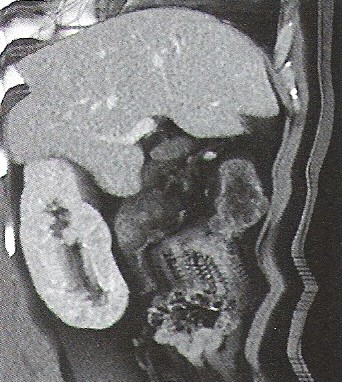
Na którym obrazie zarejestrowano badanie scyntygraficzne?
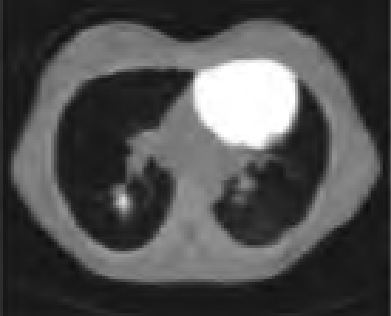
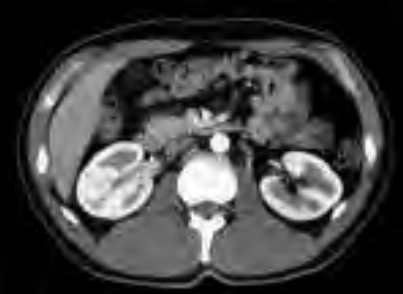
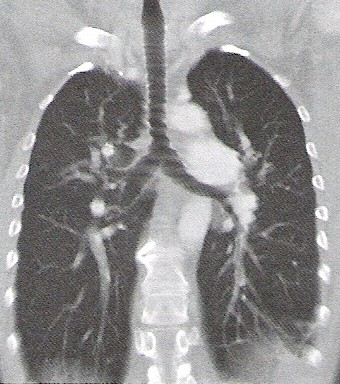
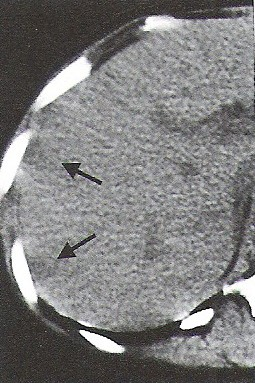
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Obrazowanie portalowe w radioterapii służy do
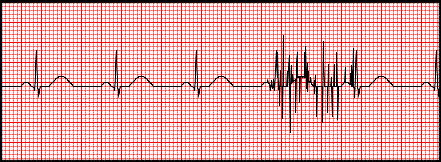
Artefakty zarejestrowane na elektrokardiogramie zostały wywołane przez
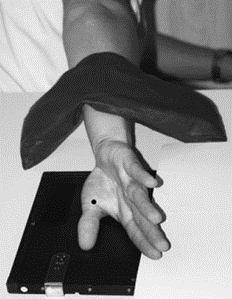
W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Na ilustracji przedstawiono ułożenie pacjenta do zdjęcia rentgenowskiego
Zamieszczony elektrokardiogram przedstawia
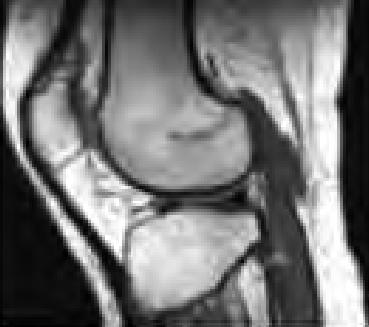
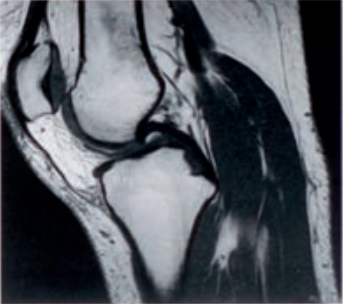
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Które urządzenia pomocnicze służą do unieruchomienia pacjenta do zabiegu radioterapii?
Jak konwencjonalnie frakcjonuje się dawkę w teleradioterapii?
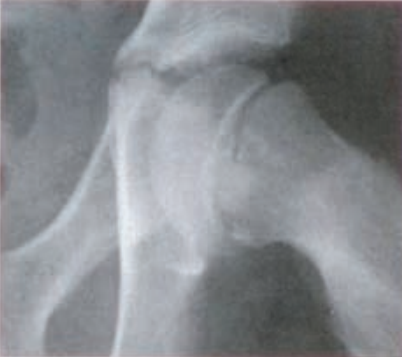
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
Radioizotopowa terapia medycyny nuklearnej polega na wprowadzeniu do tkanek lub narządów radiofarmaceutyku
„Ognisko zimne” w obrazie scyntygraficznym oznacza
W diagnostyce mammograficznej punktowy ucisk sutka stosuje się w projekcji
Na radiogramie uwidoczniono
Efekt „tea cup” widoczny jest na mammografach wykonanych w projekcji
Który radioizotop jest emiterem promieniowania alfa?
Którą strukturę anatomiczną zaznaczono strzałką na rentgenogramie?
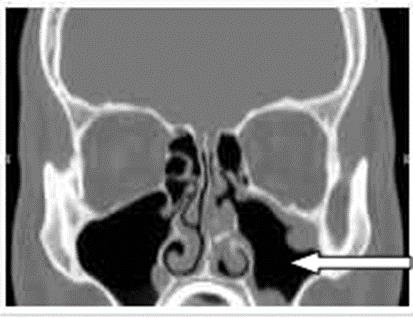
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
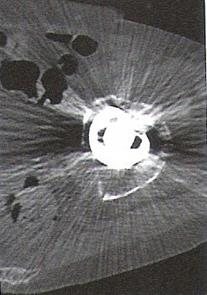
Zarejestrowany na obrazie TK artefakt jest spowodowany
Ligand stosuje się
Podczas badania EEG otwarcie oczu powoduje
Który załamek odzwierciedla repolaryzację komór w zapisie EKG?
DSA to cyfrowa
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
W radiografii mianem SID określa się
Rak drobnokomórkowy i rak niedrobnokomórkowy to postacie organiczne nowotworów złośliwych
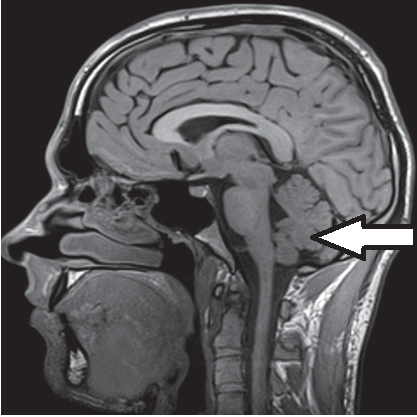
Którą strukturę anatomiczną oznaczono strzałką na obrazie rezonansu magnetycznego?