Pytanie 1
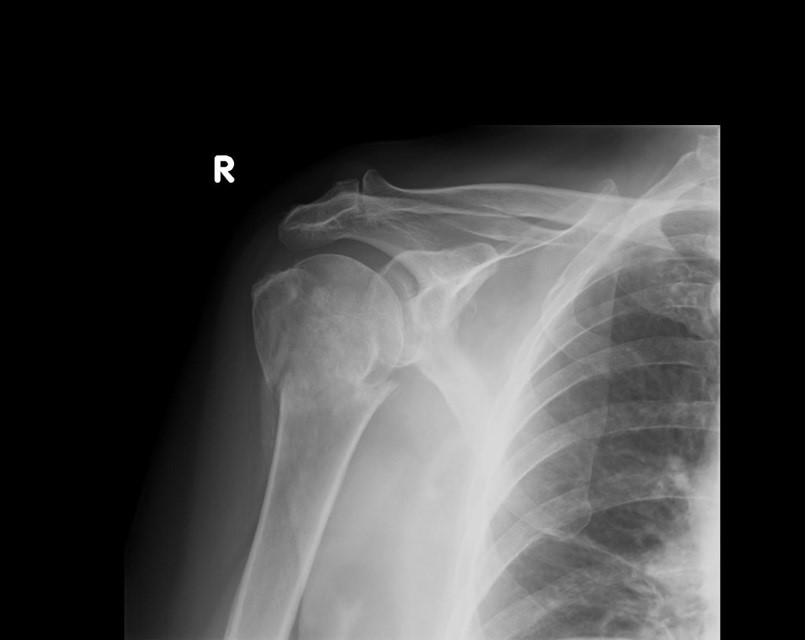
Zestaw rentgenogramów przedstawia
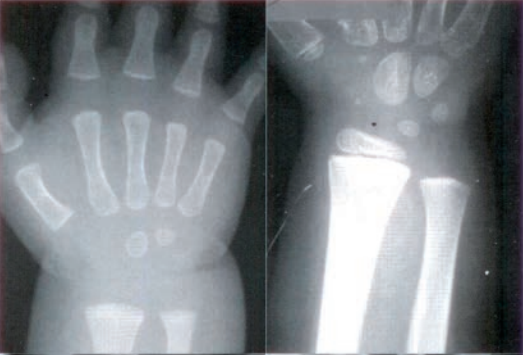
Wynik: 35/40 punktów (87,5%)
Wymagane minimum: 20 punktów (50%)
Zestaw rentgenogramów przedstawia

W radiografii mianem SID określa się
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
W zapisie EKG załamki P dodatnie w odprowadzeniu I i II, a ujemne w aVR oraz częstotliwość rytmu mniejsza niż 60/min wskazują na
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Na obrazie rezonansu magnetycznego głowy strzałką wskazano zatokę
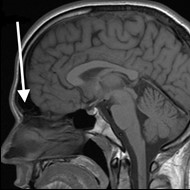
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Który obszar napromieniania w radioterapii oznacza się skrótem PTV?
Ligand stosuje się
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
W badaniu MR nadgarstka w ułożeniu na supermana pacjent leży na
Na rentgenogramie uwidoczniono badanie
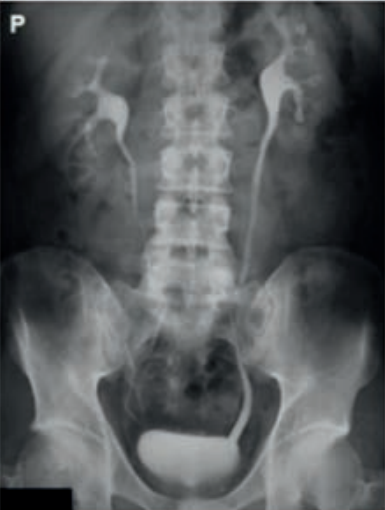
Na radiogramie uwidoczniono
Do zdjęcia prawych otworów międzykręgowych kręgosłupa szyjnego pacjent stoi w skosie
Kiedy w procesie terapii wykonuje się badanie CBCT (cone beam computed tomography)?
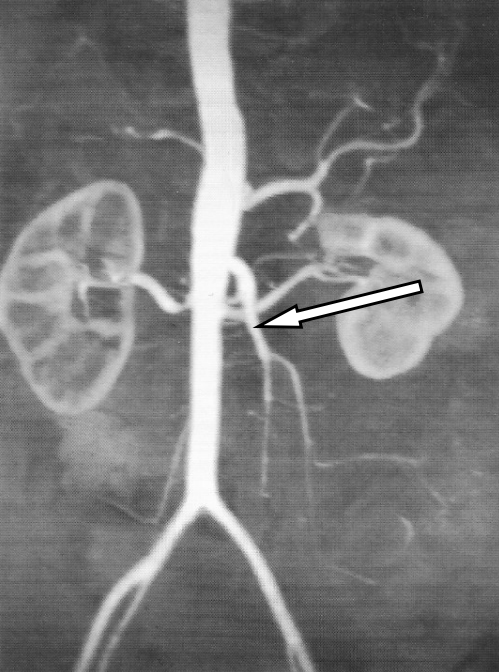
Którą tętnicę zaznaczono strzałką na obrazie MR?
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
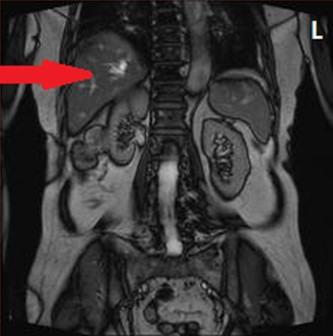
Na obrazie MR jamy brzusznej strzałką wskazano
W standardowym badaniu elektrokardiograficznym elektrodę C4 należy umieścić
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




Planowany obszar napromieniania PTV obejmuje
Strzykawka automatyczna do podawania kontrastu jest stosowana przy wykonywaniu
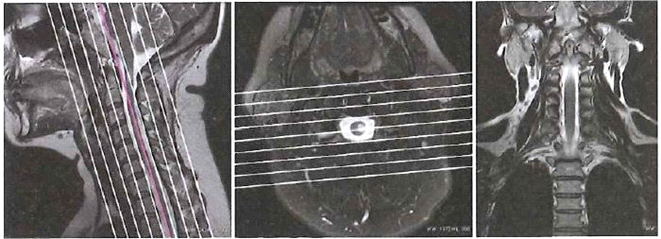
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
Który radiofarmaceutyk należy podać pacjentowi w scyntygrafii perfuzyjnej mózgu?
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

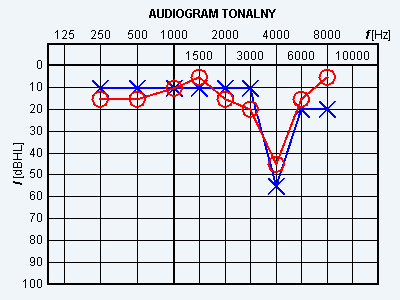
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
W brachyterapii MDR stosowane są dawki promieniowania
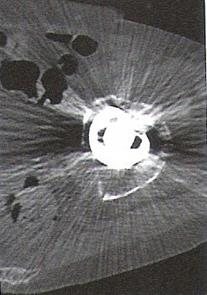
Zarejestrowany na obrazie TK artefakt jest spowodowany
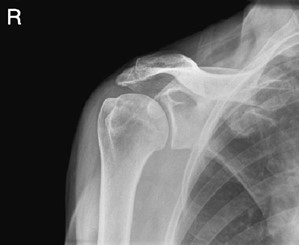
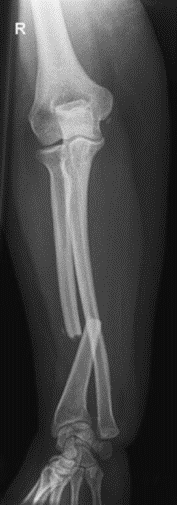
Na radiogramie uwidoczniono złamanie
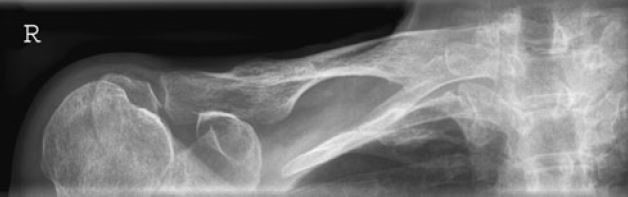
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
Czym charakteryzuje się późny odczyn popromienny?
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
Jak konwencjonalnie frakcjonuje się dawkę w teleradioterapii?
W których projekcjach wykonuje się standardowe badanie mammograficzne?
Jakie wiązki promieniowania emituje medyczny akcelerator liniowy?
Na zamieszczonym radiogramie strzałką oznaczono kość
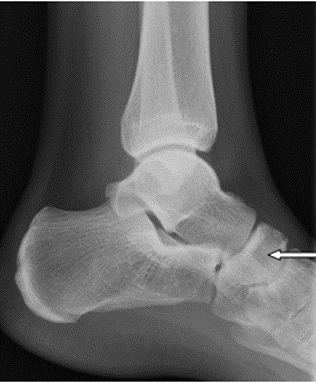
Na radiogramie uwidoczniono złamanie
Do środków kontrastujących negatywnych należą