Pytanie 1
Jakie zestawienie sprzętu laboratoryjnego wykorzystuje się do filtracji osadów?
Wynik: 32/40 punktów (80,0%)
Wymagane minimum: 20 punktów (50%)
Jakie zestawienie sprzętu laboratoryjnego wykorzystuje się do filtracji osadów?
Jaką próbkę stanowi woreczek gleby pobranej zgodnie z instrukcją?
| Instrukcja pobierania próbek glebowych | |
| Próbki pierwotne pobiera się laską glebową z wierzchniej warstwy gleby 0-20 cm, kolejno wykonując czynności: – w miejscu pobierania próbki pierwotnej (pojedynczej), rolę świeżo zaoraną przydeptać, – pionowo ustawić laskę do powierzchni gleby, – wcisnąć laskę do oporu (na wysokość poprzeczki ograniczającej), – wykonać pełny obrót i wyjąć laskę, – zawartość wgłębienia (zasobnika) przenieść do pojemnika skrobaczki. Po pobraniu próbek pojedynczych, całość wymieszać i napełnić kartonik lub woreczek. | |
Jakie procesy towarzyszy efekt egzotermiczny?
Podczas przewozu próbek wody, które mają być badane pod kątem właściwości fizykochemicznych, zaleca się, aby te próbki były
W celu sprawdzenia stężenia kwasu siarkowego(VI) odważono 1 g badanego kwasu i przeprowadzono analizę miareczkową, w której zużyto 20,4 \( \text{cm}^3 \) roztworu NaOH.
Stężenie procentowe badanego kwasu, obliczone na podstawie wzoru wynosi
$$ C_p = \frac{0,02452 \cdot V_{NaOH}}{mp} \cdot 100\% $$gdzie:
\( C_p \) – stężenie procentowe badanego kwasu; \( \% \)
\( 0,02452 \) – współczynnik przeliczeniowy; \( \text{g/cm}^3 \)
\( V_{NaOH} \) – objętość roztworu NaOH, zużyta w miareczkowaniu; \( \text{cm}^3 \)
\( mp \) – odważka badanego kwasu; g
Jakie narzędzie w laboratorium jest wykorzystywane do rozdrabniania małych ilości substancji stałych?
Skrót "cz." na etykiecie odczynnika chemicznego wskazuje, że
Podstawowy zestaw do filtracji składa się ze statywu oraz
Analiza technicznego kwasu solnego dała następujące wyniki: 30% HCl, 0,008% H2SO4, 0,04% Fe.
Korzystając z zamieszczonej tabeli wymagań, określ gatunek kwasu, pamiętając, że decyduje o nim najgorszy wskaźnik.
| Wymagania chemiczne dotyczące kwasu siarkowego | ||||
| Wymagania | Gatunki | |||
| I | II | III | IV | |
| Chlorowodór, % | > 33 | > 29 | > 28 | > 27 |
| Kwas siarkowy(VI) w przel. na SO42-, % | < 0,009 | < 0,5 | < 1,6 | < 1,8 |
| Żelazo (Fe3+), % | < 0,005 | < 0,03 | < 0,03 | < 0,05 |
Która część małej partii materiału jest najczęściej pobierana w celu przygotowania próbki ogólnej?
W laboratoriach roztwór potasu dichromianu(VI) w stężonym kwasie siarkowym(VI) wykorzystuje się do
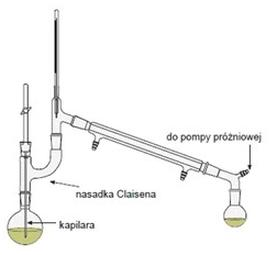
Przedstawiony na rysunku zestaw służy do destylacji
Na podstawie danych w tabeli próbkę, w której będzie oznaczany BZT, należy przechowywać
| Oznaczany parametr | Rodzaj naczynia do przechowywania | Sposób utrwalania | Dopuszczalny czas przechowywania |
|---|---|---|---|
| barwa | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C | 24 h |
| fosforany ogólne | szklane lub polietylenowe | - zakwaszenie kwasem siarkowym(VI) - schłodzenie do temperatury 2-5°C | 4 h 48 h |
| BZT | szklane | - schłodzenie do temperatury 2-5°C - przechowywanie w ciemności | 24 h |
| azot azotanowy(V) | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C - dodanie 2 cm3 chloroformu do 1 dm3 próbki | 24 h 48 h |
Na etykietach substancji chemicznych można znaleźć oznaczenia literowe R i S (zgodnie z regulacjami CLP: H i P), które wskazują
Czego się używa w produkcji z porcelany?
Jaką masę NaCl uzyskuje się poprzez odparowanie do sucha 250 g roztworu 10%?
Do kolby destylacyjnej wprowadzono 200 cm3 zanieczyszczonego acetonu o gęstości d = 0,9604 g/cm3 oraz czystości 90% masowych. W celu oczyszczenia przeprowadzono proces destylacji, w wyniku czego uzyskano 113,74 g czystego acetonu. Jakie były straty acetonu podczas destylacji?
Reagenty o najwyższej czystości to reagenty
W standardowym układzie destylacyjnym, który ma ukośną chłodnicę, wykorzystuje się chłodnicę
Jakie jest pH 0,001-molowego roztworu NaOH?
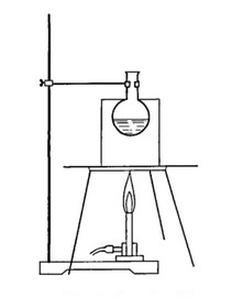
Na rysunku przedstawiono ogrzewanie kolby z cieczą w łaźni
Czystość konkretnego odczynnika chemicznego wynosi: 99,9-99,99%. Jakiego rodzaju jest ten odczynnik?
Wapno palone uzyskuje się poprzez prażenie wapienia według równania: CaCO3 → CaO + CO2. Ile kilogramów wapienia należy zastosować, aby w efekcie jego prażenia otrzymać 7 kg wapna palonego, jeśli wydajność reakcji wynosi 50%?
Masy molowe: MCa = 40 g/mol, MC = 12 g/mol, MO = 16 g/mol.
Jakie urządzenie jest wykorzystywane do oczyszczania próbki gazowej?
Aby zebrać próbki gazów, wykorzystuje się
Z analizy wykresu wynika, że substancją o najniższej rozpuszczalności w wodzie w temperaturze 100°C jest
Zestaw do filtracji pod obniżonym ciśnieniem powinien obejmować między innymi
Do wykrywania pierwiastków w niskich stężeniach w badaniach spektrograficznych należy używać reagentów
Do grupy reagentów o szczególnym zastosowaniu nie wlicza się
Ile węglanu sodu trzeba odmierzyć, aby uzyskać 200 cm3 roztworu o stężeniu 8% (m/v)?
Na skutek krystalizacji 18 g kwasu benzoesowego uzyskano 8 g czystego produktu. Jaką wydajność miała ta krystalizacja?
Przeprowadzono reakcję 13 g cynku z kwasem solnym zgodnie z równaniem: Zn + 2 HCl → ZnCl2 + H2↑. Otrzymano 1,12 dm3 wodoru (w warunkach normalnych). Masy molowe to: MZn = 65 g/mol, MH = 1g/mol, MCl = 35,5g/mol. Jaka jest wydajność tego procesu?
W wyniku rozkładu 100 g węglanu wapnia, otrzymano 25 g tlenku wapnia. Wydajność procentowa reakcji wynosi
| MCaCO3 = 100g / mol | MCaO = 56g / mol |
Preparaty zawierające KOH (tzw. żrący potaż), oznaczone są symbolem S 1/2. Na podstawie informacji zawartych w tabeli, określ zasady przechowywania tych preparatów.
| Numer zwrotu S | Warunki bezpiecznego stosowania | Numer zwrotu S | Warunki bezpiecznego stosowania |
|---|---|---|---|
| S1 | Przechowywać pod zamknięciem | S12 | Nie przechowywać pojemnika szczelnie zamkniętego |
| S2 | Chronić przed dziećmi | S13 | Nie przechowywać razem z żywnością, napojami i karmą dla zwierząt |
| S3 | Przechowywać w chłodnym miejscu | S15 | Przechowywać z dala od źródeł ciepła |
| S4 | Nie przechowywać w pomieszczeniach mieszkalnych | S16 | Nie przechowywać w pobliżu źródeł zapłonu – nie palić tytoniu |
Intensywna reakcja z FeCl3 jest wykorzystywana do identyfikacji
Sprzęt laboratoryjny przedstawiony na ilustracji stanowi element zestawu do

Transportuje się pobrane próbki wody do analiz fizykochemicznych
Odlanie cieczy z nad osadu to
Aby odcedzić galaretowaty osad, konieczne jest użycie sączka
Przykładem piany stałej jest
| faza rozproszona | faza rozpraszająca | ||
|---|---|---|---|
| gaz | ciecz | ciało stałe | |
| gaz | - | piana | piana stała |
| ciecz | aerozol ciekły | emulsja | emulsja stała |
| ciało stałe | aerozol stały | zol | zol stały |