Pytanie 1
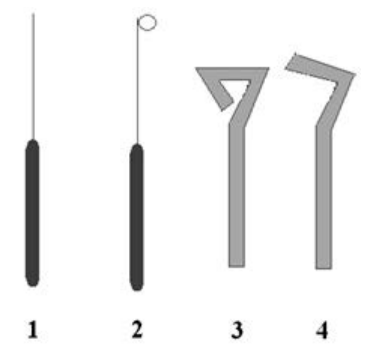
Schematyczny rysunek ezy, przyrządu używanego w laboratoriach mikrobiologicznych, został oznaczony na rysunku cyfrą
Wynik: 22/40 punktów (55,0%)
Wymagane minimum: 20 punktów (50%)
Schematyczny rysunek ezy, przyrządu używanego w laboratoriach mikrobiologicznych, został oznaczony na rysunku cyfrą

Część enzymu, która nie ma budowy białkowej i jest trwale związana z jego białkowym komponentem, nosi nazwę
Jakie składniki odżywcze w żywności są identyfikowane za pomocą odczynników Fehlinga I i II?
Czym charakteryzuje się barwa roztworu zawierającego jony Cr2O72-?
Dokładność metody definiowana jest na podstawie ustalonej wartości
Jakie urządzenie wykorzystuje się do pomiaru stężenia dwutlenku węgla, tlenku węgla oraz tlenu w atmosferze i w gazach spalinowych?
Czym są lipidy złożone?
Dostanie się do środowiska pałeczek Salmonella, hodowanych na podłożach mikrobiologicznych, skutkuje
Na zmiareczkowanie 10 cm3 roztworu KOH zużyto 10 cm3 0,1000-molowego roztworu H2SO4. Oblicz ilość KOH w badanej próbce w g/100 cm3.
| MK = 39 g/mol, MO = 16 g/mol, MH = 1 g/mol, MS = 32 g/mol |
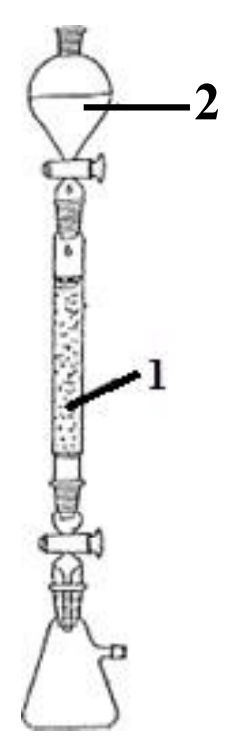
Na rysunku przedstawiono zestaw do chromatografii kolumnowej. Cyfrą 1 oznaczono
Do osadów amorficznych serowatych zalicza się
Zamieszczona instrukcja dotyczy wykonania preparatu mikroskopowego
| 1. Materiał nanieść na szkiełko podstawowe. 2. Po wyschnięciu, preparat utrwalić przez przeciągnięcie szkiełka podstawowego nad płomieniem palnika spirytusowego. 3. Następnie nanieść na szkiełko roztwór błękitu metylenowego i pozostawić do wyschnięcia. 4. Spłukać wodą destylowaną, pozostawić preparat do wyschnięcia. |
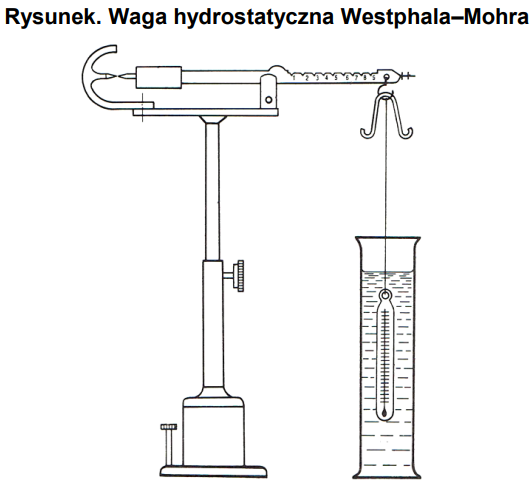
Którą właściwość fizyczną substancji można wyznaczyć za pomocą przyrządu przedstawionego na rysunku?
W ramce zamieszczono opis wykonania oznaczenia metodą
| Oznaczenie aktywności amylaz opiera się na pomiarze ilości rozpuszczonej skrobi, co określa się na podstawie zmiany intensywności zabarwienia w mieszaninie reakcyjnej, w skład której wchodzi jod. |
Związek chemiczny, który posiada skrót Gly-Ala-Leu-Ala-Tyr i został zidentyfikowany w trakcie badań analitycznych, to
Opisana metoda miareczkowania zaliczana jest do
| Ilościowe oznaczenie cukrów polega na redukcji soli miedzi(II) roztworem cukru, a następnie dodaniu do próbki roztworu KI i odmiareczkowaniu wydzielonego jodu mianowanym roztworem tiosiarczanu sodu |
Na rysunku przedstawiono aparat

Ile wynosi stężenie molowe roztworu CuSO4, którego absorbancja mierzona w kuwecie o grubości 20 mm ma wartość 0,90? Molowy współczynnik absorpcji s = 3000 dm3/molcm.

W celu wykonania posiewu redukcyjnego należy nanieść drobnoustroje na podłoże, a następnie
| A. | 1. wyżarzyć ezę, 2. obrócić szalkę, 3. ponownie nanosić drobnoustroje, zahaczając przynajmniej raz o wcześniejszą ścieżkę. |
| B. | 1. nie wyżarzać ezy, 2. obrócić szalkę, 3. ponownie nanosić drobnoustroje, zahaczając przynajmniej raz o wcześniejszą ścieżkę. |
| C. | 1. wyżarzyć ezę, 2. obrócić szalkę, 3. ponownie nanosić drobnoustroje, nie zahaczając ani razu o wcześniejszą ścieżkę. |
| D. | 1. wyżarzyć ezę, 2. pozostawić szalkę w tym samym miejscu, 3. ponownie nanosić drobnoustroje, zahaczając przynajmniej raz o wcześniejszą ścieżkę. |
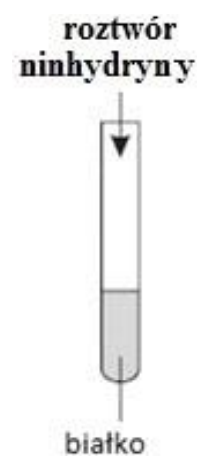
Przeprowadzono doświadczenie zgodnie ze schematem.
Roztwór w probówce zabarwił się na kolor
Spektrofotometria w podczerwieni (IR) to technika bazująca na absorpcji promieniowania w zakresie długości fal
Ilościowa analiza polegająca na dodawaniu równoważnej ilości roztworu odczynnika miareczkującego oraz precyzyjnym pomiarze jego objętości to analiza
Najczęściej wykorzystywanym odczynnikiem do barwienia próbek mikroskopowych jest
Zamieszczony opis dotyczy barwienia bakterii metodą
| − fiolet krystaliczny, 2-3 minuty, |
| − płyn Lugola, 1-2 minuty, |
| − alkohol aż do odbarwienia, ok. 30 sekund, |
| − woda – spłukanie, |
| − fuksyna w roztworze fenolowym (rozcieńczenie1:10), 20 sekund, |
| − woda – spłukanie |
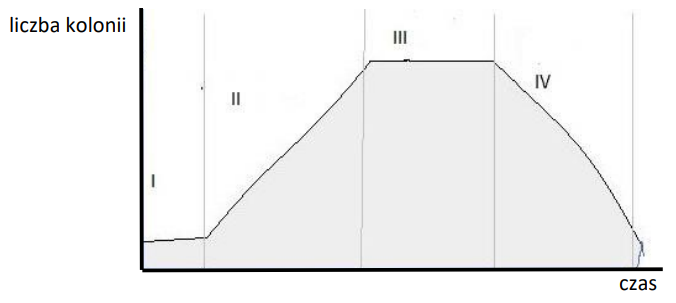
Na wykresie przedstawiającym krzywą wzrostu bakterii, cyfrą IV oznaczono fazę
Do oceny kwasowości mleka wykorzystuje się metodę miareczkowania
Na podstawie informacji zamieszczonych w tabeli wskaż wzór związku, który wytrąci się w postaci osadu.
| Badany kation | Odczynnik grupowy | NaOH | Barwienie płomienia |
|---|---|---|---|
| Mg2+ | brak | biały osad | |
| K+ | brak | fiołkowy | |
| Na+ | brak | żółty |
Dział analizy objętościowej, który dotyczy reakcji zobojętniania, to
Podczas miareczkowania kwasu octowego używając roztworu wodorotlenku sodu dochodzi do reakcji
Wśród substancji konserwujących stosowanych w żywności występują CH3COONH4 (E 264) oraz C6H5COONa (E 211). Związki te można określić jako
Podstawą klasyfikacji kationów w analizie jakościowej jest wydzielanie trudno rozpuszczalnych osadów?
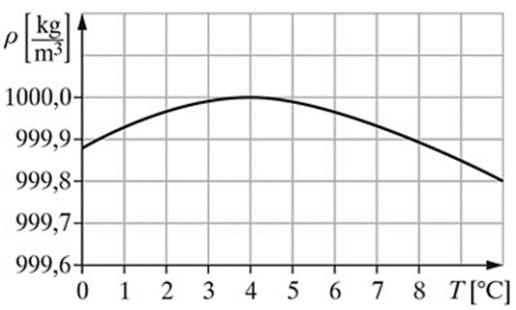
Na podstawie przedstawionego na rysunku wykresu zależności gęstości wody od temperatury, określ w jakiej temperaturze gęstość wody wynosi 1 g/cm3.
Próbkę żywności poddano ogrzewaniu w suszarce laboratoryjnej, a następnie obliczono X według wzoru. Wartość liczbowa X określa
$$ X = \frac{b - c}{a - c} \times 100\% $$gdzie:
\( a \) – masa naczyńka z badaną próbką przed ogrzewaniem [g]
\( b \) – masa naczyńka z badaną próbką po ogrzewaniu [g]
\( c \) – masa pustego naczyńka [g]
Metoda analityczna, która polega na wyznaczaniu masy osadzonej substancji z roztworu z wykorzystaniem azotanu(V) srebra, to
Jedna z analizowanych cech jakości wody ma wartość 0,8 NTU. Cechą tą jest
W mikrobiologicznych badaniach, dezynfekcja ma na celu eliminację
Podczas miareczkowania roztworu amoniaku o stężeniu 0,1 mol/dm3 za pomocą roztworu kwasu solnego o stężeniu 0,1 mol/dm3, skok krzywej leży w granicach pH 6,3–4,3. W tym miareczkowaniu jako wskaźnik należy zastosować
| Wskaźnik | Przedział pH |
| Błękit tymolowy | 1,2–2,8 |
| 8,0–9,6 | |
| Oranż metylowy | 3,1–4,4 |
| Czerwień metylowa | 4,2–6,2 |
| Błękit bromotymolowy | 6,7–7,6 |
| Fenoloftaleina | 8,0–9,8 |
| Tymoloftaleina | 9,3–10,5 |
Gdy podczas analizy ilościowej wyniki są zbliżone do wartości rzeczywistej, mówi się wtedy o
Jak nazywa się część białkowa enzymu?
Metodą, którą można oznaczyć całkowitą zawartość siarki w paliwach stałych, jest