Pytanie 1
Zarejestrowany na obrazie TK artefakt jest spowodowany
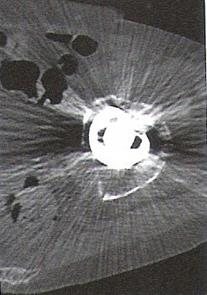
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Zarejestrowany na obrazie TK artefakt jest spowodowany

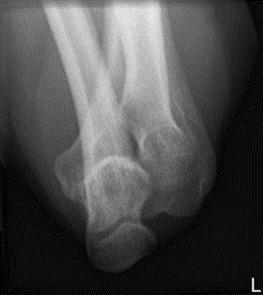
Na radiogramie uwidoczniono złamanie nasady
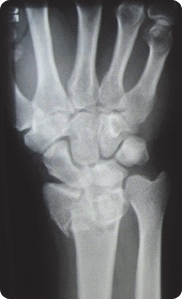
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
W standardowym badaniu elektrokardiograficznym elektrodę C4 należy umieścić
W obrazowaniu MR wykorzystuje się moment magnetyczny
Który załamek odzwierciedla szybką repolaryzację komór w zapisie EKG?
W systemie międzynarodowym ząb pierwszy przedtrzonowy po stronie lewej oznacza się symbolem
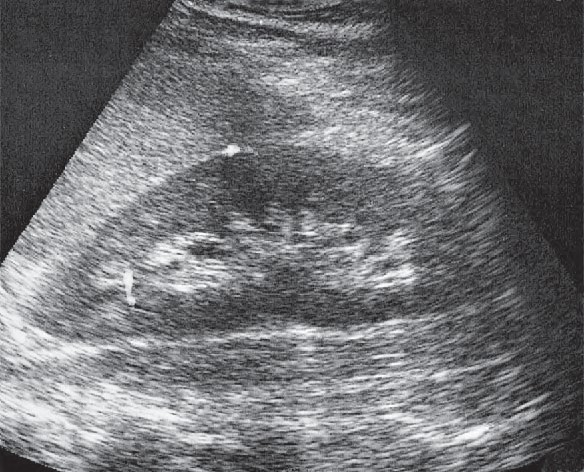
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
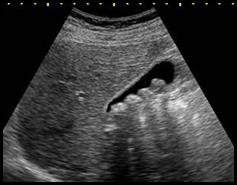
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
Badanie metodą Dopplera umożliwia
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
Na obrazie TK nadgarstka uwidocznione jest złamanie kości
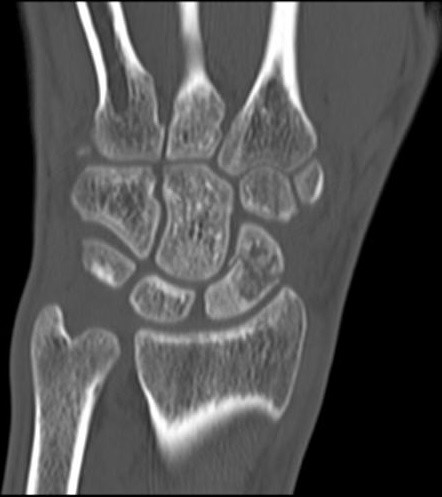
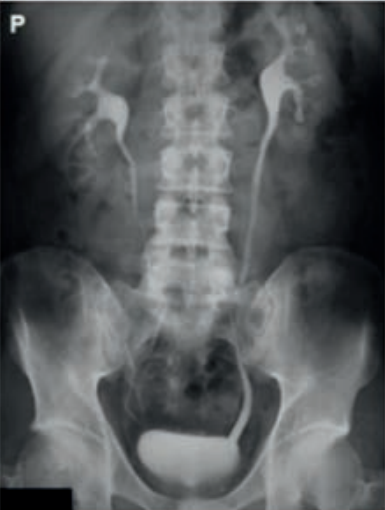
W badaniu cystografii wstępującej środek kontrastowy należy podać
W której próbie stroikowej przystawia się stroik do czoła (u podstawy nosa) lub na szczycie głowy i porównuje się przewodnictwo kostne ucha prawego i lewego?
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
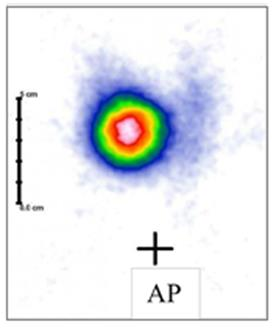
Na scyntygramie tarczycy uwidoczniono guzek
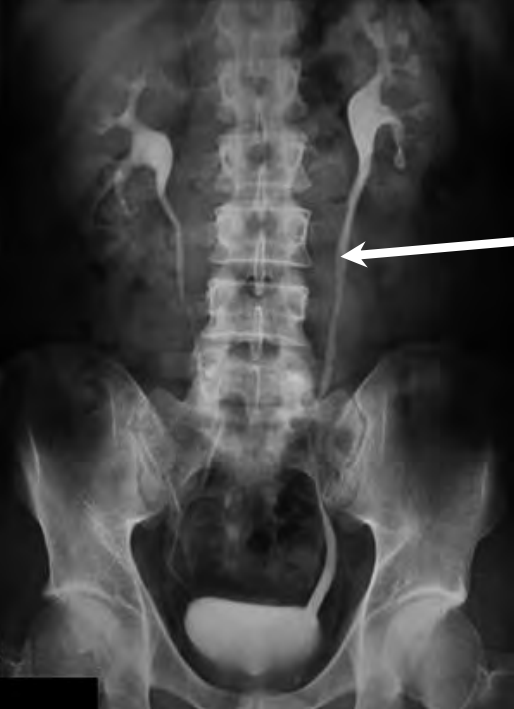
Na prawidłowo przedstawionym radiogramie badania kontrastowego strzałką zaznaczono
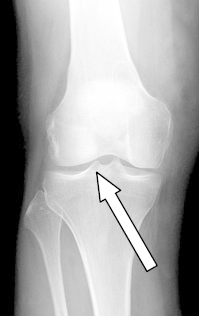
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
Ultrasonograficzne środki kontrastowe to
Fotostymulacja wykonywana jest podczas badania
Które informacje należy zamieścić na strzykawce z radiofarmaceutykiem przygotowanym przez technika elektroradiologa?
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Wyniosłość międzykłykciowa znajduje się na nasadzie
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
Do badania MR nadgarstka pacjenta należy ułożyć
Pojawienie się w zapisie EKG patologicznego załamka Q lub QS może wskazywać na
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
Który narząd widoczny jest na wydruku badania ultrasonograficznego?
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Na rentgenogramie uwidoczniono badanie
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Który środek ochrony radiologicznej pacjenta należy zastosować podczas wykonywania zdjęcia bocznego kręgosłupa szyjnego?
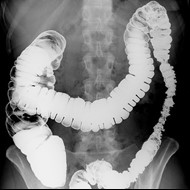
Przedstawiony obraz radiologiczny został zarejestrowany podczas badania jelita
Na prawidłowo wykonanym zdjęciu zatok w projekcji PA górny zarys piramid rzutuje się
W której projekcji należy wykonać badanie radiologiczne kręgosłupa lędźwiowego, by na otrzymanym zdjęciu wyrostki kręgów lędźwiowych układały się w charakterystyczny kształt piesków (teriera szkockiego)?
Którym skrótem w badaniu spirometrycznym oznaczana jest pojemność życiowa płuc?
DSA to cyfrowa