Pytanie 1
W trakcie oznaczania ChZT wody, określanego jako utlenialność, substancją utleniającą jest
Wynik: 15/40 punktów (37,5%)
Wymagane minimum: 20 punktów (50%)
W trakcie oznaczania ChZT wody, określanego jako utlenialność, substancją utleniającą jest
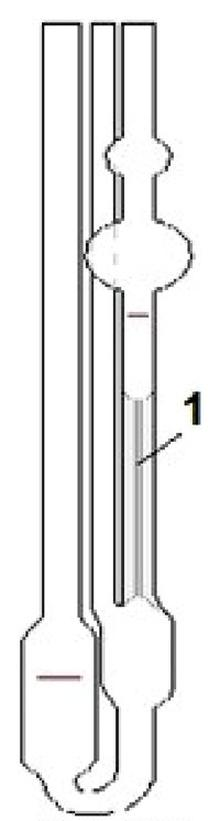
Na rysunku przedstawiającym wiskozymetr Ubbelohdego cyfrą 1 oznaczono
Drobnoustroje posiadające zdolność do rozkładu białek oraz peptydów charakteryzują się właściwościami
Badanie organoleptyczne wody przeznaczonej do ludzkiego spożycia obejmuje określenie
Który z poniższych związków chemicznych (w odpowiednio przygotowanej postaci roztworu) stanowi odczynnik grupowy dla kationów IV grupy?
Próbkę żywności poddano ogrzewaniu w suszarce laboratoryjnej, a następnie obliczono X według wzoru:
$$ X = \frac{b - c}{a - c} \times 100\% $$gdzie:
\( a \) – masa naczynia z badaną próbką przed ogrzewaniem [g]
\( b \) – masa naczynia z badaną próbką po ogrzewaniu [g]
\( c \) – masa pustego naczynia [g]
Wartość liczbowa X określa
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
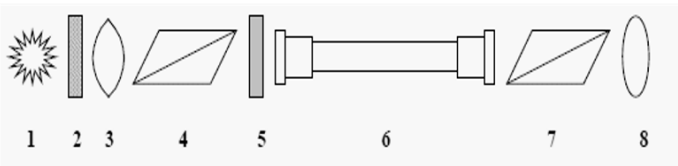
Na rysunku przedstawiającym schemat polarymetru, cyfrą 4 oznaczono
Oznaczono LZ i LJ dla czterech różnych próbek tłuszczów. Wyniki zestawiono w tabeli. Na podstawie zamieszczonych danych o liczbach właściwych wybranych tłuszczów wskaż próbkę, którą stanowi olej rzepakowy.
| Liczby właściwe wybranych tłuszczów | ||
|---|---|---|
| Rodzaj tłuszczu | Liczba zmydlania (LZ) mg KOH / g tłuszczu | Liczba jodowa (LJ) g I₂ / 100 g tłuszczu |
| Olej lniany | 187 – 197 | 169 – 192 |
| Olej sojowy | 188 – 195 | 114 – 138 |
| Olej rzepakowy | 167 – 179 | 94 – 106 |
| Tran wielorybi | 170 – 202 | 102 – 144 |
| Masło krowie | 218 – 245 | 25 – 38 |
| Smalec wieprzowy | 193 – 200 | 46 – 66 |
| Próbka | Liczba zmydlania (LZ) | Liczba jodowa (LJ) |
|---|---|---|
| 1 | 190 | 140 |
| 2 | 171 | 99 |
| 3 | 194 | 105 |
| 4 | 195 | 60 |
Na rysunku przedstawiono izolację czystych kultur bakterii metodą

Zawartość nadtlenków w oleju rzepakowym nie powinna przekraczać 5 milirównoważników aktywnego tlenu na 1 kg tłuszczu. Wartość ta, gdy jest wyższa, oznacza
Zamieszczone w tabeli dane techniczne dotyczą
| Specyfikacja urządzenia | |
|---|---|
| zakres pH | od -2,00 do 16,00pH |
| zakres temperatury | od -9,9 do 120,0 C |
| rozdzielczość: pH | 0,01pH |
| rozdzielczość temperatury | 0,1°C |
| kalibracja | automatyczna 1 lub 2 punktowa z 5 buforami |
| elektroda | szklana HI 1131B, elektrolitowa, kabel 1m |
| wymiary | 240*182*74mm |
| waga | 1,1kg |
Zgodnie z klasyfikacją Bunsena, aniony przypisywane są do jednej z 7 grup analitycznych na podstawie różnic w ich zachowaniu względem jonów
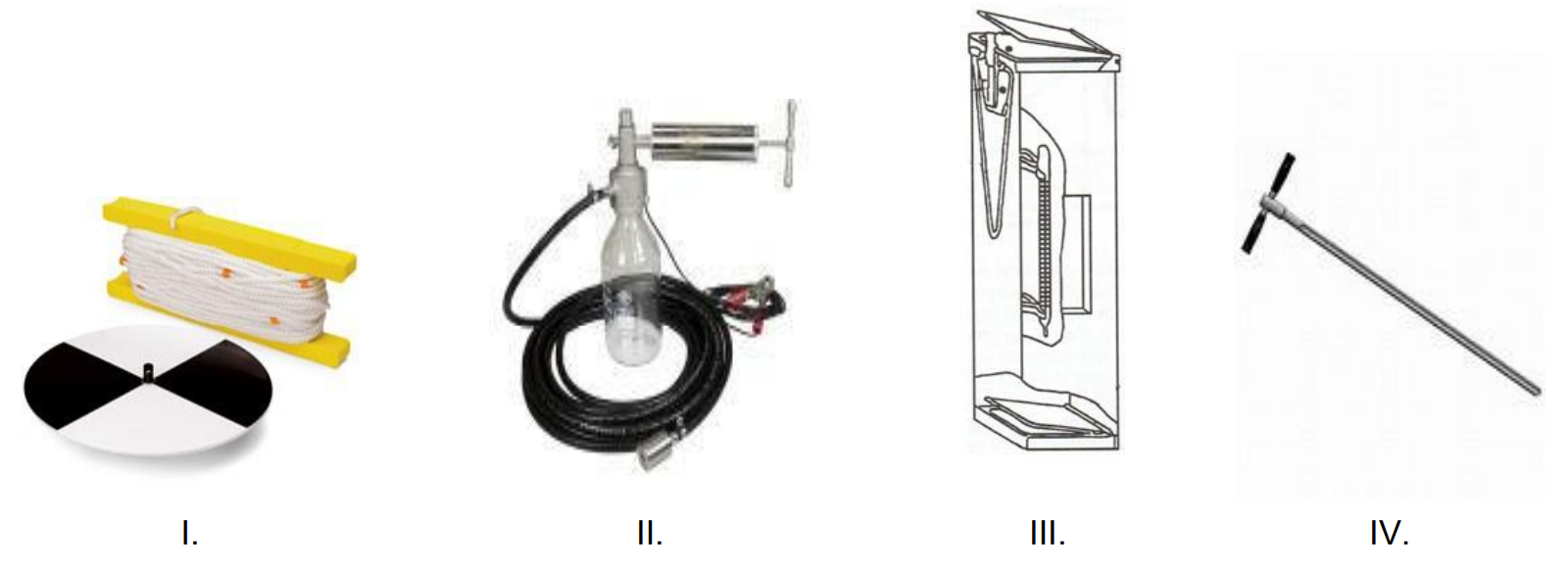
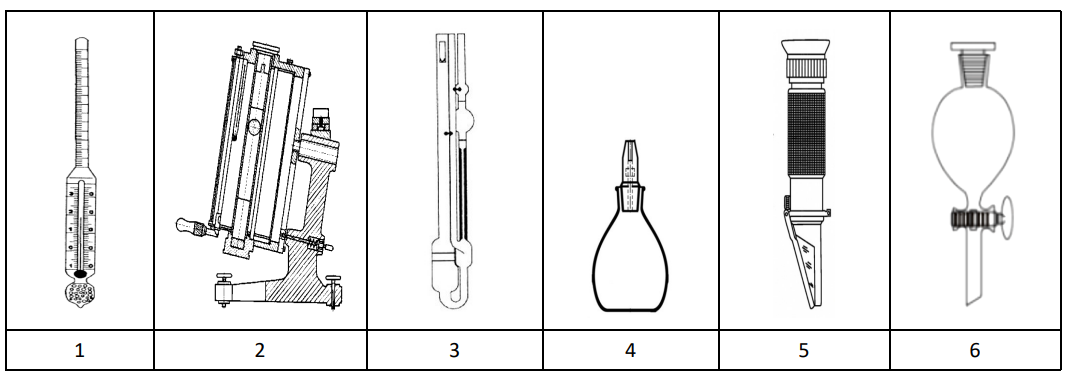
Do wyznaczania gęstości cieczy służą przyrządy oznaczone numerami
Gdzie wykorzystuje się efekt Tyndalla?
Stosunek masy proszku luźno nasypanego do objętości, którą ten proszek zajmuje, definiuje gęstość
W temperaturze 40°C lepkość oleju napędowego wynosi 3 mm2/s. Jakiego rodzaju lepkość to reprezentuje?
Na podstawie zamieszczonego fragmentu opisu wykonania ćwiczenia ustal, który wskaźnik jakości wody jest określany.
| Oznaczenie polega na określeniu ilości tlenu zużywanej do utleniania substancji organicznych w badanej próbce w ciągu n dób inkubacji w temperaturze 20°C. Ilość tę, w przeliczeniu na 1 dm³ wody, oblicza się jako różnicę zawartości tlenu przed i po inkubacji próbki. |
Parametr jakości wody, który wskazuje minimalną objętość w cm3, w której może znajdować się jedna komórka bakterii Escherichia coli lub innych pokrewnych bakterii żyjących w jelitach człowieka, określa się mianem
W tabeli przedstawiono kolejne etapy barwienia preparatu mikroskopowego metodą
| Etap 1 | Nałożenie barwnika – fioletu krystalicznego. |
| Etap 2 | Nałożenie płynu Lugola. |
| Etap 3 | Naniesienie alkoholu. |
| Etap 4 | Naniesienie barwnika – fuksyny zasadowej. |
Czym zajmuje się System Analizy Zagrożeń i Krytycznych Punktów Kontroli (HACCP)?
Jaką metodę kontroli stanu mikrobiologicznego powietrza opisano w zamieszczonej informacji?
| Otwarte płytki Petriego z podłożem stałym pozostawiono na 30 minut na wysokości 1 metra od podłogi, a następnie inkubowano przez 48 godzin w temperaturze 37°C. Po tym czasie wyhodowane kolonie zliczono i zidentyfikowano ich szczepy. |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Roztwór K2CrO4 jest używany jako wskaźnik przy oznaczaniu chlorków w metodzie Mohra. Powoduje on zmianę koloru mieszaniny reakcyjnej, co jest skutkiem
Jaką metodą można ustalić ilość tłuszczów w produktach pochodzenia roślinnego?
Wzrost dyfuzyjny bakterii w hodowli płynnej przedstawia probówka oznaczona na rysunku jako

Analiza wody basenowej w celu wykrycia bakterii polega na podgrzewaniu próbki w inkubatorze przez 48 godzin w temperaturze 36±2°C. Jaki proces jest opisany?
W analizie najczęściej oznacza się parametry CHZT i BZT
Z jaką precyzją należy zważyć próbkę o masie 20 mg, aby błąd względny nie wynosił więcej niż 0,05%?
Najczęściej wykorzystywanym odczynnikiem do barwienia próbek mikroskopowych jest
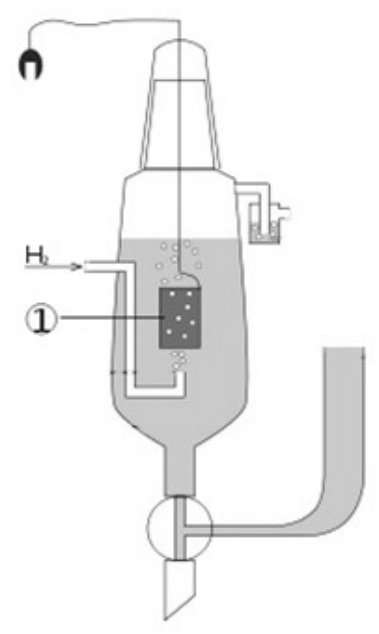
Na schemacie przedstawiającym elektrodę wodorową, cyfrą 1 oznaczono
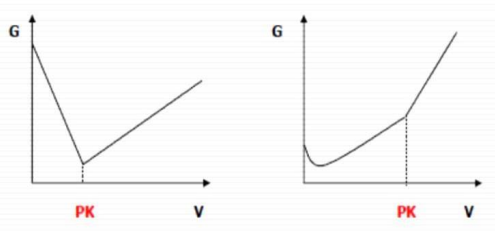
Zakończenie miareczkowania ustala się na podstawie pomiaru zmiany przewodnictwa roztworu poddanego miareczkowaniu w metodzie
Wykresy przedstawiają przebieg krzywych miareczkowania
Jaką metodę wykorzystuje się do wykrywania i pomiaru ilościowego substancji optycznie czynnych?
W celu wykonania posiewu redukcyjnego należy nanieść drobnoustroje na podłoże, a następnie
| A. | 1. wyżarzyć ezę, 2. obrócić szalkę, 3. ponownie nanosić drobnoustroje, zahaczając przynajmniej raz o wcześniejszą ścieżkę. |
| B. | 1. nie wyżarzać ezy, 2. obrócić szalkę, 3. ponownie nanosić drobnoustroje, zahaczając przynajmniej raz o wcześniejszą ścieżkę. |
| C. | 1. wyżarzyć ezę, 2. obrócić szalkę, 3. ponownie nanosić drobnoustroje, nie zahaczając ani razu o wcześniejszą ścieżkę. |
| D. | 1. wyżarzyć ezę, 2. pozostawić szalkę w tym samym miejscu, 3. ponownie nanosić drobnoustroje, zahaczając przynajmniej raz o wcześniejszą ścieżkę. |
Jakie kationy wchodzą w skład II grupy analitycznej?
Jakie właściwości cieczy określa areometr?
W trakcie oznaczania węglanu sodu przy użyciu wodorotlenku sodu metodą Wardera warto miareczkować próbkę od razu przy umiarkowanym mieszaniu, ponieważ mogą się rozpuszczać cząsteczki CO2 z atmosfery, co skutkuje
W ramce przedstawiono równania reakcji zachodzące podczas pośredniego jodometrycznego oznaczania
| 2Cu2+ + 4I- →2CuI + I2 I2 + S2O32- → 2I- + S4O62- |
Na którym rysunku przedstawiono sprzęt stosowany do pomiaru mętności wody?