Pytanie 1
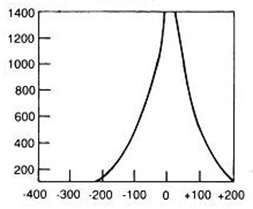
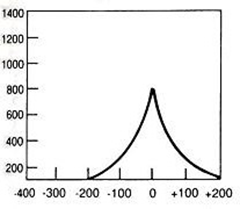
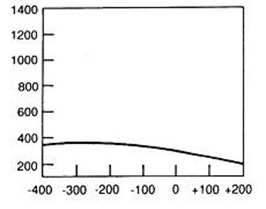
Ile razy i jak zmieni się wartość natężenia promieniowania X przy zwiększeniu odległości OF ze 100 cm do 200 cm?
Wynik: 18/40 punktów (45,0%)
Wymagane minimum: 20 punktów (50%)
Ile razy i jak zmieni się wartość natężenia promieniowania X przy zwiększeniu odległości OF ze 100 cm do 200 cm?
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
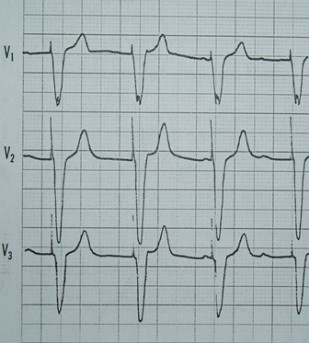
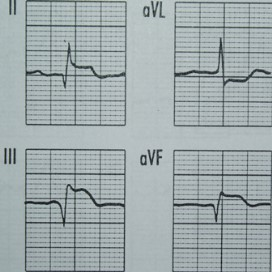
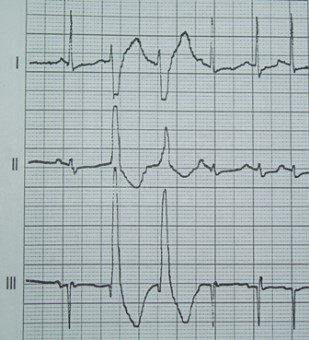
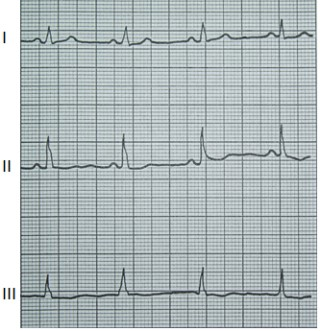
Przedstawiony zapis elektrokardiograficzny może wskazywać na
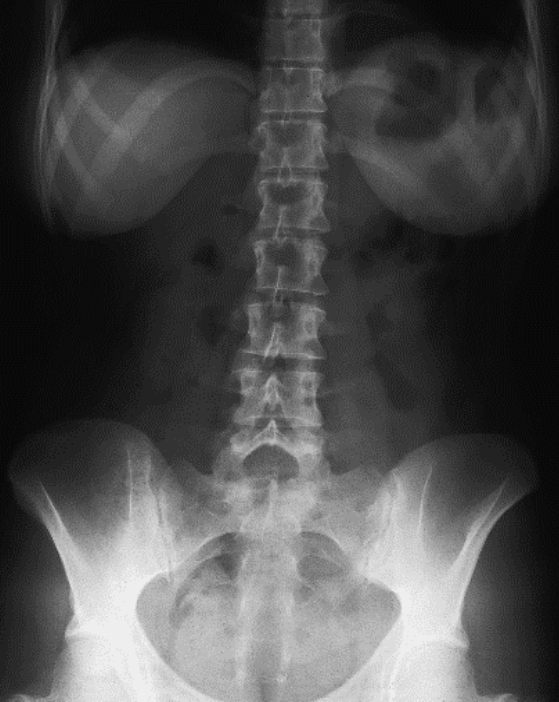
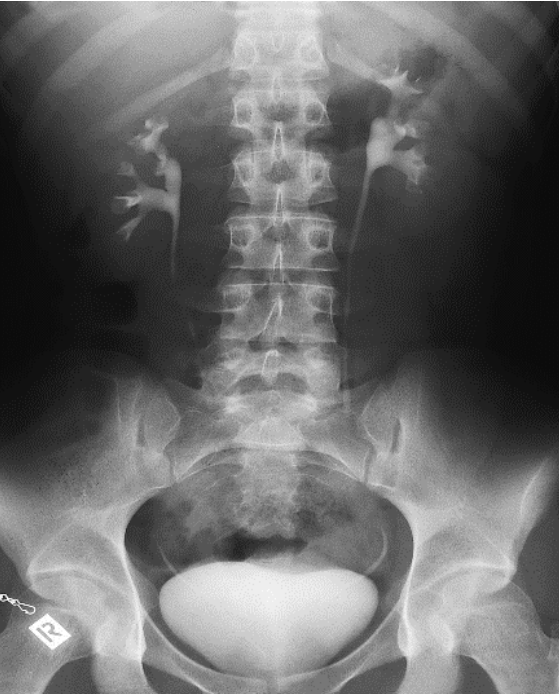
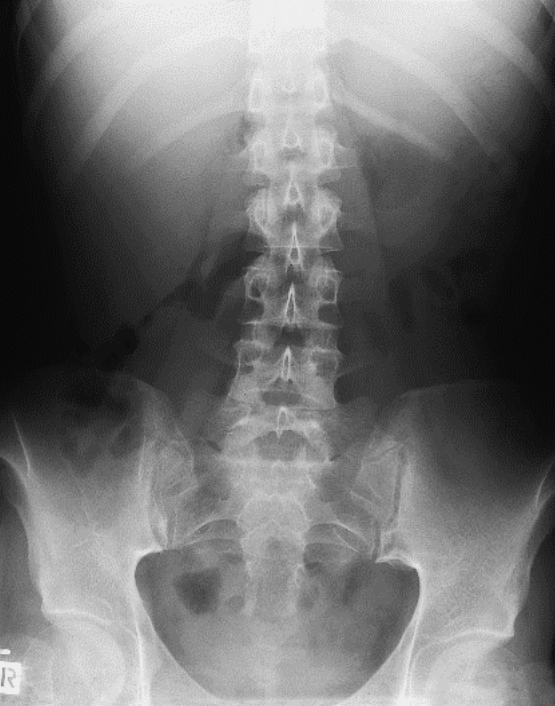
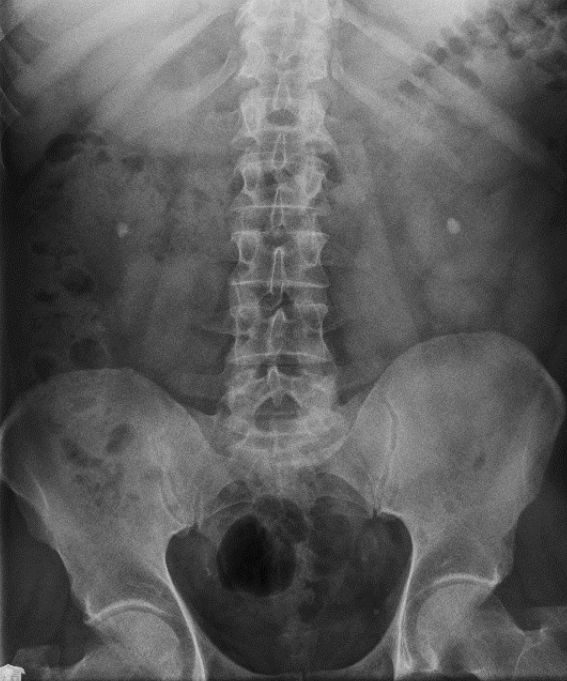
Na którym radiogramie uwidoczniona jest kamica nerkowa?
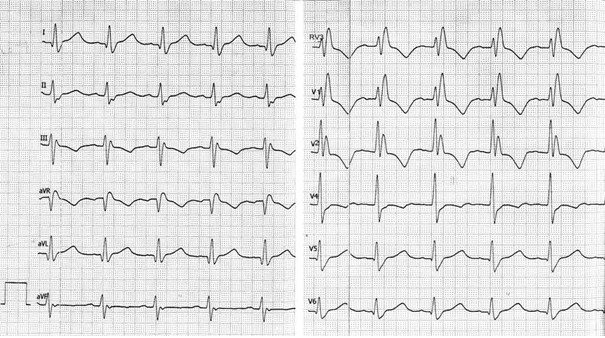
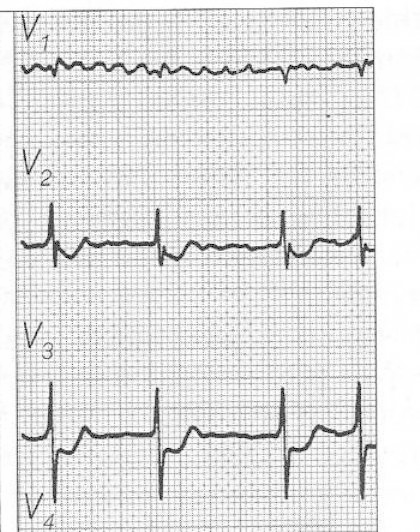
Zamieszczony elektrokardiogram przedstawia
„Ognisko zimne” w obrazie scyntygraficznym oznacza
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Jaki kolor ma warstwa korowa kości w badaniu MR na obrazie T1- zależnym?
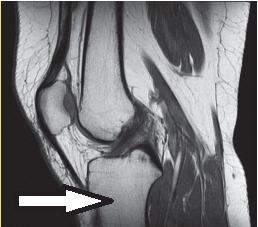
Którą kość oznaczono na obrazie rezonansu magnetycznego?
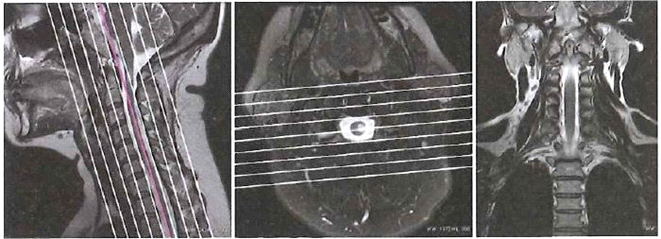
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
Obrazy DDR są tworzone w trakcie
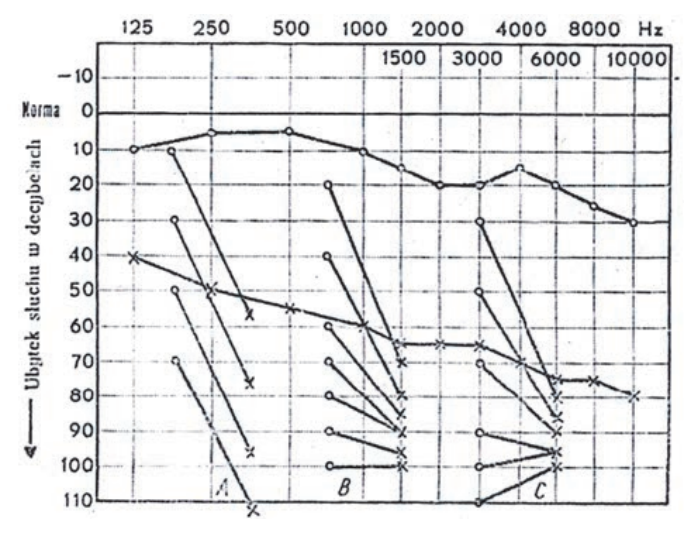
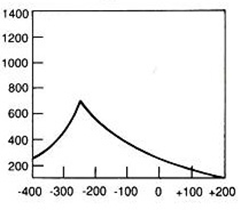
Audiogram przedstawia próbę
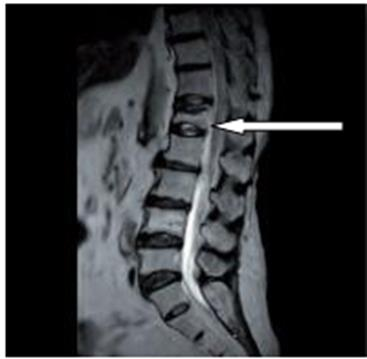
Na obrazie rezonansu magnetycznego strzałką wskazano patologiczny kręg
Rytm alfa i beta rejestruje się podczas badania
Jednostką indukcji magnetycznej jest
Na którym z zapisów EKG została uwidoczniona fala Pardee'go?
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
W którym miejscu, zgodnie z zasadami wykonywania badania EKG, należy umocować żółtą elektrodę przedsercową V2?
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Podczas badania gammakamerą źródłem promieniowania jest
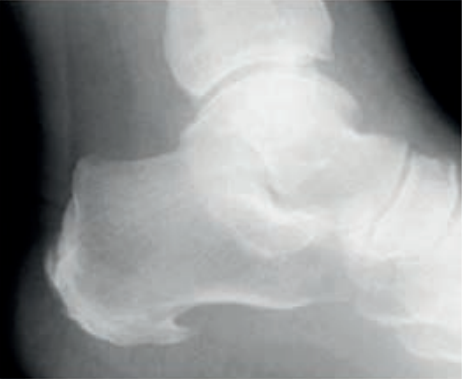
Co zostało uwidocznione na zamieszczonym radiogramie?
W lampie rentgenowskiej promieniowanie X powstaje w wyniku hamowania
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
Cholangiografia to badanie radiologiczne
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
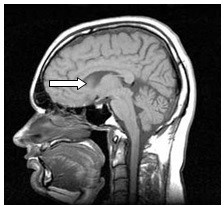
W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Badanie gęstości mineralnej kości metodą DXA należy wykonać
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
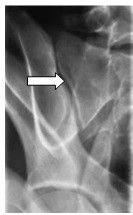
Którą strukturę anatomiczną zaznaczono strzałką na rentgenogramie?
Pozytywny środek cieniujący najczęściej stosowany w rentgenodiagnostyce powinien charakteryzować się
W diagnostyce mammograficznej punktowy ucisk sutka stosuje się w projekcji
Efekt „tea cup” widoczny jest na mammografach wykonanych w projekcji
W leczeniu izotopowym tarczycy podaje się
W zapisie EKG linia izoelektryczna obrazuje
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
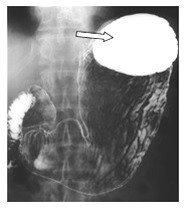
Który element żołądka zaznaczono strzałką na zdjęciu rentgenowskim?
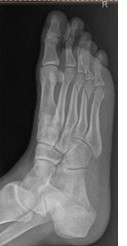
Na rentgenogramie stopy uwidocznione jest złamanie
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
W pracowni ultrasonograficznej technik elektroradiolog nie korzysta z przepisów dotyczących