Pytanie 1
Jakie urządzenie jest wykorzystywane do procesu ekstrakcji?
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Jakie urządzenie jest wykorzystywane do procesu ekstrakcji?
W tabeli zestawiono objętości molowe czterech gazów odmierzone w warunkach normalnych.
Dla którego spośród wymienionych w tabeli gazów objętość molowa najbardziej odchyla się od wartości obliczonej dla gazu doskonałego?
| Gaz | SO2 | CHCl3(para) | O3 | NH3 |
|---|---|---|---|---|
| Objętość molowa (dm3/mol) | 21,89 | 22,60 | 21,6 | 22,08 |
Jakie oznaczenie znajduje się na naczyniach szklanych kalibrowanych do wlewu?
Z partii materiału należy pobrać ogólną próbkę w ilości odpowiadającej promilowi całej partii. Na podstawie podanej informacji określ, ile pierwotnych próbek, każda ważąca 10 g, trzeba pobrać z partii cukru o masie 0,5 t, aby uzyskać reprezentatywną próbkę ogólną?
Ze względu na czystość, substancja oznakowana zamieszczoną etykietą powinna być wykorzystywana głównie do

Czy próbkę laboratoryjną przechowuje się w lodówce, gdy występuje w niej
Podczas pobierania próby wody do oznaczania metali ciężkich zaleca się stosowanie butelek wykonanych z:
Aby oddzielić połączenia szlifów, należy w miejscu ich styku wprowadzić
W którym wierszu tabeli podano ilości substancji i wody, potrzebne do sporządzenia 350 g roztworu o stężeniu 7%?
| Masa substancji | Masa wody | |
|---|---|---|
| A. | 24,5 g | 350 g |
| B. | 24,5 g | 325,5 g |
| C. | 7 g | 343 g |
| D. | 7 g | 350 g |
Które z wymienionych reakcji chemicznych stanowi reakcję redoks?
Który z poniższych zestawów obejmuje jedynie sprzęt do pomiarów?
Ile masy kwasu mrówkowego jest wymagane do uzyskania 11,2 dm3 tlenku węgla(II) (w warunkach normalnych) w procesie odwodnienia kwasu mrówkowego (M = 46 g/mol) za pomocą kwasu siarkowego(VI), zakładając efektywność procesu na poziomie 70%?
Proces mineralizacji próbki, który polega na jej spopieleniu w piecu muflowym w temperaturze 300-500°C i rozpuszczeniu pozostałych resztek w kwasach w celu oznaczenia zawartości metali ciężkich, to mineralizacja
Według zasady pierwszeństwa, znajdując na opakowaniu zbiorczym odczynnika piktogramy pokazane na rysunku, należy zwrócić szczególną uwagę na to, że substancja jest
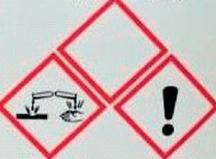
Zamieszczony piktogram odnosi się do substancji o klasie i kategorii zagrożenia:
Do grupy reagentów o szczególnym zastosowaniu nie wlicza się
Jakie urządzenie służy do pomiaru temperatury topnienia substancji chemicznych?
Metoda przygotowania próbki do badania, która nie jest
Piktogram ukazujący czaszkę oraz skrzyżowane kości piszczelowe jest typowy dla substancji o działaniu
Procedura oznaczenia kwasowości mleka. Do wykonania analizy, zgodnie z powyższą procedurą, potrzebne są
| Do kolby stożkowej o pojemności 300 cm3 pobrać dokładnie 25 cm3 badanego mleka i rozcieńczyć wodą destylowaną do objętości 50 cm3. Dodać 2-3 krople fenoloftaleiny i miareczkować mianowanym roztworem wodorotlenku sodu do uzyskania lekko różowego zabarwienia. |
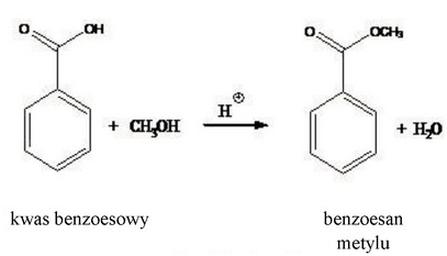
Do reakcji estryfikacji użyto 150 g kwasu benzoesowego (M = 122,12 g/mol), w wyniku której otrzymano czysty preparat benzoesanu metylu (M = 136,2 g/mol). Ile gramów benzoesanu metylu otrzymano, jeżeli reakcja przebiegała z wydajnością 92%?
Temperatura wrzenia aniliny przy normalnym ciśnieniu wynosi 457,13 K. W trakcie jej oczyszczania metodą destylacji prostej pod ciśnieniem atmosferycznym należy zebrać frakcję wrzącą w przedziale temperatur
Oblicz masę wapienia, który został rozłożony, jeśli w trakcie reakcji uzyskano 44,8 dm3 CO2 (w warunkach standardowych).
MC = 12 g/mol, MCa = 40 g/mol, MO = 16 g/mol
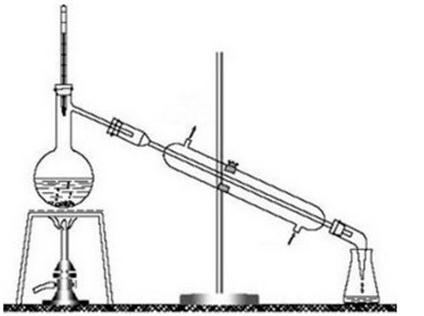
Na rysunku przedstawiono zestaw do
Którego odczynnika należy użyć do przygotowania roztworu wzorcowego, zawierającego jony \( \text{Fe}^{3+} \)?
Który symbol literowy umieszczany na naczyniach miarowych wskazuje na kalibrację do "wlewu"?
W trakcie pobierania próbek wody, które mają być analizowane pod kątem składników podatnych na rozkład fotochemiczny, należy
Piknometr służy do określania
Po przeprowadzeniu krystalizacji z 120 g kwasu szczawiowego uzyskano 105 g produktu o wysokiej czystości. Jaki był poziom zanieczyszczeń w kwasie szczawiowym?
W celu uzyskania 500 g mieszaniny oziębiającej o temperaturze -18oC należy zmieszać
| Tabela. Mieszaniny oziębiające | ||
|---|---|---|
| Temperatura mieszaniny [°C] | Skład mieszaniny | Stosunek masowy |
| -2 | Woda + chlorek amonu | 10 : 3 |
| -15 | Woda + rodanek amonu | 10 : 13 |
| -18 | Lód + chlorek amonu | 10 : 3 |
| -21 | Lód + chlorek sodu | 3 : 1 |
| -22 | Lód + chlorek amonu + azotan(V) amonu | 25 : 5 : 11 |
| -25 | Lód + azotan(V) amonu | 1 : 1 |
Aby wykonać chromatografię cienkowarstwową, należy przygotować eluent składający się z toluenu, acetonu oraz kwasu mrówkowego w proporcjach objętościowych 10:4:1. Jakie ilości poszczególnych składników powinny być wykorzystane do uzyskania 300 cm3 eluentu?
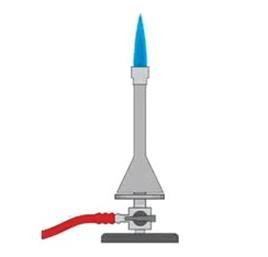
Na rysunku przedstawiono palnik Bunsena. Którym numerem oznaczono element do regulowania dopływu powietrza?

Temperatura topnienia mocznika wynosi 133 °C. W celu określenia czystości preparatów tej substancji, przeprowadzono badania temperatury ich topnienia, uzyskując wyniki przedstawione w tabeli. Wskaż preparat o najmniejszym stopniu czystości.
| Preparat | A | B | C | D |
|---|---|---|---|---|
| Zakres temperatury topnienia [°C] | 132-133 | 130-133 | 125-133 | 128-133 |
Aby ustalić miano roztworu wodnego NaOH, należy zastosować
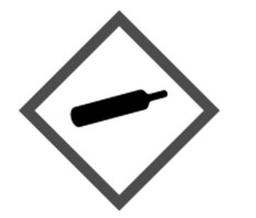
Na opakowaniu fenolu umieszcza się przedstawiony na rysunku znak ostrzegawczy, który oznacza, że jest to substancja

Próbki wody, które mają być badane pod kątem zawartości krzemu, powinny być przechowywane w pojemnikach
Na diagramie przedstawiającym proces pobierania prób środowiskowych do analizy literą Y oznaczono próbkę
Jak definiuje się próbkę wzorcową?
Na rysunku przedstawiono palnik
Podczas pipetowania menisk górny określa się dla roztworów