Pytanie 1
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
Wynik: 31/40 punktów (77,5%)
Wymagane minimum: 20 punktów (50%)
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
W trakcie obrazowania metodą rezonansu magnetycznego wykorzystywane jest zjawisko wysyłania sygnału emitowanego przez
Przy podejrzeniu ciała obcego w oczodole należy wykonać
Odprowadzenie II rejestruje różnicę potencjałów między
Do prób aktywacyjnych stosowanych w badaniu EEG zalicza się
W której technice obrazowania zostają zarejestrowane jednocześnie dwa przeciwbieżne kwanty promieniowania gamma o równej energii 511 keV?
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
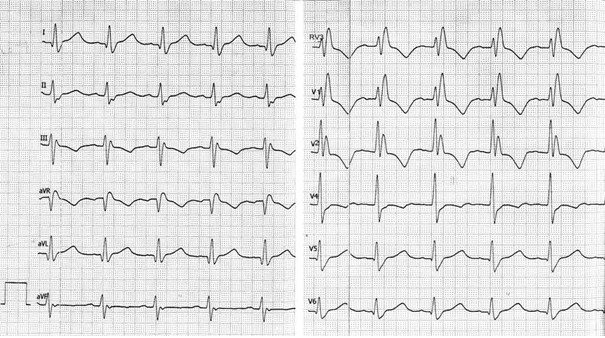
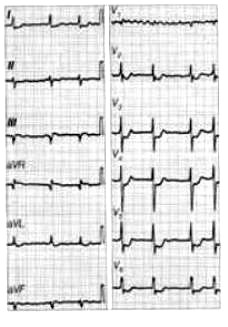
Przedstawiony zapis elektrokardiograficzny może wskazywać na
W badaniu EKG elektrodę przedsercową V4 należy umocować
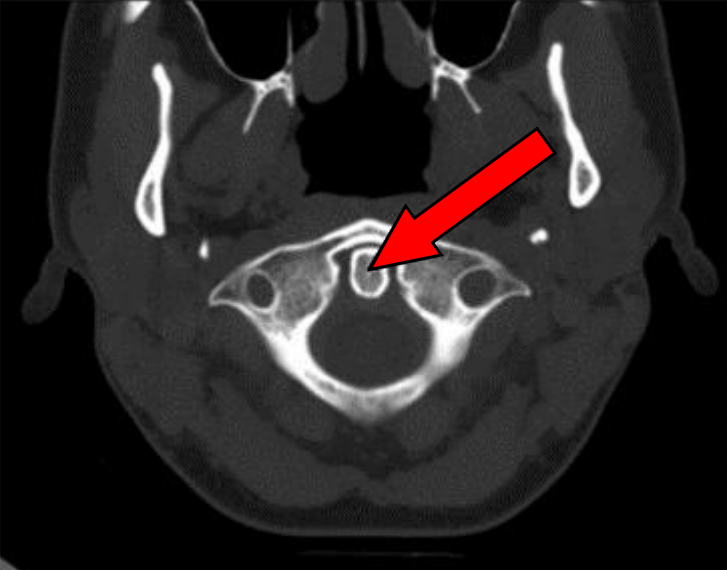
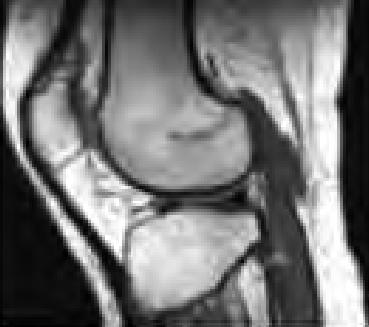
Na przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano
Badanie polegające na wprowadzeniu cewnika przez pęcherz moczowy do moczowodu i miedniczki nerkowej i podaniu środka kontrastującego to
Fala głosowa rozchodzi się
W obrazowaniu MR do uwidocznienia naczyń krwionośnych jest stosowana sekwencja
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
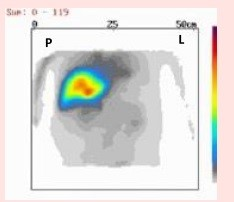
Który narząd został uwidoczniony na przedstawionym obrazie scyntygraficznym?
Podczas teleradioterapii piersi lewej narządem krytycznym jest
W zapisie EKG załamek U występuje bezpośrednio po załamku
Na radiogramie czaszki strzałką zaznaczono
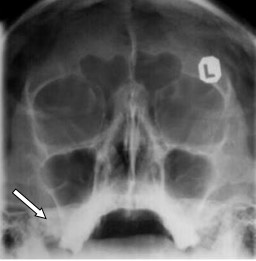
W radioterapii hadronowej leczenie odbywa się przy użyciu
Na zamieszczonym rentgenogramie strzałką zaznaczono
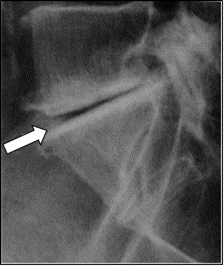
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
Na którym obrazie zarejestrowano badanie scyntygraficzne?
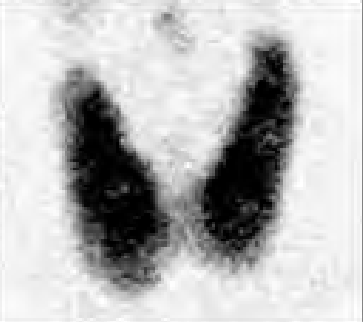
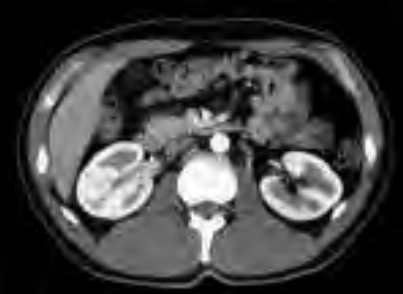
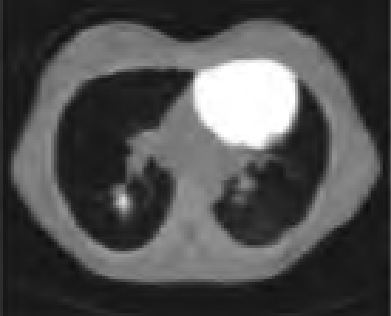
Wskazaniem do wykonania badania spirometrycznego jest
W metodzie RM (rezonansu magnetycznego) po umieszczeniu pacjenta w silnym, stałym polu magnetycznym dochodzi do oddziaływania
Ligand stosuje się
Który załamek odzwierciedla szybką repolaryzację komór w zapisie EKG?
Na elektrokardiogramie uwidoczniono
Gadolin jako dożylny środek kontrastowy stosowany w MR powoduje
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

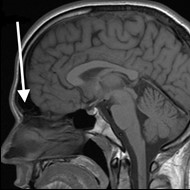
Na obrazie rezonansu magnetycznego głowy strzałką wskazano zatokę
Fistulografia to badanie kontrastowe
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Który środek ochrony radiologicznej pacjenta należy zastosować podczas wykonywania zdjęcia bocznego kręgosłupa szyjnego?
W technice napromieniania SSD mierzona jest odległość źródła promieniowania od
Podczas wykonywania zdjęcia rentgenowskiego klatki piersiowej w celu ochrony radiologicznej pacjenta należy zastosować
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
W obrazowaniu metodą rezonansu magnetycznego T1 oznacza czas
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
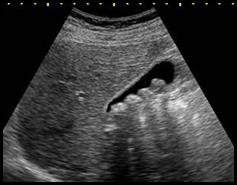
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?