Pytanie 1
Proces, w którym woda jest usuwana z zamrożonego materiału poprzez sublimację lodu
(czyli bezpośrednie przejście do stanu pary z pominięciem stanu ciekłego) nazywa się
Wynik: 35/40 punktów (87,5%)
Wymagane minimum: 20 punktów (50%)
Proces, w którym woda jest usuwana z zamrożonego materiału poprzez sublimację lodu
(czyli bezpośrednie przejście do stanu pary z pominięciem stanu ciekłego) nazywa się
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na podstawie danych w tabeli próbkę, w której będzie oznaczany BZT, należy przechowywać
| Oznaczany parametr | Rodzaj naczynia do przechowywania | Sposób utrwalania | Dopuszczalny czas przechowywania |
|---|---|---|---|
| barwa | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C | 24 h |
| fosforany ogólne | szklane lub polietylenowe | - zakwaszenie kwasem siarkowym(VI) - schłodzenie do temperatury 2-5°C | 4 h 48 h |
| BZT | szklane | - schłodzenie do temperatury 2-5°C - przechowywanie w ciemności | 24 h |
| azot azotanowy(V) | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C - dodanie 2 cm3 chloroformu do 1 dm3 próbki | 24 h 48 h |
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
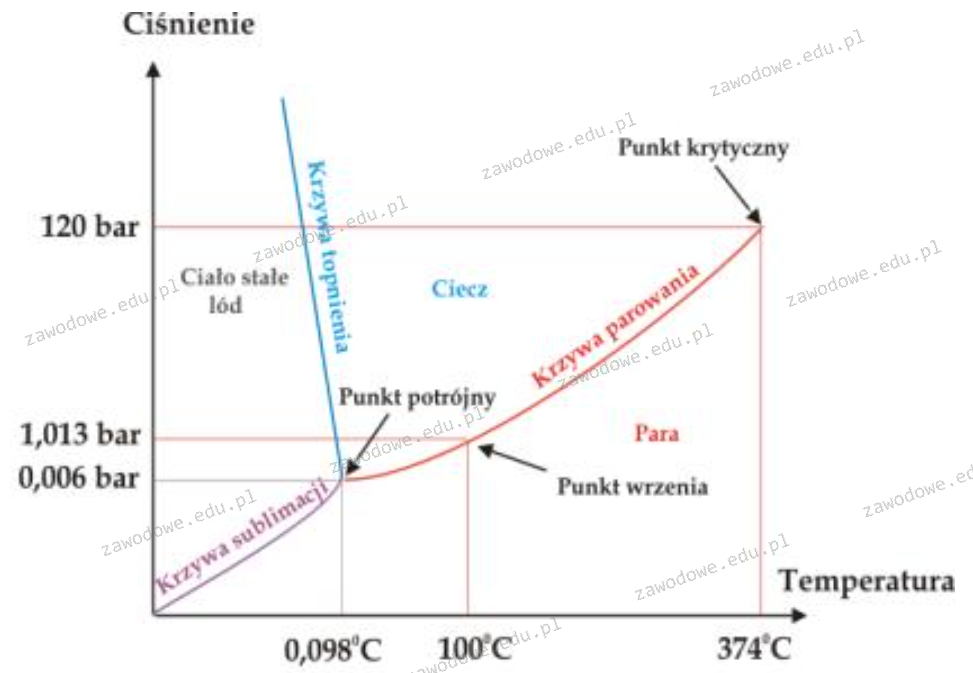
Korzystając z wykresu wskaż, w jakiej postaci występuje woda w temperaturze 10°C i pod ciśnieniem 100 barów.
Nie należy używać do czyszczenia szklanych naczyń laboratoryjnych
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Oblicz, jaką ilość węglanu sodu w gramach należy przygotować, aby uzyskać 500 cm3 roztworu tej soli o stężeniu 0,1000 mol/dm3.
MNa = 23 g/mol, MC = 12 g/mol, MO = 16 g/mol
Aby oczyścić zwęglone osady w probówce, należy zastosować
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Symbol "In" znajduje się na
Aby przygotować 500 g roztworu o stężeniu 10% (m/m), ile substancji należy odważyć?
Który z poniższych sposobów homogenizacji próbki jest najbardziej odpowiedni do przygotowania próbki gleby do analizy chemicznej?
W którym wierszu są zapisane nazwy wyłącznie rozpuszczalników palnych?
| Właściwości wybranych rozpuszczalników. | ||||
|---|---|---|---|---|
| Rozpuszczalnik | Gęstość [g/cm3] | Temperatura wrzenia [°C] | Temperatura zapłonu [°C] | Rozpuszczalność w wodzie [g/100 cm3] |
| Eter dietylowy | 0,71 | 35 | -45 | 7 |
| Heksan | 0,66 | 60-80 | -23 | 0,01 |
| Aceton | 0,79 | 57 | -18 | ∞ |
| Benzen | 0,88 | 80 | -11 | 0,07 |
| Chloroform | 1,49 | 61 | - | 0,82 |
| Tetrachlorometan | 1,59 | 77 | - | 0,08 |
| Etanol | 0,81 | 78 | 12 | ∞ |
| Chlorometan | 1,34 | 41 | - | 2 |
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Deminimalizowaną wodę można uzyskać przez
Jakie urządzenie jest wykorzystywane do oczyszczania próbki gazowej?
Wybierz poprawny zapis jonowy spośród podanych reakcji, w których otrzymywany jest siarczan(VI) baru.
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
W przypadku zanieczyszczeń szklanych naczyń osadami o charakterze nieorganicznym, takimi jak wodorotlenki, tlenki oraz węglany, do ich oczyszczania używa się
Do narzędzi pomiarowych zalicza się
Korzystając z danych w tabeli wskaż, ile cm3 36% roztworu HCl należy użyć, aby przygotować 250 cm3 0,1-molowego roztworu tego kwasu.
| % wagowy [%] | d420 [g/cm3] | m HCl w 100 cm3 [g/100cm3] | CM HCl [mol/dm3] |
|---|---|---|---|
| 30 | 1,1492 | 34,48 | 9,46 |
| 32 | 1,1593 | 37,10 | 10,17 |
| 34 | 1,1691 | 39,75 | 10,90 |
| 36 | 1,1789 | 42,44 | 11,64 |
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Oddzielanie płynnej mieszanki poprzez jej odparowanie, a potem skroplenie poszczególnych składników to
Którą substancję można bezpośrednio wyrzucić do odpadów komunalnych?
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Ogólna próbka, jednostkowa lub pierwotna powinna
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na podstawie zmierzonej temperatury topnienia można określić związek organiczny oraz ustalić jego
Z przedstawionego opisu wynika, że kluczową właściwością próbki analitycznej jest jej
Próbka analityczna to fragment materiału stworzony z myślą o przeprowadzeniu badania lub obserwacji. Powinna odzwierciedlać przeciętny skład i cechy materiału, który jest badany.
W celu przeprowadzenia opisanego doświadczenia, należy przygotować:
| Opis procesu wydzielenia kwasu acetylosalicylowego z tabletek |
|---|
| Pięć rozgniecionych tabletek aspiryny (polopiryny) umieszcza się w kolbie stożkowej o pojemności 100 ml, dodaje 10 ml etanolu i ogrzewa na łaźni wodnej, aż do momentu rozpadnięcia się tabletek. W roztworze znajduje się kwas acetylosalicylowy, natomiast masa tabletkowa pozostaje w osadzie. Osad ten odsącza się na ogrzanym lejku szklanym zaopatrzonym w sączek karbowany. Do odebiornego przesączu dodaje się 20-30 ml zimnej wody destylowanej. Dodatek wody powoduje wypadanie osadu aspiryny z roztworu (zmniejsza się rozpuszczalność aspiryny w roztworze wodno-alkoholowym). Wydzielone kryształy odsączyć na lejku sitowym i suszyć na powietrzu. |
Zgodnie z zasadami BHP w laboratorium, po zakończeniu pracy z odczynnikami chemicznymi należy:
Resztki szkła, osadników czy inne odpady stałe powstałe w laboratorium analitycznym powinny być umieszczone
W karcie charakterystyki substancji znajduje się piktogram, którym powinna być oznakowana substancja

Do metalowego sprzętu laboratoryjnego używanego w praktykach analitycznych zalicza się
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wskaż metodę rozdzielenia układu, w którym fazą rozproszoną jest ciało stałe, a fazą rozpraszającą gaz.
| faza rozproszona | faza rozpraszająca | ||
|---|---|---|---|
| gaz | ciecz | ciało stałe | |
| gaz | - | piana | piana stała |
| ciecz | aerozol ciekły | emulsja | emulsja stała |
| ciało stałe | aerozol stały | zol | zol stały |
Aby uzyskać drobnokrystaliczny osad BaSO4, należy wykonać poniższe kroki:
Do zlewki wlać 20 cm3 roztworu BaCl2, następnie dodać 100 cm3 wody destylowanej oraz kilka kropli roztworu HCl. Zawartość zlewki podgrzać na łaźni wodnej, a potem, ciągle mieszając, dodać 35 cm3 roztworu H2SO4.
Mieszaninę ogrzewać na łaźni wodnej przez 1 godzinę. Osad odsączyć i przepłukać kilkakrotnie gorącą wodą zakwaszoną kilkoma kroplami roztworu H2SO4.
Według przedstawionej procedury, do uzyskania osadu BaSO4 potrzebne są: