Pytanie 1
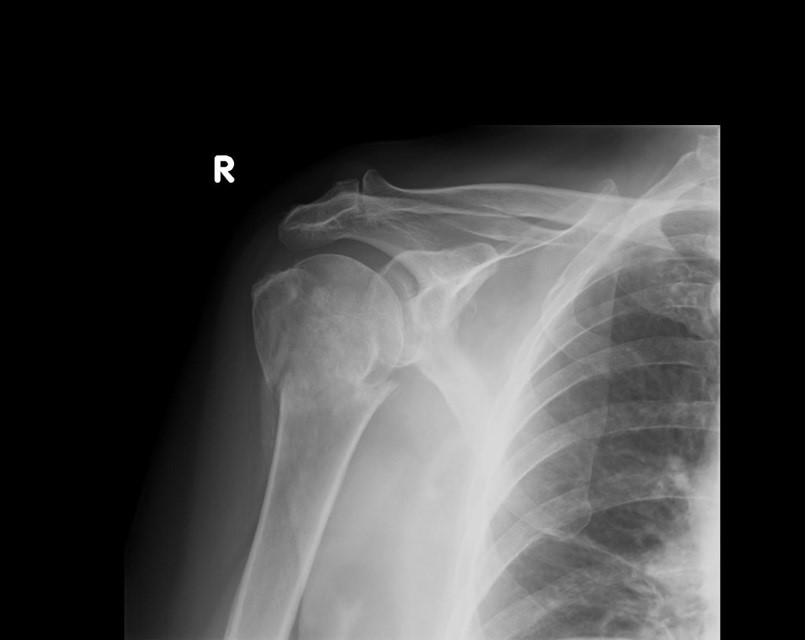
Na radiogramie uwidoczniono złamanie
Wynik: 21/40 punktów (52,5%)
Wymagane minimum: 20 punktów (50%)
Na radiogramie uwidoczniono złamanie

W radiografii mianem SID określa się
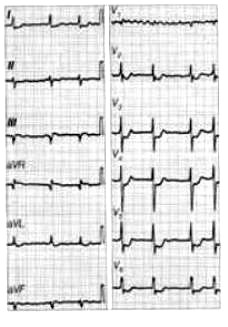
Na elektrokardiogramie uwidoczniono
W trakcie obrazowania metodą rezonansu magnetycznego wykorzystywane jest zjawisko wysyłania sygnału emitowanego przez
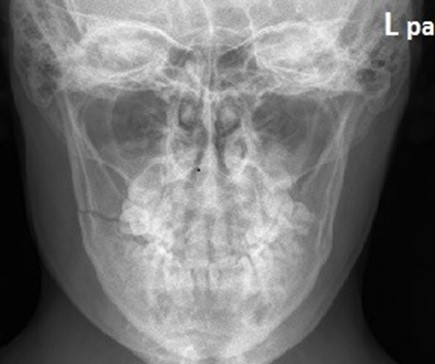
Na radiogramie żuchwy uwidoczniono złamanie w okolicy
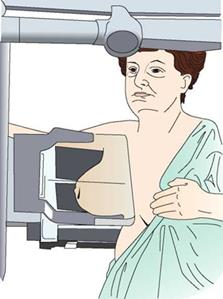
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Które informacje należy zamieścić na strzykawce z radiofarmaceutykiem przygotowanym przez technika elektroradiologa?
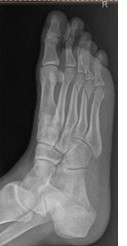
Na rentgenogramie stopy uwidocznione jest złamanie
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
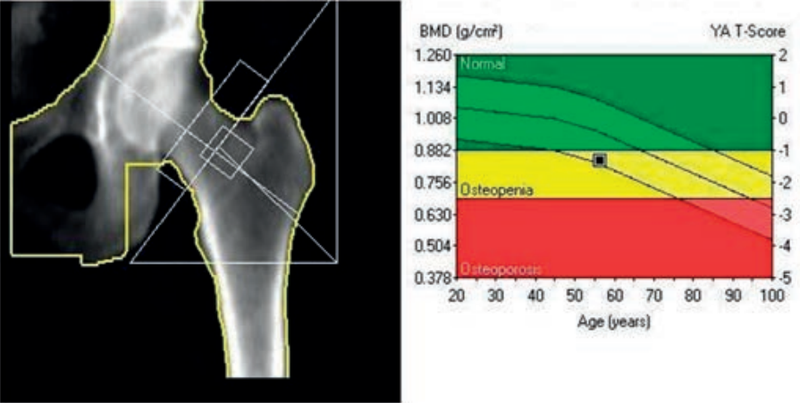
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
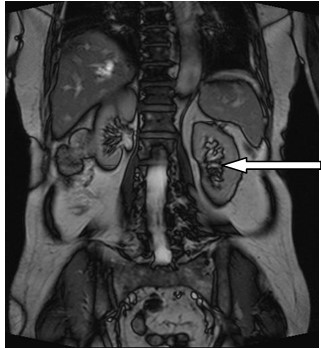
Który narząd został oznaczony strzałką na obrazie rezonansu magnetycznego?
Który system informatyczny jest wykorzystywany do archiwizowania i przesyłania obrazów na stacje diagnostyczne w standardzie DICOM?
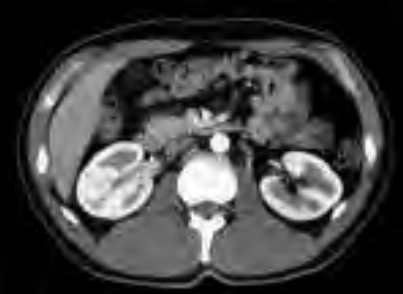
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
Na obrazie radiologicznym uwidoczniono złamanie kości
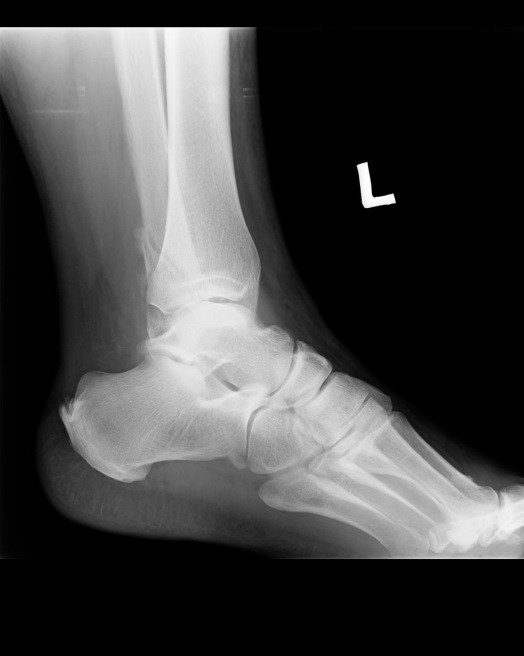
Na radiogramie uwidoczniono
Na którym obrazie zarejestrowano badanie scyntygraficzne?
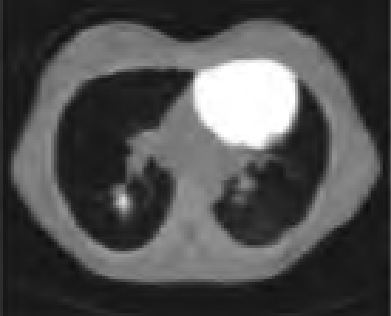
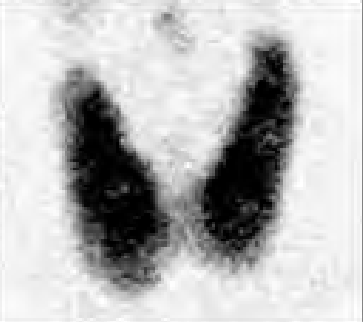
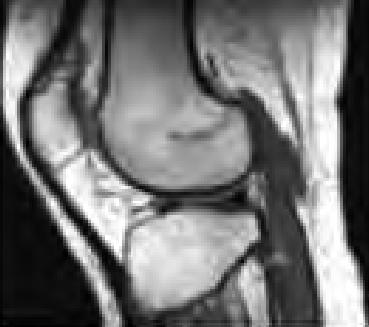
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
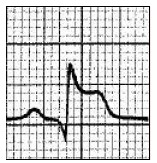
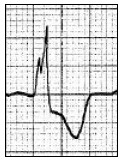
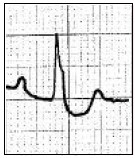
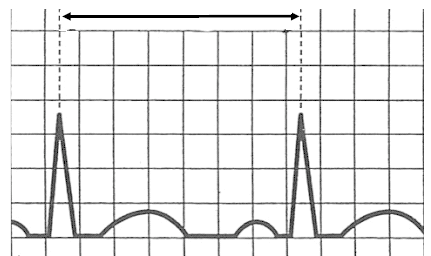
Który zapis EKG przedstawia falę Pardee'go?

Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
W ultrasonografii występuje zależność:
Promieniowanie jonizujące pośrednio to
Na schemacie oznaczono
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Powierzchnia gabinetu rentgenowskiego, w którym zainstalowany jest aparat rentgenowski wyposażony w oddzielną lampę, nie może być mniejsza niż
Znak umieszczony w pracowni rezonansu magnetycznego zakazuje wstępu osobom

Który stan patologiczny został zarejestrowany podczas wykonywania badania EKG?
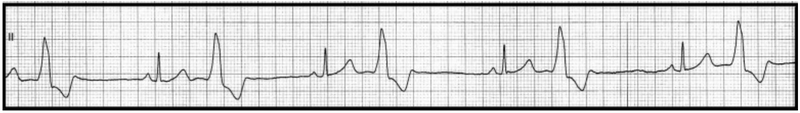
Zamieszczone obrazy związane są z badaniem
Zwiększenie napięcia na lampie rentgenowskiej powoduje
W przypadku migotania komór w zapisie EKG występuje
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
SPECT to
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji
W radiografii mianem SID określa się