Pytanie 1
Lordoza to fizjologiczna krzywizna kręgosłupa występująca
Wynik: 21/40 punktów (52,5%)
Wymagane minimum: 20 punktów (50%)
Lordoza to fizjologiczna krzywizna kręgosłupa występująca
W badaniu EKG punktem przyłożenia odprowadzenia przedsercowego C2 jest
W brachyterapii MDR stosowane są dawki promieniowania
Która metoda diagnostyczna służy do określenia gęstości minerału kostnego w ujęciu objętościowym g/cm³?
Badanie gęstości mineralnej kości metodą DXA należy wykonać
Gadolin jako dożylny środek kontrastowy stosowany w MR powoduje
W badaniu mammograficznym jedną z podstawowych projekcji jest projekcja
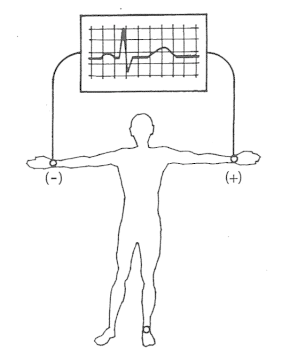
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
Przy ułożeniu do zdjęcia AP czaszki płaszczyzna
W scyntygrafii kośćca „ogniska gorące” oznaczają miejsca
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

Pozytywny środek cieniujący najczęściej stosowany w rentgenodiagnostyce powinien charakteryzować się
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
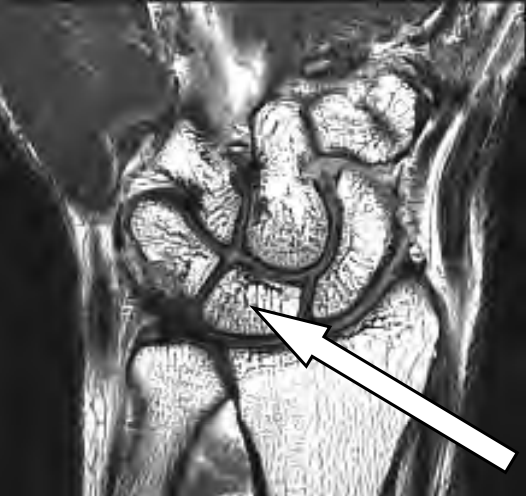
Na obrazie RM nadgarstka lewego strzałką oznaczono kość
Technika stereotaktyczna polega na napromienianiu nowotworu
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
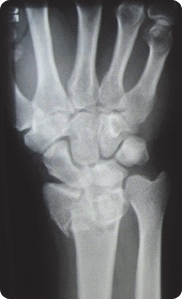
Na radiogramie uwidoczniono złamanie nasady
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
W radiologii analogowej lampy rentgenowskiej z tubusem używa się do wykonania zdjęcia
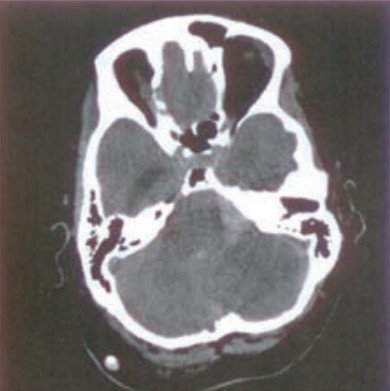
Zamieszczony obraz został wykonany metodą
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
W której projekcji należy wykonać badanie radiologiczne kręgosłupa lędźwiowego, by na otrzymanym zdjęciu wyrostki kręgów lędźwiowych układały się w charakterystyczny kształt piesków (teriera szkockiego)?
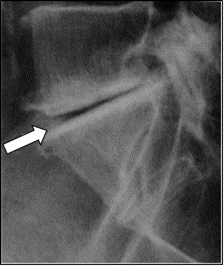
Na zamieszczonym rentgenogramie strzałką zaznaczono
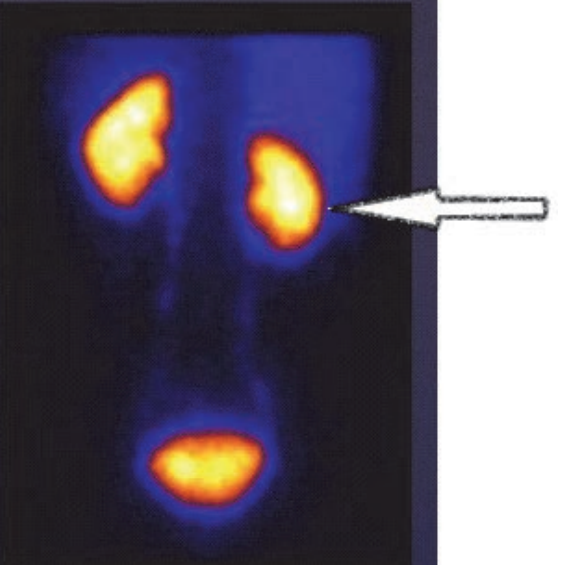
Na scyntygramie strzałką oznaczono
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?
Rozpoczęcie badania TK nerek po 20-30 sekundach od początku podania środka kontrastowego umożliwia diagnostykę
SPECT to
Czym charakteryzuje się późny odczyn popromienny?
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
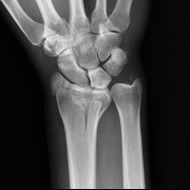
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
W scyntygrafii perfuzyjnej płuc pacjentowi podawany jest radioizotop
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
Którą kasetę należy wykorzystać do wykonania rentgenogramu klatki piersiowej w projekcji bocznej u 35-letniej pacjentki o wzroście 165 cm i wadze 54 kg?
Wyniosłość międzykłykciowa znajduje się na nasadzie
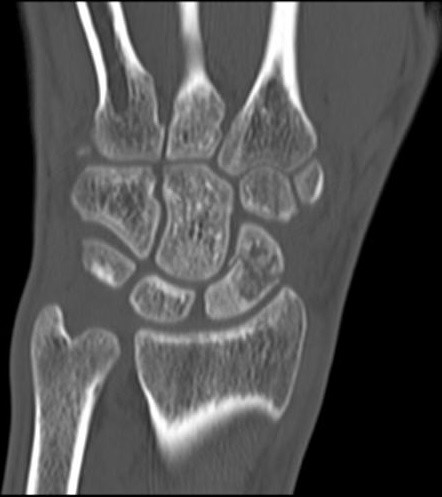
Na obrazie TK nadgarstka uwidocznione jest złamanie kości
Hiperfrakcjonowanie dawki w radioterapii oznacza napromienienie pacjenta
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie