Pytanie 1
Zarejestrowane na elektrokardiogramie miarowe fale f w kształcie „zębów piły” poprzedzielane prawidłowymi zespołami QRS są charakterystyczne dla
Wynik: 20/40 punktów (50,0%)
Wymagane minimum: 20 punktów (50%)
Zarejestrowane na elektrokardiogramie miarowe fale f w kształcie „zębów piły” poprzedzielane prawidłowymi zespołami QRS są charakterystyczne dla
Zgodnie z obowiązującą procedurą radiologiczną zdjęcie jamy brzusznej przy podejrzeniu zapalenia nerek zostanie wykonane w projekcji
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
Który obraz MR mózgu został wykonany w sekwencji DWI?
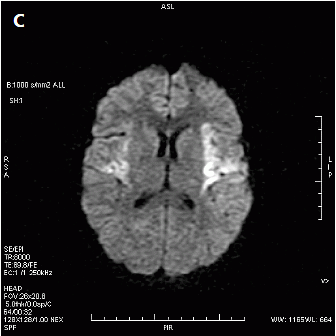
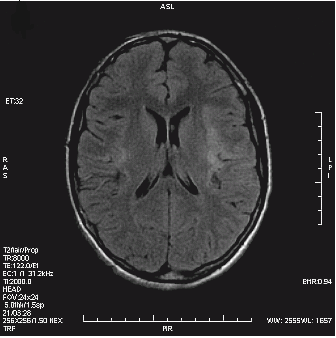
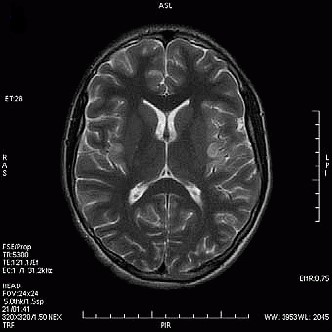
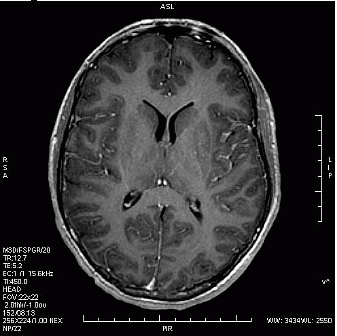
W pracowni radioterapii wyświetlenie na ekranie monitora aparatu komunikatu „ROTATION” oznacza prowadzoną terapię
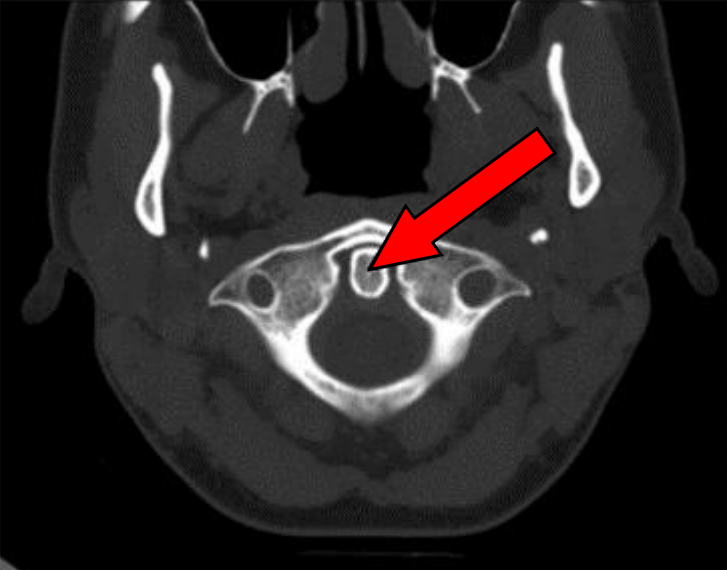
Na przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
Fala głosowa rozchodzi się
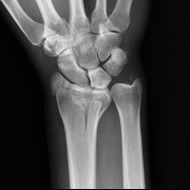
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
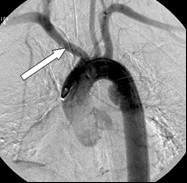
Na obrazie cyfrowej angiografii subtrakcyjnej strzałką zaznaczono
Badanie metodą Dopplera umożliwia
Radiofarmaceutyki stosowane w medycynie nuklearnej powstają dzięki połączeniu radioizotopu
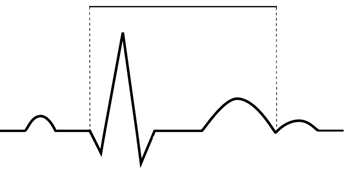
Na wykresie EKG zaznaczono
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
W leczeniu izotopowym tarczycy należy podać
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

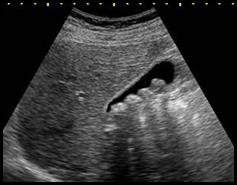
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem jest
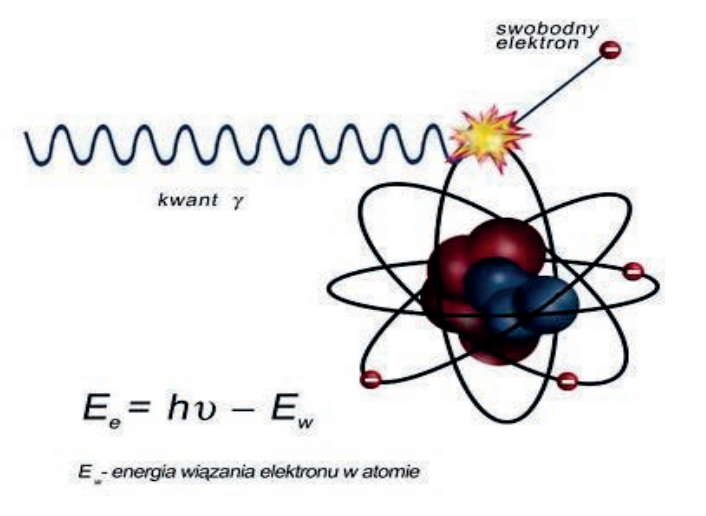
Na zamieszczonej rycinie przedstawiono
W systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej oznacza się symbolem
Co określa M₀ w systemie klasyfikacji nowotworów TNM?
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
Na przedstawionym scyntygramie ukazano duży obszar
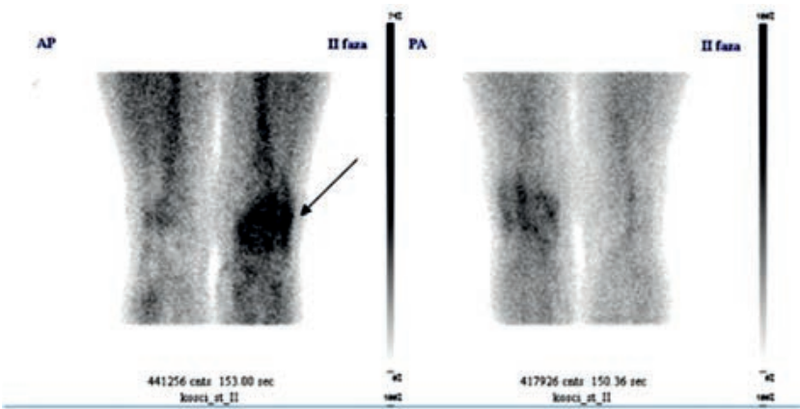
Na obrazie uwidoczniono
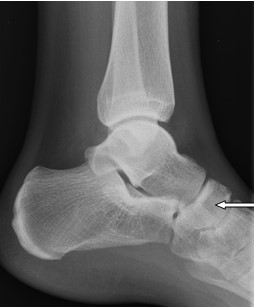
Na radiogramie strzałką oznaczono
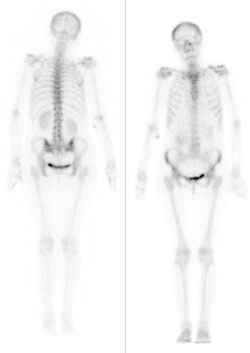
Na którym obrazie zarejestrowano badanie scyntygraficzne?
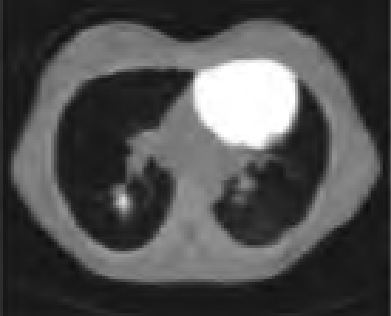
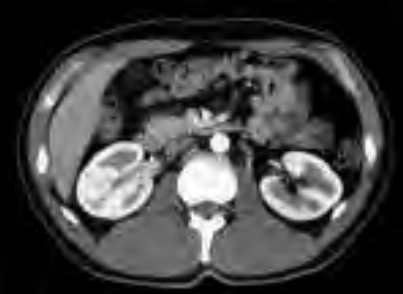
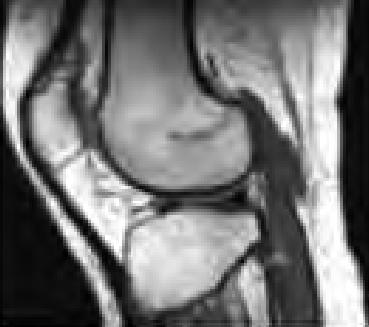
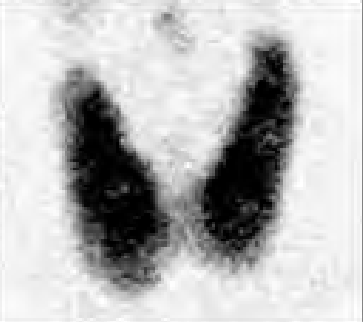
Cholangiografia to badanie radiologiczne
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Na zamieszczonym obrazie radiologicznym nadgarstka strzałką wskazano kość
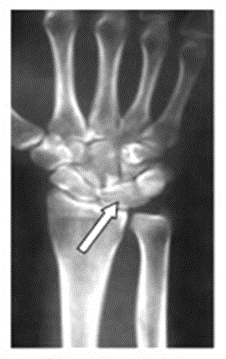
Na elektrokardiogramie uwidoczniono
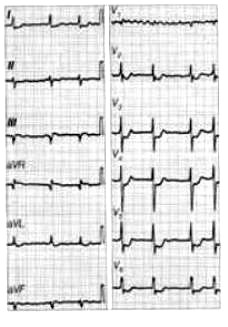
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
W radiologii stomatologicznej ząb o numerze 23 to kieł
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Który artefakt jest widoczny na skanie tomografii komputerowej?
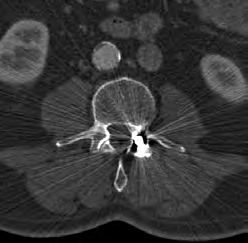
Technik elektroradiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta:
Promieniowanie rentgenowskie jest