Pytanie 1
Aby uzyskać roztwór AgNO3 (masa molowa AgNO3 to 169,8 g/mol) o stężeniu 0,1 mol/dm3, należy rozpuścić w wodzie destylowanej i dopełnić kolbę wodą destylowaną do zaznaczonej kreski.
Wynik: 18/40 punktów (45,0%)
Wymagane minimum: 20 punktów (50%)
Aby uzyskać roztwór AgNO3 (masa molowa AgNO3 to 169,8 g/mol) o stężeniu 0,1 mol/dm3, należy rozpuścić w wodzie destylowanej i dopełnić kolbę wodą destylowaną do zaznaczonej kreski.
Zjawisko fizyczne, które polega na rozkładaniu struktury krystalicznej substancji stałej oraz przenikaniu jej cząsteczek lub jonów do cieczy, nosi nazwę
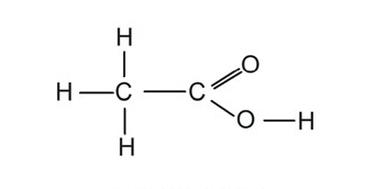
Związek o podanym wzorze to kwas
Sączenie na gorąco powinno być użyte, aby
Naczynia miarowe, skalibrowane "na wlew" (IN) to:
Reakcja neutralizacji wodorotlenku sodu z kwasem solnym zrealizowana jest zgodnie z równaniem:
NaOH + HCl → NaCl + H2O Masy molowe: MNaOH = 40 g/mol, MHCl = 36,5 g/mol Aby zneutralizować 10 g wodorotlenku sodu, wymagane jest
Substancje chemiczne, które zazwyczaj wykorzystuje się w eksperymentach preparatywnych oraz w jakościowych analizach, charakteryzujące się czystością w przedziale 99-99,9%, nazywa się
Przedstawiony schemat ideowy ilustruje proces wytwarzania N2 → NO → NO2 → HNO3
Zamieszczony piktogram odnosi się do substancji o klasie i kategorii zagrożenia:
Przykładem piany stałej jest
| faza rozproszona | faza rozpraszająca | ||
|---|---|---|---|
| gaz | ciecz | ciało stałe | |
| gaz | - | piana | piana stała |
| ciecz | aerozol ciekły | emulsja | emulsja stała |
| ciało stałe | aerozol stały | zol | zol stały |
Do filtracji osadów drobnokrystalicznych wykorzystuje się filtry
Odważka analityczna przygotowana w fabryce zawiera 0,1 mola EDTA. Posiadając taką jedną odważkę analityczną, jakie roztwory można przygotować?
Aby podnieść stężenie mikroelementów w roztworze, próbkę należy poddać
Przedstawiono wyciąg z karty charakterystyki substancji chemicznej. Na podstawie informacji zawartej w zamieszczonym fragmencie karty wskaż wzór chemiczny substancji, której można użyć jako materiału neutralizującego lodowaty kwas octowy.
Kwas octowy lodowaty 99,5% Materiały zapobiegające rozprzestrzenianiu się skażenia i służące do usuwania skażenia Jeżeli to możliwe i bezpieczne, zlikwidować lub ograniczyć wyciek (uszczelnić, zamknąć dopływ cieczy, uszkodzone opakowanie umieścić w opakowaniu awaryjnym). Ograniczyć rozprzestrzenianie się rozlewiska przez obwałowanie terenu; zebrane duże ilości cieczy odpompować. Małe ilości rozlanej cieczy przysypać niepalnym materiałem chłonnym (ziemia, piasek oraz materiałami neutralizującymi kwasy, np. węglanem wapnia lub sodu, zmielonym wapieniem, dolomitem), zebrać do zamykanego pojemnika i przekazać do zniszczenia. Zanieczyszczoną powierzchnię spłukać wodą. Popłuczyny zebrać i usunąć jako odpad niebezpieczny. |
Proces nitrowania najczęściej realizuje się, stosując organiczny substrat
Jaką próbkę stanowi woreczek gleby pobranej zgodnie z instrukcją?
| Instrukcja pobierania próbek glebowych | |
| Próbki pierwotne pobiera się laską glebową z wierzchniej warstwy gleby 0-20 cm, kolejno wykonując czynności: – w miejscu pobierania próbki pierwotnej (pojedynczej), rolę świeżo zaoraną przydeptać, – pionowo ustawić laskę do powierzchni gleby, – wcisnąć laskę do oporu (na wysokość poprzeczki ograniczającej), – wykonać pełny obrót i wyjąć laskę, – zawartość wgłębienia (zasobnika) przenieść do pojemnika skrobaczki. Po pobraniu próbek pojedynczych, całość wymieszać i napełnić kartonik lub woreczek. | |
Zgodnie z instrukcją dotyczącą pobierania próbek nawozów (na podstawie normy PN-EN 12579:2001), liczbę punktów pobierania próbek pierwotnych ustala się według wzoru nsp = 0,5·√V, gdzie V oznacza objętość jednostki badanej w m3. Wartość nsp zaokrągla się do liczby całkowitej, a dodatkowo nie może być mniejsza niż 12 ani większa niż 30.
Dlatego dla objętości V = 4900 m3, nsp wynosi
Aby oddzielić galaretowaty osad typu Fe(OH)3 od roztworu, jaki sączek należy zastosować?
W standardowym układzie destylacyjnym, który ma ukośną chłodnicę, wykorzystuje się chłodnicę
Związki chromu(VI) oddziałują negatywnie na środowisko, ponieważ
W przypadku odczynnika, w którym nawet najczulsze techniki analizy chemicznej nie są w stanie wykryć zanieczyszczeń, a jego badanie wymaga zastosowania metod opartych na zjawiskach fizycznych, zalicza się on do kategorii czystości
Po zakończeniu pomiarów pH, elektrody powinny być przepłukane
Z analizy wykresu wynika, że substancją o najniższej rozpuszczalności w wodzie w temperaturze 100°C jest
Gdzie należy przechowywać cyjanek potasu KCN?
Preparaty zawierające KOH (tzw. żrący potaż), oznaczone są symbolem S 1/2. Na podstawie informacji zawartych w tabeli, określ zasady przechowywania tych preparatów.
| Numer zwrotu S | Warunki bezpiecznego stosowania | Numer zwrotu S | Warunki bezpiecznego stosowania |
|---|---|---|---|
| S1 | Przechowywać pod zamknięciem | S12 | Nie przechowywać pojemnika szczelnie zamkniętego |
| S2 | Chronić przed dziećmi | S13 | Nie przechowywać razem z żywnością, napojami i karmą dla zwierząt |
| S3 | Przechowywać w chłodnym miejscu | S15 | Przechowywać z dala od źródeł ciepła |
| S4 | Nie przechowywać w pomieszczeniach mieszkalnych | S16 | Nie przechowywać w pobliżu źródeł zapłonu – nie palić tytoniu |
Czystość konkretnego odczynnika chemicznego wynosi: 99,9-99,99%. Jakiego rodzaju jest ten odczynnik?
Podczas analizowania zmienności składu wód płynących w skali rocznej, próbki wody powinny być zbierane i badane przynajmniej raz na
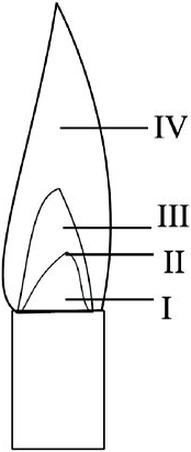
Na rysunku przedstawiającym płomień palnika gazowego najwyższa temperatura płomienia znajduje się w strefie
Kalibracja pH-metru nie jest potrzebna po
Zawarty fragment instrukcji odnosi się do
Po dodaniu do kolby Kjeldahla próbki analizowanego materiału, kwasu siarkowego(VI) oraz katalizatora, należy delikatnie ogrzewać zawartość kolby za pomocą palnika gazowego. W początkowym etapie ogrzewania zawartość kolby wykazuje pienienie i zmienia kolor na ciemniejszy. W tym czasie należy przeprowadzać ogrzewanie bardzo ostrożnie, a nawet z przerwami, aby uniknąć "wydostania się" czarnobrunatnej masy do szyjki kolby.
Do rozpuszczania próbek wykorzystuje się wodę królewską, która stanowi mieszaninę stężonych kwasów
Roztwór o dokładnej masie z odważki analitycznej powinien być sporządzony
Na zdjęciu przedstawiono proces

Z uwagi na bezpieczeństwo pracy, ciecze żrące powinny być podgrzewane w łaźniach
Zestaw do filtracji pod obniżonym ciśnieniem powinien obejmować między innymi
Podaj nazwę reagentu chemicznego, który w specyficznych warunkach reaguje tylko z jednym jonem, pierwiastkiem lub związkiem chemicznym?
Chemikalia, dla których upłynął okres przydatności,
W którym z podanych równań reakcji dochodzi do zmiany stopni utlenienia atomów?
Aby przygotować 0,5 dm3 roztworu HCl o stężeniu 0,2 mol/dm3, jaką kolbę miarową o pojemności należy wykorzystać?
W wypadku oblania skóry kwasem mrówkowym należy
| Wyciąg z karty charakterystyki Skład: kwas mrówkowy 80%, woda 11-20% Pierwsza pomoc. Po narażeniu przez drogi oddechowe. Natychmiast wezwać lekarza. Po kontakcie ze skórą. Zanieczyszczoną skórę natychmiast przemyć dużą ilością wody. |