Pytanie 1
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Którą kasetę należy wykorzystać do wykonania rentgenogramu klatki piersiowej w projekcji bocznej u 35-letniej pacjentki o wzroście 165 cm i wadze 54 kg?
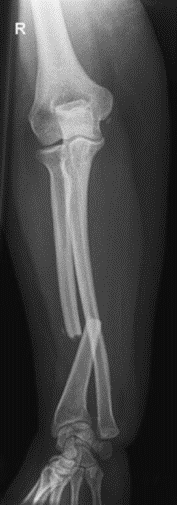
Na radiogramie uwidoczniono złamanie
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Glukoza podawana pacjentowi w badaniu PET jest znakowana radioaktywnym
W badaniu PET stosuje się tylko radioizotopy emitujące
Jaki sposób frakcjonowania dawki jest stosowany w radioterapii konwencjonalnej?
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
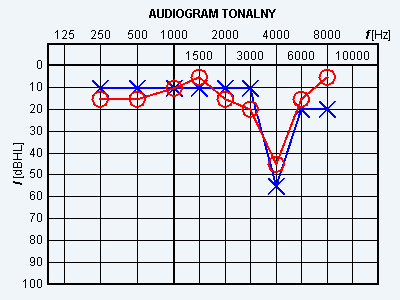
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
Do prób aktywacyjnych stosowanych w badaniu EEG zalicza się
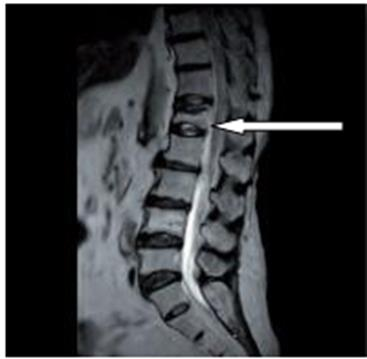
Na obrazie rezonansu magnetycznego strzałką wskazano patologiczny kręg
Zadaniem technika elektroradiologii w pracowni badań naczyniowych jest
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
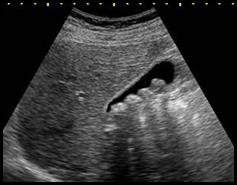
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
Co jest przyczyną artefaktu widocznego na obrazie MR?
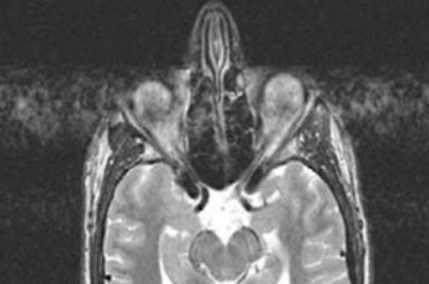
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
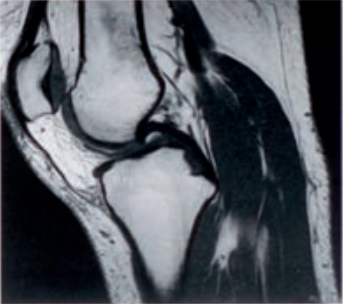
Które znaczniki są wykorzystywane w scyntygrafii tarczycy?
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
Podczas wykonywania badania EKG czarną elektrodę kończynową należy umieścić na kończynie dolnej
Podczas wykonywania zdjęcia rentgenowskiego klatki piersiowej w celu ochrony radiologicznej pacjenta należy zastosować
Na obrazie MR jamy brzusznej strzałką wskazano
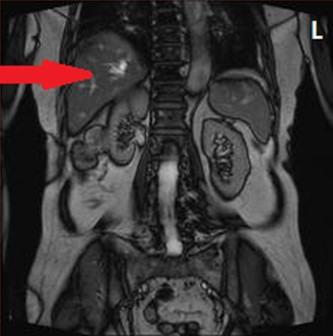
Technika stereotaktyczna polega na napromienianiu nowotworu
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
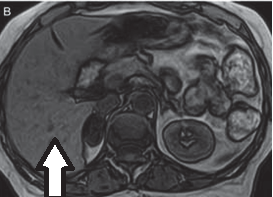
W trakcie obrazowania metodą rezonansu magnetycznego wykorzystywane jest zjawisko wysyłania sygnału emitowanego przez
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
Radioizotopowa terapia medycyny nuklearnej polega na wprowadzeniu do tkanek lub narządów radiofarmaceutyku
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
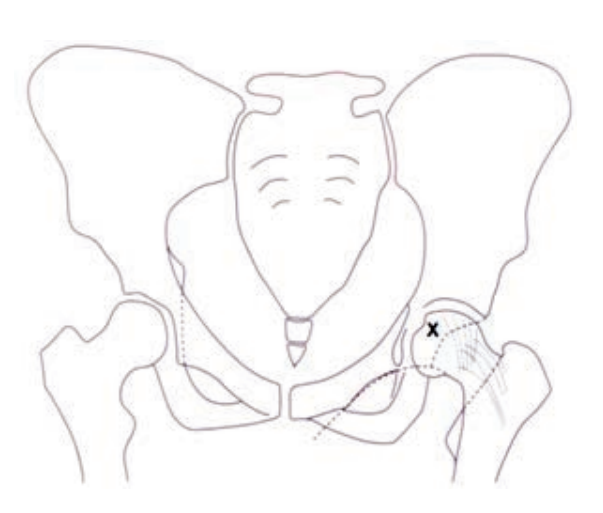
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Do zdjęcia prawych otworów międzykręgowych kręgosłupa szyjnego pacjent stoi w skosie
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
Które zdjęcia należy wykonać pacjentom z chorobą reumatoidalną stawów kolanowych?
Na scyntygramie tarczycy został uwidoczniony guzek
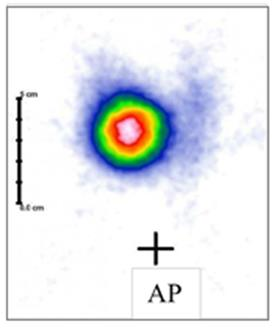
W radiologii stomatologicznej ząb o numerze 23 to kieł
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce