Pytanie 1
W leczeniu izotopowym tarczycy podaje się
Wynik: 32/40 punktów (80,0%)
Wymagane minimum: 20 punktów (50%)
W leczeniu izotopowym tarczycy podaje się
Którą strukturę anatomiczną oznaczono na obrazie rezonansu magnetycznego?
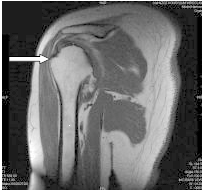
Zdjęcie którego zęba górnego zlecił na skierowaniu lekarz stomatolog?
Limfografia to badanie kontrastowe
Kto jest odpowiedzialny za wykonywanie testów podstawowych kontroli jakości gammakamery w Zakładzie Medycyny Nuklearnej?
W których projekcjach podstawowych wykonuje się standardowe badanie mammograficzne?
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
Na radiogramie TK głowy strzałką wskazano
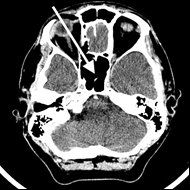
W leczeniu izotopowym tarczycy należy podać
Znak umieszczony w pracowni rezonansu magnetycznego zakazuje wstępu osobom

Do zdjęcia prawych otworów międzykręgowych kręgosłupa szyjnego pacjent stoi w skosie
Co jest przyczyną artefaktu widocznego na obrazie MR?
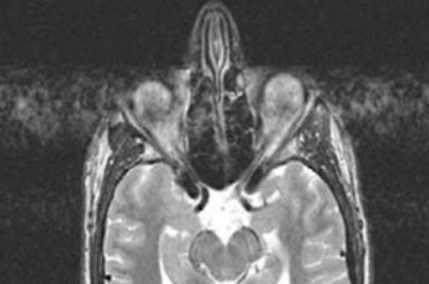
Hałas podczas badania tomografii rezonansu magnetycznego jest efektem ubocznym pracy
Ultrasonograficzne środki kontrastowe to
Zamieszczony rentgenogram został zarejestrowany podczas wykonania
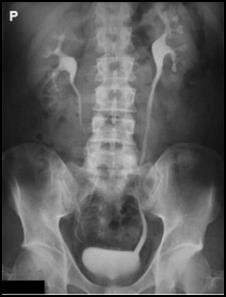
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
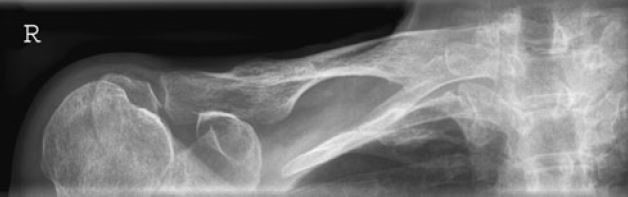
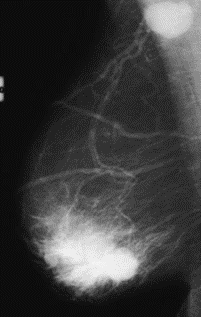
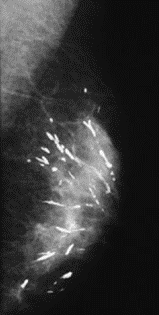
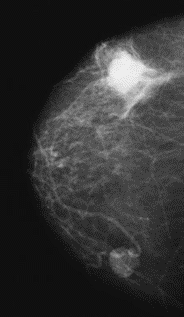
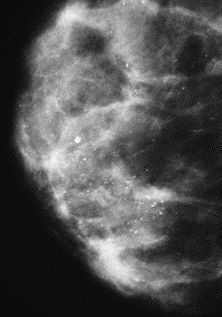
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?
Który radioizotop jest emiterem promieniowania alfa?
Zastosowana w badaniu radiologicznym kratka przeciwrozproszeniowa powoduje
Proces chemicznego wywoływania radiogramów polega na
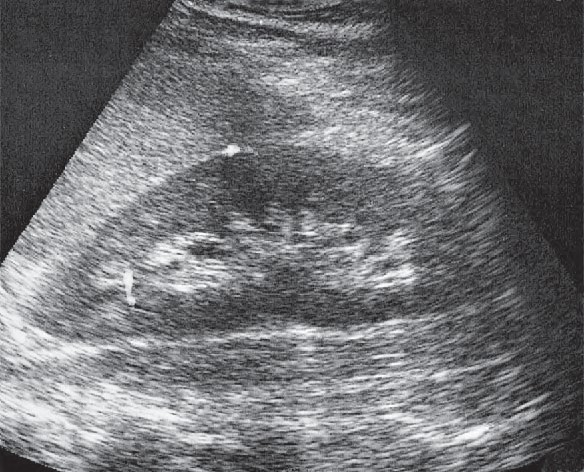
Który narząd widoczny jest na wydruku badania ultrasonograficznego?
Podczas teleradioterapii piersi lewej narządem krytycznym jest
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
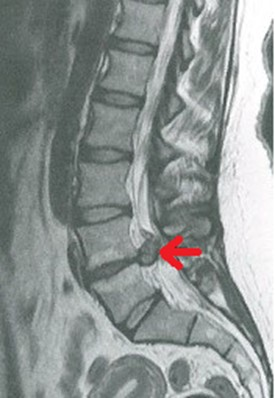
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
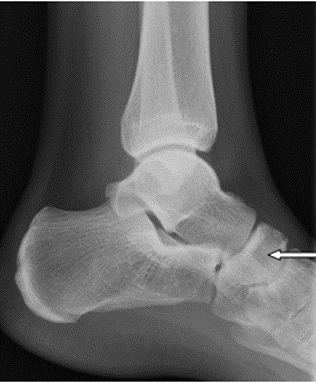
Na zamieszczonym radiogramie strzałką oznaczono kość
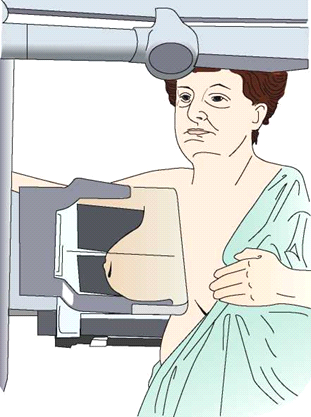
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
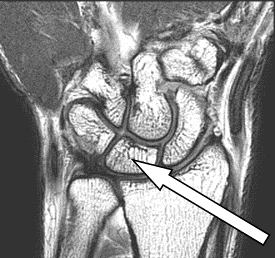
Na zamieszczonym obrazie RM nadgarstka lewego strzałką wskazano kość
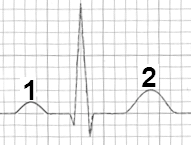
Który załamek odzwierciedla repolaryzację komór w zapisie EKG?
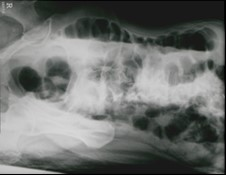
Które badanie zostało zarejestrowane na przedstawionym radiogramie?
Ile razy i jak zmieni się wartość natężenia promieniowania X przy zwiększeniu odległości OF ze 100 cm do 200 cm?
W badaniu EKG punktem przyłożenia odprowadzenia przedsercowego C2 jest
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
Na schemacie oznaczono
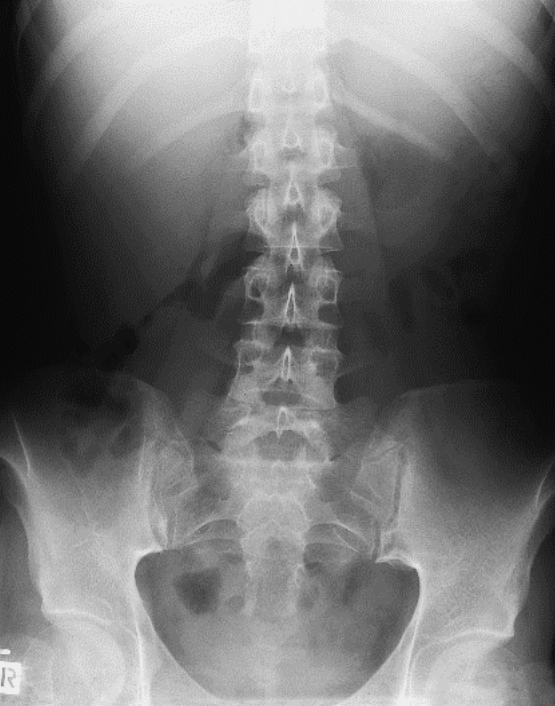
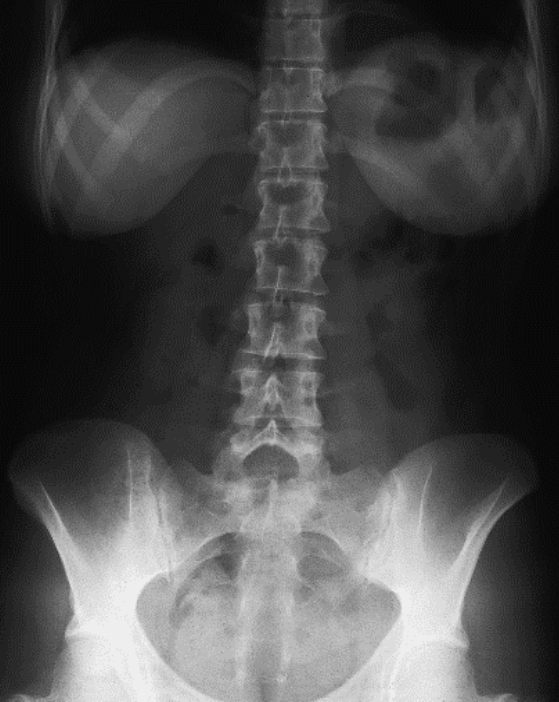
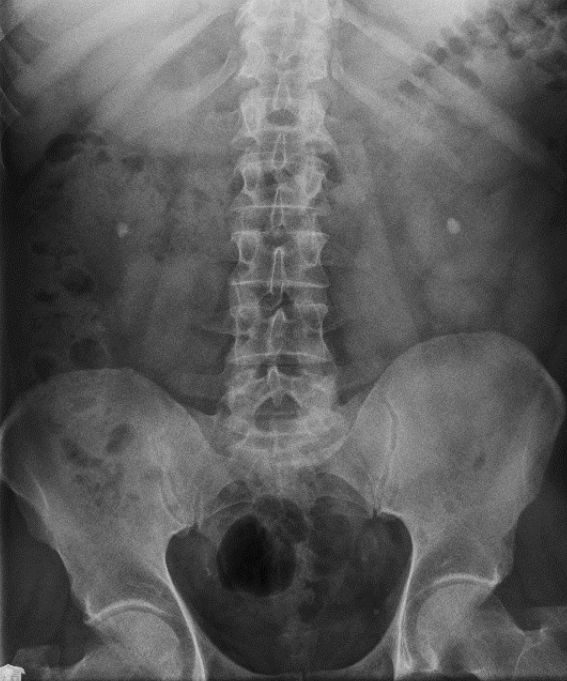
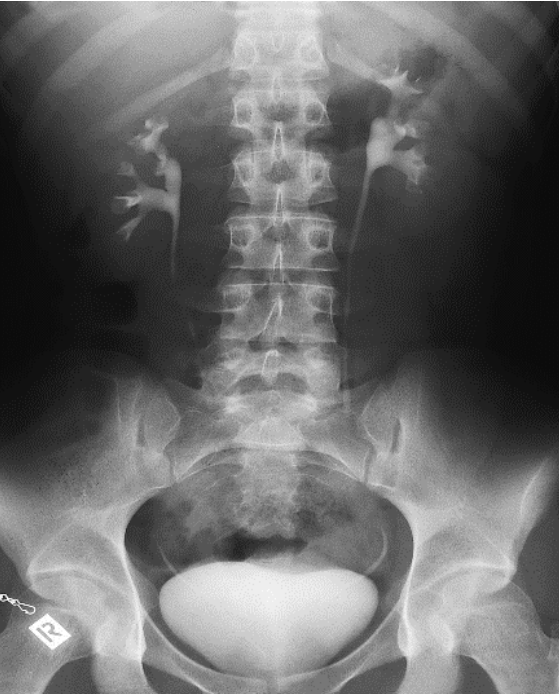
Na którym radiogramie uwidoczniona jest kamica nerkowa?
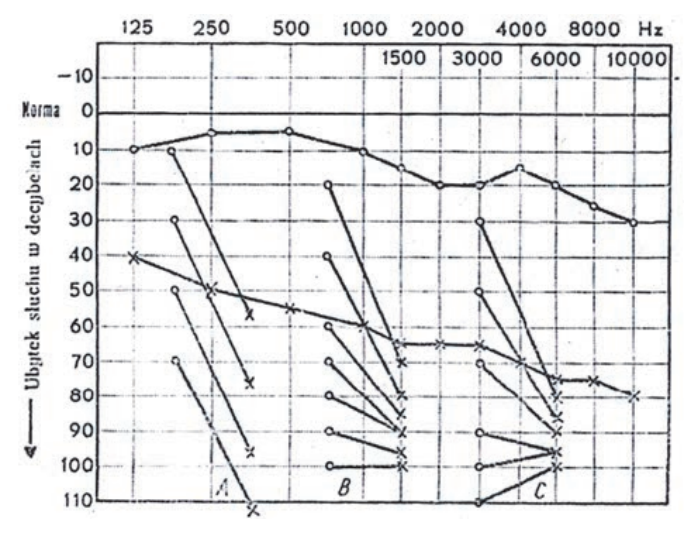
Audiogram przedstawia próbę
Do wczesnych odczynów popromiennych po radioterapii zalicza się
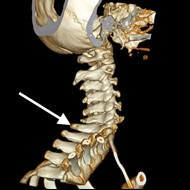
Na obrazie TK kręgosłupa strzałką wskazano wyrostek
Obrazowanie w sekwencjach STIR, FLAIR, SE wykonywane jest w badaniu