Pytanie 1
Korzystając z wykresu określ, której substancji można rozpuścić najwięcej w temperaturze 30°C.
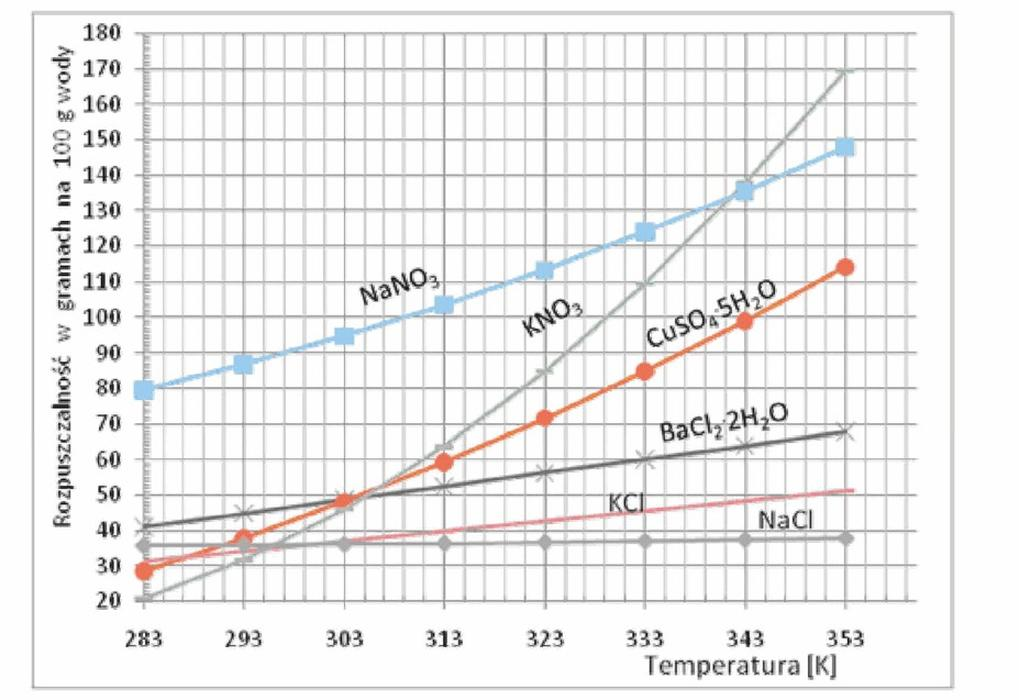
Wynik: 31/40 punktów (77,5%)
Wymagane minimum: 20 punktów (50%)
Korzystając z wykresu określ, której substancji można rozpuścić najwięcej w temperaturze 30°C.

Nie należy podgrzewać cieczy w szczelnie zamkniętych pojemnikach, ponieważ
Zestaw do filtracji nie zawiera
Jaką metodą nie można rozdzielać mieszanin?
Próbka wzorcowa to próbka
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Reakcja miedzi metalicznej z stężonym kwasem azotowym(V) prowadzi do powstania azotanu(V) miedzi(II) oraz jakiego związku?
Aby przeprowadzić syntezę substancji organicznej w temperaturze 150°C, należy zastosować łaźnię
50 cm3 alkoholu etylowego zmieszano w kolbie miarowej z 50 cm3 wody. W wyniku zjawiska kontrakcji objętość otrzymanego roztworu wyniosła 97,5 cm3. Ile wynosi stężenie procentowe (v/v) roztworu alkoholu w wodzie po zmieszaniu i stężenie procentowe roztworu alkoholu (v/v) po uzupełnieniu kolby wodą do 100 cm3?
| Stężenie procentowe (v/v) roztworu alkoholu w wodzie po zmieszaniu | Stężenie procentowe (v/v) roztworu alkoholu po uzupełnieniu kolby wodą do 100 cm3 | |
|---|---|---|
| A. | 49,2% | 48,0% |
| B. | 50,0% | 49,7% |
| C. | 51,3%, | 50,0% |
| D. | 53,3% | 50,2% |
Jaką masę siarczanu(VI) miedzi(II)-woda(1/5) należy poddać suszeniu, aby otrzymać 300 g soli bezwodnej?
| CuSO4 · 5H2O → CuSO4 + 5H2O |
| (MCuSO4·5H2O = 249,5 g/mol, MCuSO4 = 159,5 g/mol, MH2O = 18,0 g/mol) |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Metoda oczyszczania substancji, która opiera się na różnicy w rozpuszczalności substancji docelowej oraz zanieczyszczeń w zastosowanym rozpuszczalniku, nosi nazwę
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Naczynia miarowe o kształcie rurek poszerzonych w środku, z wąskim i wydłużonym dolnym końcem, przeznaczone do pobierania i transportowania cieczy o ściśle określonej objętości, to
Z próbek przygotowuje się ogólną próbkę
Wodę do badań mikrobiologicznych powinno się pobierać do butelek
Aby zebrać próbki gazów, wykorzystuje się
Jakie środki stosuje się do czyszczenia szkła miarowego, które zostało zanieczyszczone substancjami tłustymi?
Na etykiecie kwasu siarkowego(VI) znajduje się zapis:
Określ gęstość kwasu siarkowego(VI).
KWAS SIARKOWY MIN. 95% CZ.D.A. H2SO4 M = 98,08 g/mol 1 l – 1,84 kg |
Metodą, która nie umożliwia przeniesienia składników próbki do roztworu, jest
Technika oddzielania płynnych mieszanin, w której wykorzystuje się różnice w prędkości migracji składników przez odpowiednią bibułę, nazywa się
Na podstawie zamieszczonych w tabeli opisów metod rozdzielania mieszanin, dobierz odpowiadające im nazwy.
| Tabela. Metody rozdzielania mieszanin | |
|---|---|
| Lp. | Opis metody |
| I. | Zlewanie cieczy znad osadu. |
| II. | Przeprowadzenie ciekłego rozpuszczalnika w stan pary. |
| III. | Wyodrębnianie z mieszaniny ciał stałych lub cieczy składnika przy pomocy rozpuszczalnika tak dobranego, aby rozpuszczał żądany związek chemiczny. |
| IV. | Powolne opadanie cząstek substancji stałej w cieczy pod wpływem własnego ciężaru. |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Odważka analityczna przygotowana w fabryce zawiera 0,1 mola EDTA. Posiadając taką jedną odważkę analityczną, jakie roztwory można przygotować?
Roztwór amoniaku o stężeniu 25% nie powinien być trzymany
Sód powinien być przechowywany
Aby wykonać chromatografię cienkowarstwową, należy przygotować eluent składający się z toluenu, acetonu oraz kwasu mrówkowego w proporcjach objętościowych 10:4:1. Jakie ilości poszczególnych składników powinny być wykorzystane do uzyskania 300 cm3 eluentu?
250 cm3 roztworu kwasu octowego o stężeniu 10% objętościowych zostało rozcieńczone pięciokrotnie. Jakie jest stężenie otrzymanego roztworu?
Aby oszacować czystość MgCO3, poddano prażeniu próbkę o wadze 5 g tej soli aż do osiągnięcia stałej masy. W trakcie prażenia zachodzi reakcja:
MgCO3 → MgO + CO2 Całkowity ubytek masy wyniósł 2,38 g.
(Masy molowe reagentów to: MgCO3 – 84 g/mol, MgO – 40 g/mol, CO2 – 44 g/mol) Jaką czystość miała próbka węglanu magnezu?
Które z poniższych równań ilustruje reakcję, w której powstają produkty gazowe?
W celu rozdrabniania niewielkich ilości bardzo twardego materiału wykorzystuje się moździerze
Proces, w którym woda jest usuwana z zamrożonego materiału poprzez sublimację lodu
(czyli bezpośrednie przejście do stanu pary z pominięciem stanu ciekłego) nazywa się
Czy próbkę laboratoryjną przechowuje się w lodówce, gdy występuje w niej
Co oznacza zapis cz.d.a. na etykiecie opakowania odczynnika chemicznego?
Aby oddzielić mieszankę etanolu i wody, konieczne jest przeprowadzenie procesu
Próbka pobrana z próbki ogólnej, która odzwierciedla cechy partii produktu, określa się jako próbka
Aparat przedstawiony na ilustracji służy do

Zgodnie z zasadami BHP w laboratorium, po zakończeniu pracy z odczynnikami chemicznymi należy: