Pytanie 1
Ile razy i jak zmieni się wartość natężenia promieniowania X przy zwiększeniu odległości OF ze 100 cm do 200 cm?
Wynik: 30/40 punktów (75,0%)
Wymagane minimum: 20 punktów (50%)
Ile razy i jak zmieni się wartość natężenia promieniowania X przy zwiększeniu odległości OF ze 100 cm do 200 cm?
Testy specjalistyczne aparatów rentgenowskich do zdjęć wewnątrzustnych są przeprowadzane
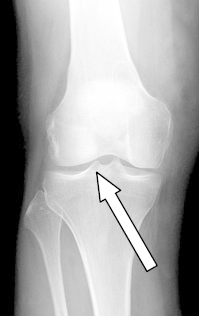
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
W metodzie RM (rezonansu magnetycznego) po umieszczeniu pacjenta w silnym, stałym polu magnetycznym dochodzi do oddziaływania
Podczas badania EEG otwarcie oczu powoduje
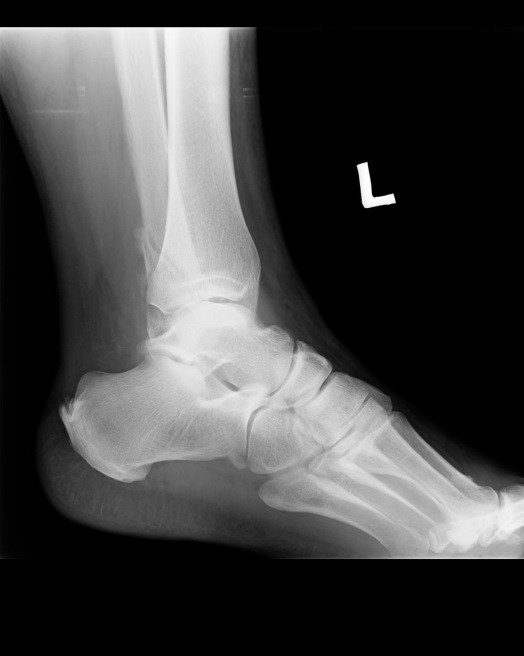
Na obrazie radiologicznym uwidoczniono złamanie kości
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
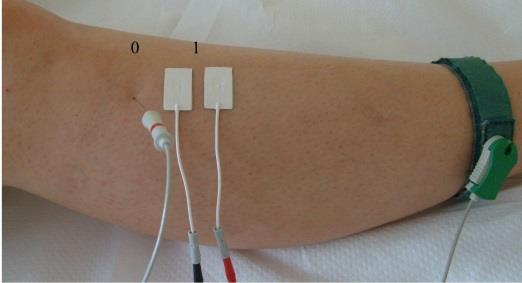
Na ilustracji przedstawiono przygotowanie pacjenta do badania
Fistulografia to badanie kontrastowe
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
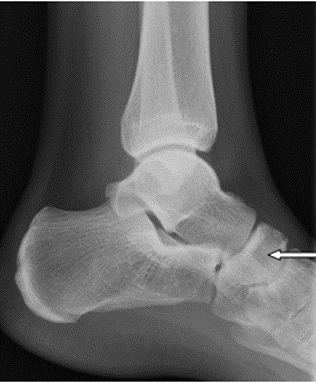
Na zamieszczonym radiogramie strzałką oznaczono kość
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
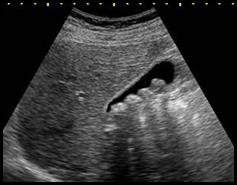
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
Na prawidłowo wykonanym zdjęciu zatok w projekcji PA górny zarys piramid rzutuje się
W pracowni radioterapii wyświetlenie na ekranie monitora aparatu komunikatu „ROTATION” oznacza prowadzoną terapię
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
Wskazaniem do wykonania przesiewowego badania densytometrycznego jest
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
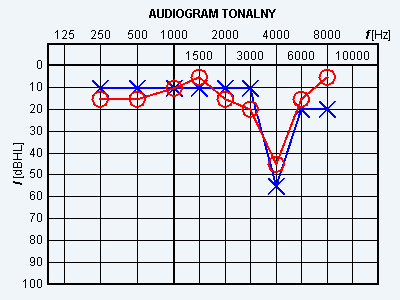
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
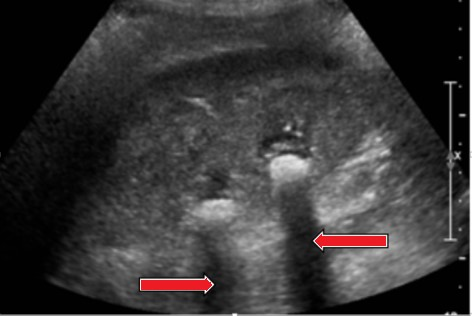
Który artefakt wskazano strzałkami na obrazie USG nerki?
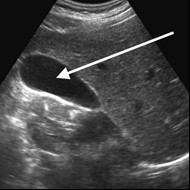
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
Zwiększenie napięcia na lampie rentgenowskiej powoduje
Technikę bramkowania oddechowego stosuje się w badaniu MR
Na radiogramie uwidoczniono złamanie nasady
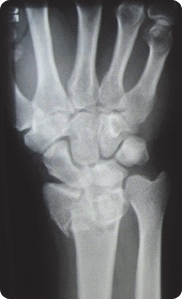
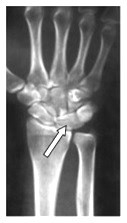
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
W systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej oznacza się symbolem
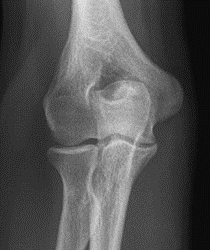
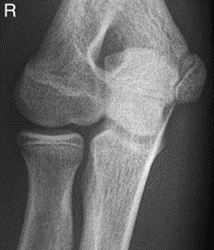
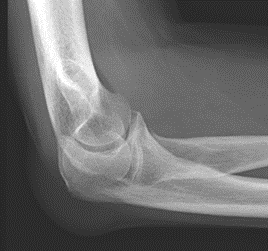
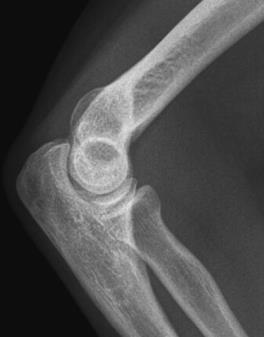
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
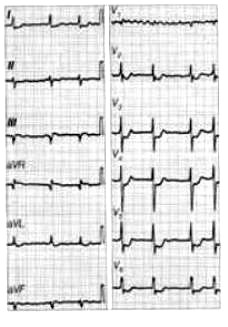
Na elektrokardiogramie uwidoczniono
Zwiększenie napięcia na lampie rentgenowskiej powoduje
W radiografii mianem SID określa się
Pielografia zstępująca umożliwia diagnostykę
Ligand stosuje się
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Cholangiografia to badanie radiologiczne