Pytanie 1
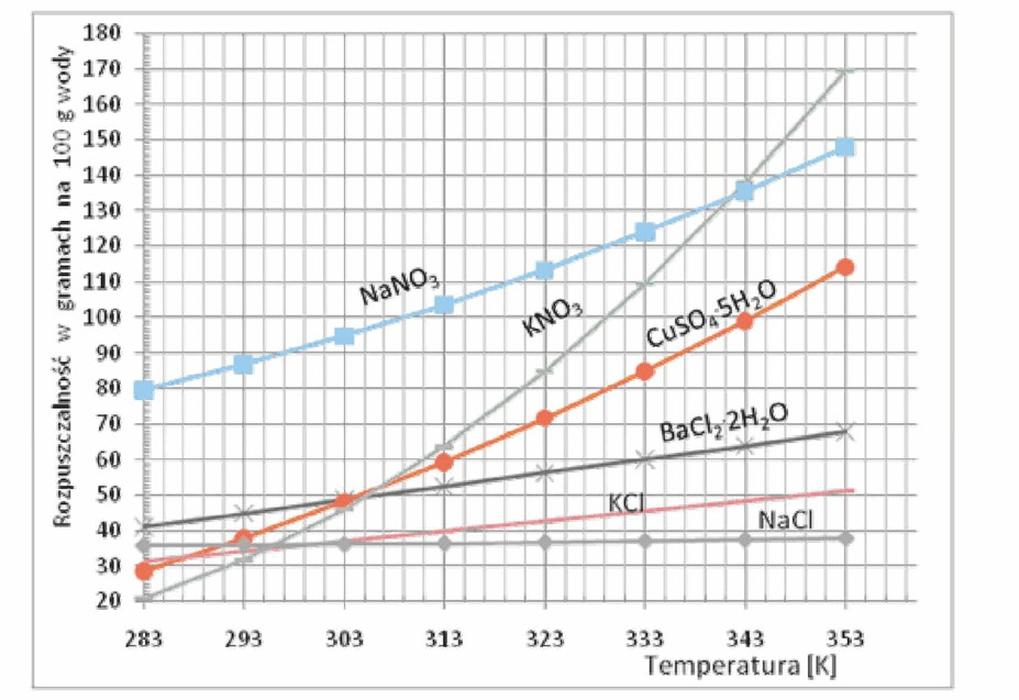
Korzystając z wykresu określ, w jakiej temperaturze należy rozpuszczać azotan(V) potasu, aby całkowicie rozpuścić 110 g soli w 100 g wody.
Wynik: 30/40 punktów (75,0%)
Wymagane minimum: 20 punktów (50%)
Korzystając z wykresu określ, w jakiej temperaturze należy rozpuszczać azotan(V) potasu, aby całkowicie rozpuścić 110 g soli w 100 g wody.

W przypadku kontaktu ze stężonym roztworem zasady, co należy zrobić jak najszybciej?
Jakie oznaczenie znajduje się na naczyniach szklanych kalibrowanych do wlewu?
Jaką metodą nie można rozdzielać mieszanin?
Wybór lokalizacji do poboru próbek wody z rzeki nie jest uzależniony od
Procedura oznaczenia kwasowości mleka. Do wykonania analizy, zgodnie z powyższą procedurą, potrzebne są
| Do kolby stożkowej o pojemności 300 cm3 pobrać dokładnie 25 cm3 badanego mleka i rozcieńczyć wodą destylowaną do objętości 50 cm3. Dodać 2-3 krople fenoloftaleiny i miareczkować mianowanym roztworem wodorotlenku sodu do uzyskania lekko różowego zabarwienia. |
Przedstawiony na rysunku zagłębnik stosuje się do pobierania próbek
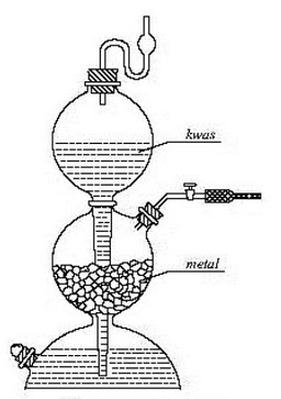
Na rysunku przedstawiono aparat
Średnia masa wody wypływająca z pipety o deklarowanej pojemności 25 cm3, w temperaturze 25°C wynosi 24,80 g. Korzystając z danych zamieszczonych w tabeli wskaż wartość poprawki kalibracyjnej dla tej pipety.
| Masa wody zajmującej objętość 1 dm3 w zależności od temperatury pomiaru | |
|---|---|
| Temperatura °C | Masa wody g |
| 20 | 997,17 |
| 21 | 997,00 |
| 22 | 996,80 |
| 23 | 996,59 |
| 24 | 996,38 |
| 25 | 996,16 |
| 26 | 995,93 |
| 27 | 995,69 |
| 28 | 995,45 |
| 29 | 995,18 |
| 30 | 994,92 |
W jakim celu używa się kamyczków wrzenne w trakcie długotrwałego podgrzewania cieczy?
W procesie oddzielania osadu od roztworu, po przeniesieniu osadu na sączek, najpierw należy go
Próbka, której celem jest ustalenie poziomu składników, dla których oznaczenia przygotowane przez różne laboratoria są niezgodne, to próbka
Wskaź sprzęt laboratoryjny, który znajduje się w zestawie do filtracji pod obniżonym ciśnieniem?
W wyniku reakcji 100 g azotanu(V) ołowiu(II) z jodkiem potasu otrzymano 120 g jodku ołowiu(II). Wydajność reakcji wyniosła
| Pb(NO3)2 + 2KI → PbI2 + 2KNO3 | |
| (MPb(NO3)2 = 331 g/mol, MKI = 166 g/mol, MPbI2 = 461 g/mol, MKNO3 = 101 g/mol) |
Zabieg, który wykonuje się podczas pobierania próbki wody do analizy, mający na celu zachowanie jej składu chemicznego w trakcie transportu, określa się mianem
W trakcie korzystania z odczynnika opisanego na etykiecie, należy szczególnie zwrócić uwagę na zagrożenia związane
Laboratoryjny stół powinien być zaopatrzony w instalację gazową oraz
Naczynia miarowe o kształcie rurek poszerzonych w środku, z wąskim i wydłużonym dolnym końcem, przeznaczone do pobierania i transportowania cieczy o ściśle określonej objętości, to
Wagi laboratoryjne można klasyfikować według nośności oraz precyzji na
Po zmieszaniu wszystkie pierwotne próbki danej partii materiału tworzą próbkę
Jakie środki stosuje się do czyszczenia szkła miarowego, które zostało zanieczyszczone substancjami tłustymi?
Dla cieczy bezbarwnej odczyt w biurecie pokazanej na rysunku wynosi

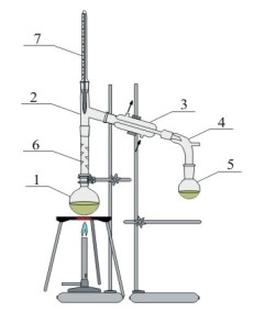
Na rysunku numerem 3 oznaczono
Technika oddzielania płynnych mieszanin, w której wykorzystuje się różnice w prędkości migracji składników przez odpowiednią bibułę, nazywa się
Nie należy używać gorącej wody do mycia
Skrót "cz." na etykiecie odczynnika chemicznego wskazuje, że
Na podstawie zamieszczonych informacji, wskaż ilości odczynników, które są niezbędne do przygotowania skali wzorców do kolorymetrycznego oznaczania rozpuszczalnych fosforanów(V).
| Przygotowanie skali wzorców do kolometrycznego oznaczania fosforanów(V) | ||||||||
| Do ośmiu cylindrów Nesslera o pojemności 100 cm3 odmierzyć kolejno wzorcowy roztwór roboczy KH2PO4 według poniższej tabeli SKALA WZORCÓW (PO43-) i uzupełnić wodą do kreski. Do każdego cylindra dodać 2 cm3 roztworu molibdenianu amonu (heksaamonoheptamolibdenian(VI)), wymieszać, dodać 0,2 cm3 roztworu SnCl2 i ponownie wymieszać. | ||||||||
| SKALA WZORCÓW (PO43-) | ||||||||
| Wzorcowy roztwór roboczy [cm3] | 0,0 | 0,5 | 1,0 | 2,0 | 3,0 | 5,0 | 7,0 | 10,0 |
| Zawartość PO43- [mg] | 0,0 | 0,005 | 0,01 | 0,02 | 0,03 | 0,05 | 0,07 | 0,10 |
| Roztwór | KH₂PO₄ | (NH₄)₆Mo₇O₂₄ | SnCl₂ |
|---|---|---|---|
| A. | 28,5 cm³ | 8,0 cm³ | 0,16 cm³ |
| B. | 0,285 cm³ | 16,0 cm³ | 1,6 cm³ |
| C. | 28,5 cm³ | 16,0 cm³ | 1,6 cm³ |
| D. | 0,285 cm³ | 8,0 cm³ | 16 cm³ |
W trakcie destylacji cieczy wykorzystuje się tzw. kamienie wrzenne, ponieważ
Jakie urządzenie wykorzystuje się do pomiaru lepkości cieczy?
Roztwór zawierający 16,00 g siarczanu(VI) miedzi(II) nasycono siarkowodorem. Masa wytrąconego siarczku miedzi(II), po odsączeniu i wysuszeniu, wynosiła 8,64 g. Oblicz procentową wydajność tej reakcji.
Równanie reakcji:
\( \text{CuSO}_4 + \text{H}_2\text{S} \rightarrow \text{CuS} + \text{H}_2\text{SO}_4 \)
\( \text{M CuSO}_4 = 160 \, \text{g/mol} \)
\( \text{M CuS} = 96 \, \text{g/mol} \)
Temperatura topnienia mocznika wynosi 133 °C. W celu określenia czystości preparatów tej substancji, przeprowadzono badania temperatury ich topnienia, uzyskując wyniki przedstawione w tabeli. Wskaż preparat o najmniejszym stopniu czystości.
| Preparat | A | B | C | D |
|---|---|---|---|---|
| Zakres temperatury topnienia [°C] | 132-133 | 130-133 | 125-133 | 128-133 |
Reagenty o czystości na poziomie 99,999% — 99,9999% to reagenty
Aby ustalić miano roztworu wodnego NaOH, należy zastosować
Jakie metody można zastosować do rozdzielania i koncentracji składników próbki?
Sprzęt laboratoryjny przedstawiony na ilustracji stanowi element zestawu do

Aby oddzielić mieszankę etanolu i wody, konieczne jest przeprowadzenie procesu
Jakie urządzenie wykorzystuje się do pobierania próbek gazów?
Użycie płuczek jest konieczne w trakcie procesu
Przykładem piany stałej jest
| faza rozproszona | faza rozpraszająca | ||
|---|---|---|---|
| gaz | ciecz | ciało stałe | |
| gaz | - | piana | piana stała |
| ciecz | aerozol ciekły | emulsja | emulsja stała |
| ciało stałe | aerozol stały | zol | zol stały |
Aparat przedstawiony na ilustracji służy do
