Pytanie 1
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Wynik: 31/40 punktów (77,5%)
Wymagane minimum: 20 punktów (50%)
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
W pracowni radioterapii wyświetlenie na ekranie monitora aparatu komunikatu „ROTATION” oznacza prowadzoną terapię
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




Podczas teleradioterapii piersi lewej narządem krytycznym jest
Który detektor w radiografii wymaga laserowego czytnika obrazu?
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
W badaniu PETCT radioizotop ulega
Radioizotopowa terapia medycyny nuklearnej polega na wprowadzeniu do tkanek lub narządów radiofarmaceutyku
Wiązka elektronów najczęściej stosowana jest do leczenia zmian nowotworowych w obrębie
Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
W badaniu PET CT wykorzystuje się radioizotopy emitujące promieniowanie
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Przedstawiony obraz został zarejestrowany podczas wykonywania
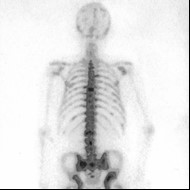
Zwiększenie napięcia na lampie rentgenowskiej powoduje
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
Który radioizotop jest stosowany w diagnostyce i terapii raka tarczycy?
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę
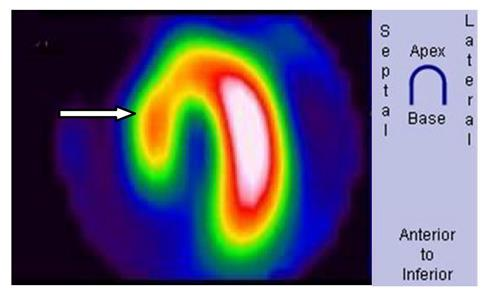
Obrazy DDR są tworzone w trakcie
Który środek ochrony radiologicznej pacjenta należy zastosować podczas wykonywania zdjęcia bocznego kręgosłupa szyjnego?
Jaki jest cel stosowania bolusa w radioterapii?
Warstwa półchłonna (WP) służy do obliczania
Elementem systemu rejestracji obrazu, w którym fotony promieniowania X są bezpośrednio konwertowane na sygnał elektryczny, jest
Na zarejestrowanych obrazach badania renoscyntygraficznego widać, że prawa nerka pacjenta
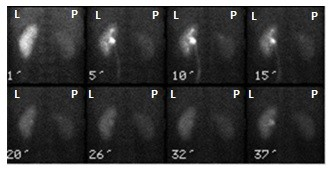
Skrótem CTV w radioterapii oznacza się
Rozpraszanie promieniowania X, w wyniku którego następuje zwiększenie długości fali promieniowania, to zjawisko
Jaka jest standardowa odległość OF do wykonania rentgenowskich zdjęć kości i stawów kończyny górnej?
Ligand stosuje się
Który radioizotop jest emiterem promieniowania alfa?
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
Na scyntygramie tarczycy został uwidoczniony guzek
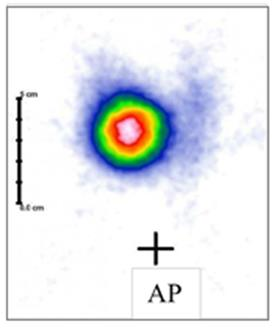
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Które urządzenia pomocnicze służą do unieruchomienia pacjenta do zabiegu radioterapii?
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
W technice napromieniania SSD mierzona jest odległość źródła promieniowania