Pytanie 1
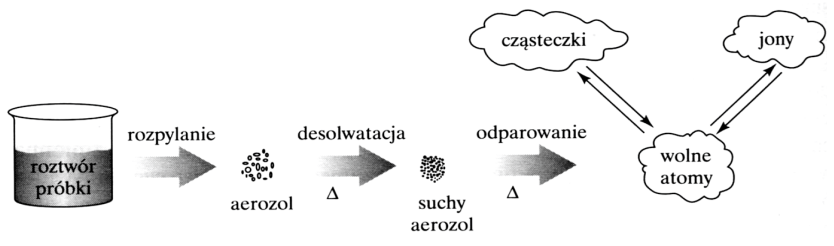
Na schemacie przedstawiono procesy, które zachodzą podczas przygotowania próbek do badań z wykorzystaniem
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
Na schemacie przedstawiono procesy, które zachodzą podczas przygotowania próbek do badań z wykorzystaniem

Jakim urządzeniem określa się temperaturę zapłonu oleju opałowego?
Obecność skrobi w bulwie ziemniaka można wykryć, stosując
Zespół enzymów, obecny zarówno w organizmach roślinnych, jak i zwierzęcych, który katalizuje proces hydrolizy wiązań peptydowych w białkach oraz peptydach, to
Aby przeprowadzić analizę gleby, przygotowuje się jej zawiesinę w wodzie destylowanej lub w roztworze neutralnej soli, na przykład KCl, w celu określenia jej
W zamieszczonym opisie przedstawiono fragment instrukcji obsługi
| Umieść probówki w adapterach. Zawsze umieszczaj probówki symetrycznie celem prawidłowego wyważenia rotora. W przypadku użycia tylko jednej probówki niezbędne jest umieszczenie przeciwwagi po stronie przeciwnej. Po zamknięciu pokrywy zostaje ona automatycznie zablokowana ... |
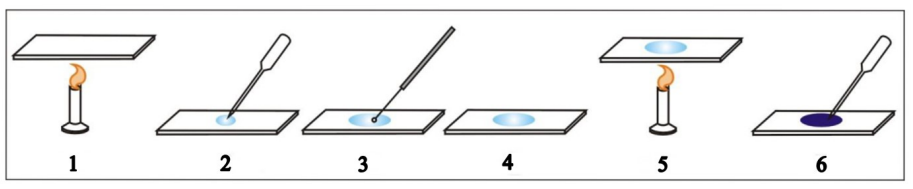
Rysunek przedstawia poszczególne etapy wykonania preparatu mikroskopowego utrwalonego. Cyfrą 3 oznaczono
Jakie warunki powinny panować w pomieszczeniu, w którym znajdują się wagi?
| Temperatura | Wilgotność | |
|---|---|---|
| A. | 20-25 °C | 30-80% |
| B. | 20-25 °C | 20-60% |
| C. | 15-30 °C | 30-80% |
| D. | 15-30 °C | 20-60% |
Korzystając ze wzoru, oblicz zawartość tlenu (w procentach nasycenia X) w próbce wody, jeżeli stężenie rozpuszczonego w niej tlenu wynosi 7,7 mg/dm3, a temperatura wody jest równa 284 K.
| Temperatura °C | Rozpuszczalność O2 mg/dm3 |
|---|---|
| 0 | 14,64 |
| 1 | 14,22 |
| 3 | 13,44 |
| 5 | 12,74 |
| 7 | 12,11 |
| 9 | 11,53 |
| 11 | 11,00 |
| 13 | 10,53 |
| 15 | 10,08 |
| 17 | 9,66 |
| 19 | 9,27 |
| X = a · 100% b |
| gdzie: a – oznaczona zawartość tlenu rozpuszczonego w wodzie, mg/dm3 b – rozpuszczalność O2, mg/dm3 |
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
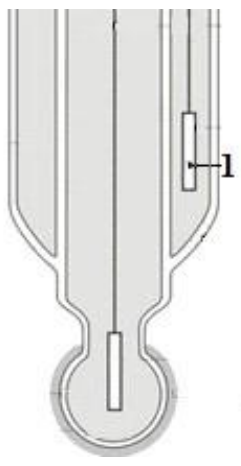
Na rysunku przedstawiono schemat szklanej elektrody zespolonej. Cyfrą 1 oznaczono
Analizując próbkę wody powierzchniowej stwierdzono, że zawartość azotanów wynosi 4,5 mg/dm3, siarczanów 120 mg/dm3, a stężenie jonów chlorkowych 180 mg/dm3. Na podstawie danych zawartych w tabeli wskaż klasę czystości wody, z której została pobrana próbka.
| Wartości graniczne wskaźników jakości wody w klasach jakości wód powierzchniowych | |||||
|---|---|---|---|---|---|
| Wskaźnik [mg/dm³] | I klasa czystości | II klasa czystości | III klasa czystości | IV klasa czystości | V klasa czystości | Wartości dopuszczalne |
| azotany | 5,0 | 15,0 | 25,0 | 50,0 | >50,0 |
| siarczany | 100 | 150 | 250 | 300 | > 300 |
| chlorki | 100 | 200 | 300 | 400 | > 400 |
Skręcalność optyczną cukrów mierzy się przy użyciu
Jaką metodę kontroli stanu mikrobiologicznego powietrza opisano w ramce?
| Otwarte płytki Petriego z podłożem stałym pozostawiono na 30 minut na wysokości 1 metra od podłogi, a następnie inkubowano przez 48 godzin w temperaturze 37°C. Po tym czasie wyhodowane kolonie zliczono i zidentyfikowano ich szczepy. |
W jakiej metodzie analizy instrumentalnej wykorzystuje się zdolność substancji optycznie aktywnej do skręcania płaszczyzny światła spolaryzowanego?
W dwóch nieoznaczonych probówkach znajdują się roztwory: w jednej – glukozy, a w drugiej - sacharozy. Jakiego odczynnika trzeba użyć, aby rozpoznać glukozę?
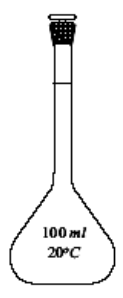
Wskaż, w jakim rodzaju analizy stosowany jest sprzęt przedstawiony na rysunku.
Reakcja ksantoproteinowa umożliwia identyfikację aminokwasu, który zawiera w swojej budowie
Jaką metodą można ustalić ilość tłuszczów w produktach pochodzenia roślinnego?
Lakmus to wskaźnik pH, który w roztworze zasadowym zmienia kolor na
W ramce scharakteryzowano odczynniki
| Łączą się z danym jonem ubocznym, wiążąc go w trwałe zespoły i tym samym wyłączają go z udziału w roztworze lub obniżają znacznie jego stężenie. |
Oceniając organoleptycznie wodę przeznaczoną do picia przez ludzi, należy określić między innymi
Ze względu na zmieniającą się podczas miareczkowania objętość badanego roztworu, należy obliczyć poprawkę p w przypadku miareczkowania
| p = Vpróbki + Vwody + Vtitrantu Vpróbki + Vwody |
Wskaż błędnie określone efekty reakcji analitycznych kationów I grupy.
| Odczynnik strącający | Reakcje analityczne | |||
|---|---|---|---|---|
| Ag+ | Hg22+ | Pb2+ | ||
| A. | HCl | biały osad AgCl rozpuszczalny w NH3·H2O | biały osad Hg2Cl2 | biały osad PbCl2 rozpuszczalny w gorącej wodzie |
| B. | H2SO4 | biały Ag2SO4 (ze stężonych roztworów), rozpuszczalny w gorącej wodzie | biały osad Hg2SO4 rozpuszczalny w wodzie królewskiej | biały osad PbSO4 rozpuszczalny w roztworze NaOH |
| C. | NaOH | brunatny osad Ag2O rozpuszczalny w NH3·H2O | czarny osad HgO i Hg | biały osad Pb(OH)2 rozpuszczalny w roztworze NaOH |
| D. | NH3aq | brunatny jon kompleksowy Ag(NH3)2+ | biały osad soli amidortęciowej rozpuszczalny w stężonym HNO3 | żółty osad Pb(OH)2 rozpuszczalny w gorącej wodzie |
Gdy podczas analizy ilościowej wyniki są zbliżone do wartości rzeczywistej, mówi się wtedy o
Pomiarów wykonywanych z użyciem wysokosprawnego chromatografu cieczowego dokonuje się w ramach
To pytanie jest dostępne tylko dla zalogowanych użytkowników. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
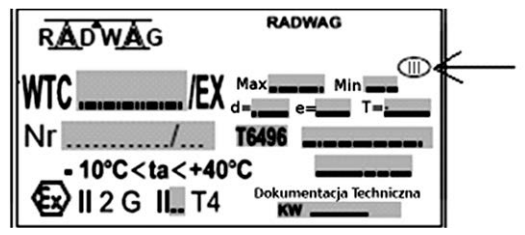
Strzałka zamieszczona na rysunku, przedstawiającym tabliczkę znamionową wagi, wskazuje na
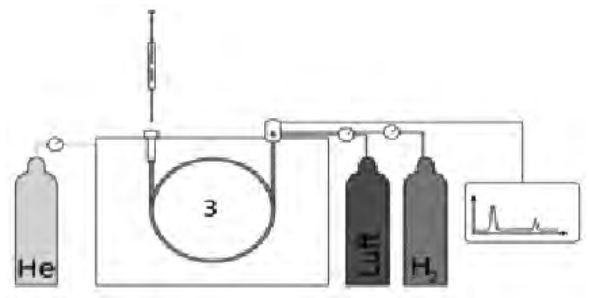
Na rysunku przedstawiającym schemat chromatografu gazowego numerem 3 oznaczono
Oznaczono LZ i LJ dla czterech różnych próbek tłuszczów. Wyniki zestawiono w tabeli:
Na podstawie zamieszczonych danych o liczbach właściwych wybranych tłuszczów wskaż próbkę, którą stanowi olej rzepakowy.
| Liczby właściwe wybranych tłuszczów | ||
|---|---|---|
| Rodzaj tłuszczu | Liczba zmydlania (LZ) mg KOH / g tłuszczu | Liczba jodowa (LJ) g I₂ / 100 g tłuszczu |
| Olej lniany | 187 – 197 | 169 – 192 |
| Olej sojowy | 188 – 195 | 114 – 138 |
| Olej rzepakowy | 167 – 179 | 94 – 106 |
| Tran wielorybi | 170 – 202 | 102 – 144 |
| Masło krowie | 218 – 245 | 25 – 38 |
| Smalec wieprzowy | 193 – 200 | 46 – 66 |
| Próbka | Liczba zmydlania (LZ) | Liczba jodowa (LJ) |
|---|---|---|
| 1 | 190 | 140 |
| 2 | 171 | 99 |
| 3 | 194 | 105 |
| 4 | 195 | 60 |
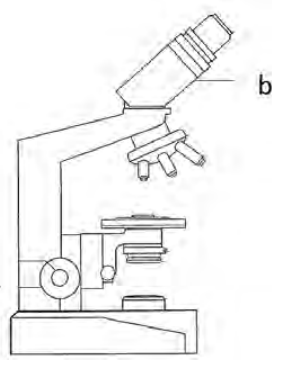
Na rysunku przedstawiającym schemat mikroskopu optycznego literą b oznaczono
W celu wykonania posiewu redukcyjnego należy nanieść drobnoustroje na podłoże, a następnie
| A. | 1. wyżarzyć ezę, 2. obrócić szalkę, 3. ponownie nanosić drobnoustroje, zahaczając przynajmniej raz o wcześniejszą ścieżkę. |
| B. | 1. nie wyżarzać ezy, 2. obrócić szalkę, 3. ponownie nanosić drobnoustroje, zahaczając przynajmniej raz o wcześniejszą ścieżkę. |
| C. | 1. wyżarzyć ezę, 2. obrócić szalkę, 3. ponownie nanosić drobnoustroje, nie zahaczając ani razu o wcześniejszą ścieżkę. |
| D. | 1. wyżarzyć ezę, 2. pozostawić szalkę w tym samym miejscu, 3. ponownie nanosić drobnoustroje, zahaczając przynajmniej raz o wcześniejszą ścieżkę. |
W analizowanej próbce oznaczono obecność baru, wytrącając go jako BaSO4. Otrzymano osad o masie 200 mg. Jaka była zawartość baru w próbce, jeśli mnożnik analityczny wynosi 0,5885?
Analiza składników chemicznych próbki substancji organicznej odbywa się w badaniu
Gęstość wody w temperaturze 25oC wynosi
| T [K] | ||
|---|---|---|
| T [K] | d [g/cm³] | η [cP] |
| 293 | 0,99823 | 1,0050 |
| 298 | 0,99707 | 0,8937 |
| 303 | 0,99567 | 0,8007 |
| 308 | 0,99406 | 0,7225 |
| 313 | 0,99222 | 0,6560 |
| 318 | 0,99025 | 0,5988 |
| 323 | 0,98807 | 0,5494 |
| 328 | 0,98573 | 0,5064 |
| 333 | 0,98324 | 0,4688 |
Dostanie się do środowiska pałeczek Salmonella, hodowanych na podłożach mikrobiologicznych, skutkuje
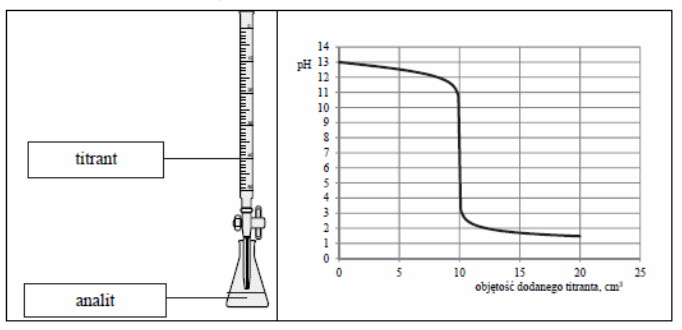
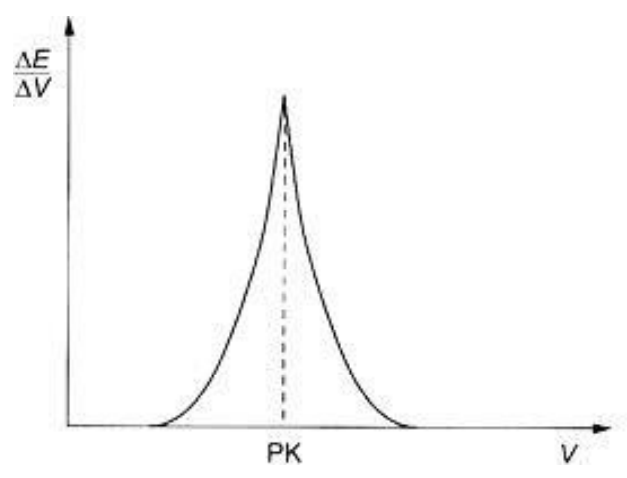
Na rysunku przedstawiono wyznaczanie punktu końcowego miareczkowania metodą
Aby przygotować podłoże do badań mikrobiologicznych, należy
Analiza, która opiera się na kontrolowanym wprowadzaniu roztworu o znanym stężeniu do badanego roztworu, to metoda oznaczeń ilościowych zwana
Które równanie przedstawia reakcję wytrącania osadu?