Pytanie 1
Na radiogramie uwidoczniono złamanie
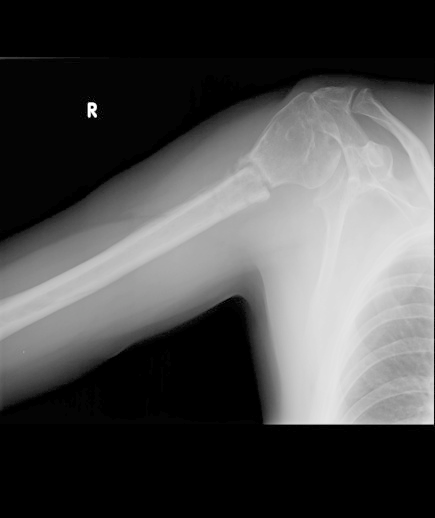
Wynik: 31/40 punktów (77,5%)
Wymagane minimum: 20 punktów (50%)
Na radiogramie uwidoczniono złamanie

Przedstawiony zapis elektrokardiograficzny może wskazywać na
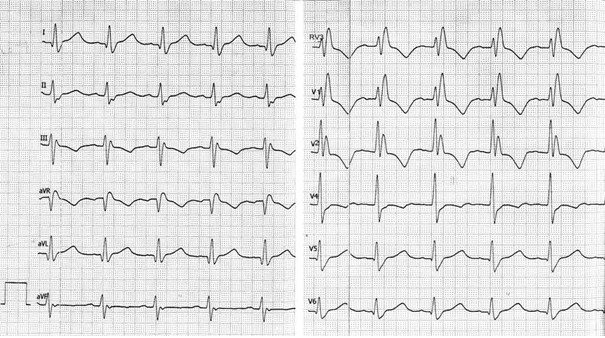
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
Na obrazie MR jamy brzusznej strzałką wskazano
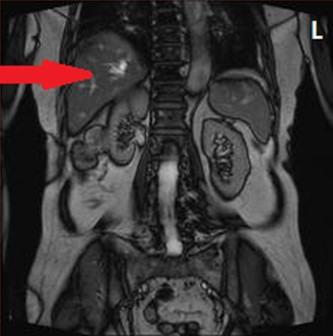
Który obraz MR mózgu został wykonany w sekwencji DWI?
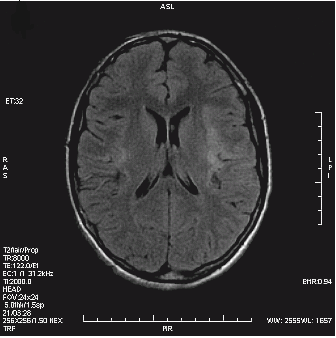
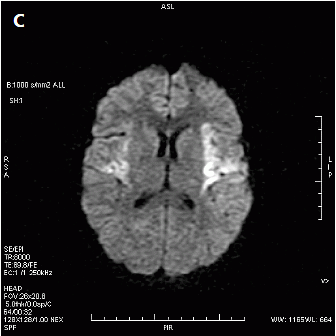
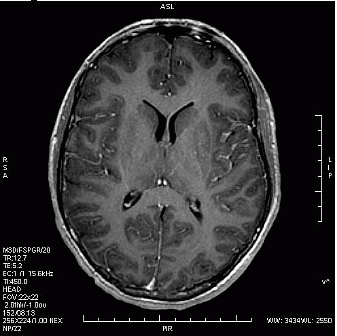
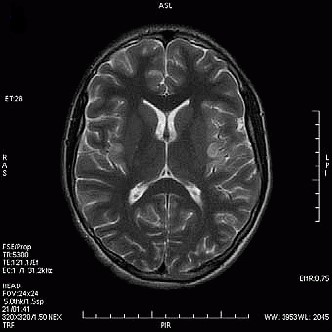
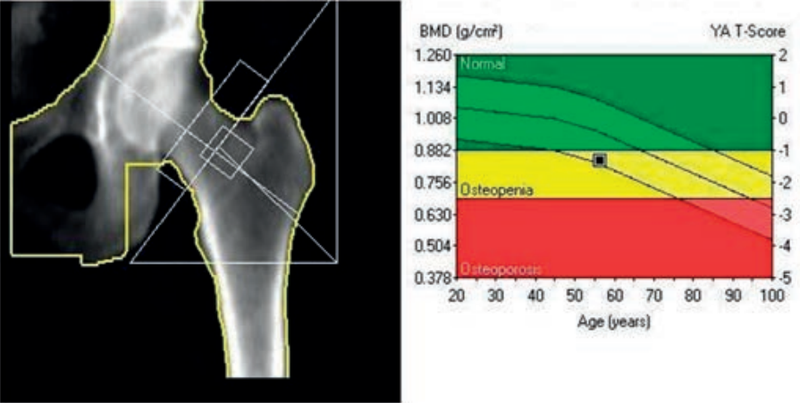
Badanie gęstości mineralnej kości metodą DXA należy wykonać
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji
W radiografii mianem SID określa się
Zwiększenie napięcia na lampie rentgenowskiej powoduje
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Artefakty zarejestrowane na elektrokardiogramie zostały wywołane przez
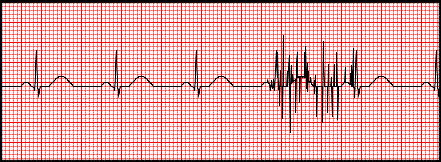
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
W ułożeniu do rentgenografii AP stawu kolanowego promień główny pada
Z kratką przeciwrozproszeniową należy wykonać zdjęcie
Celiakografia jest badaniem kontrastowym
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Którą kasetę należy wykorzystać do wykonania rentgenogramu klatki piersiowej w projekcji bocznej u 35-letniej pacjentki o wzroście 165 cm i wadze 54 kg?
Do środków kontrastujących negatywnych należą
W badaniu PET CT wykorzystuje się radioizotopy emitujące promieniowanie
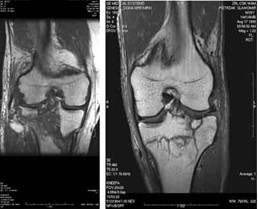
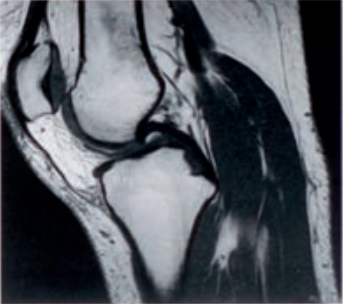
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
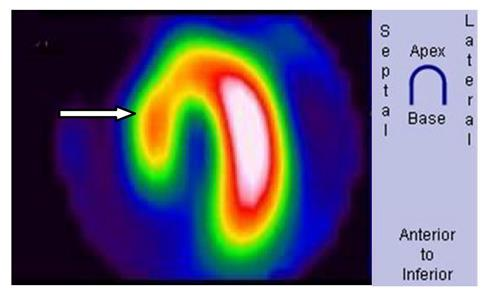
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę
W celu unieruchomienia okolicy badanej podczas wykonywania zdjęcia nadgarstka u osoby dorosłej należy zastosować
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
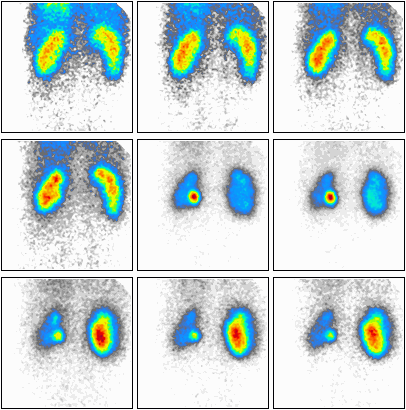
Podczas którego badania zostały zarejestrowane przedstawione obrazy?
Które urządzenia pomocnicze służą do unieruchomienia pacjenta do zabiegu radioterapii?
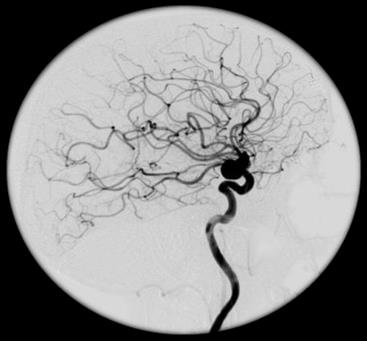
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
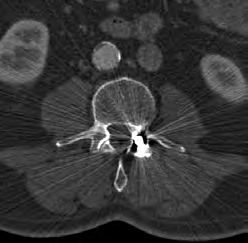
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

Zamieszczone obrazy związane są z badaniem
Badanie polegające na wprowadzeniu cewnika przez pęcherz moczowy do moczowodu i miedniczki nerkowej i podaniu środka kontrastującego to
Który artefakt jest widoczny na skanie tomografii komputerowej?
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
W scyntygrafii kośćca „ogniska gorące” oznaczają miejsca
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
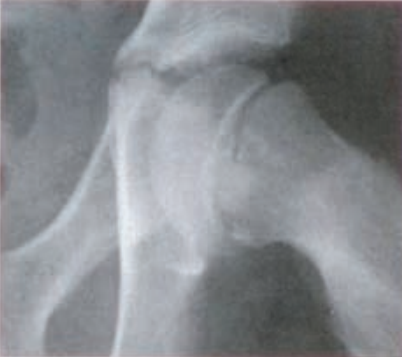
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
Który program wtórnej rekonstrukcji obrazów TK pozwala na odwzorowanie wnętrza jelita grubego, tchawicy i oskrzeli?
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?