Pytanie 1
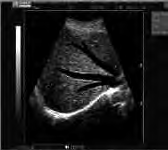
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
Wynik: 29/40 punktów (72,5%)
Wymagane minimum: 20 punktów (50%)
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono

W badaniu EKG punktem przyłożenia odprowadzenia przedsercowego C2 jest
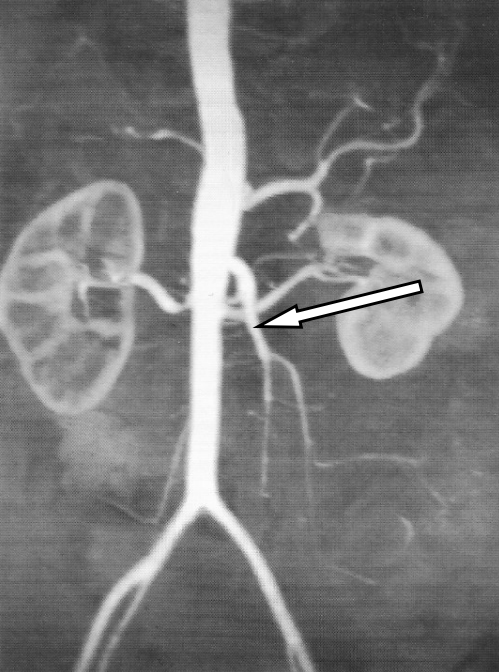
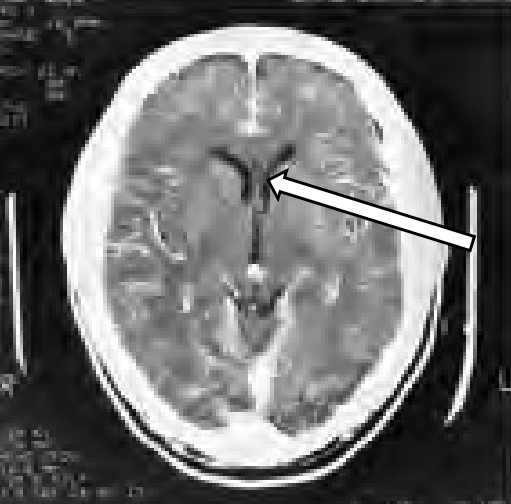
Którą tętnicę zaznaczono strzałką na obrazie MR?
Przy podejrzeniu ciała obcego w oczodole należy wykonać
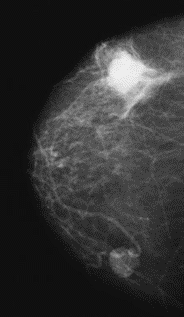
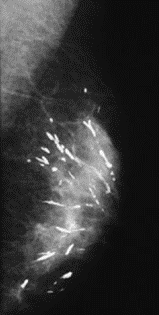
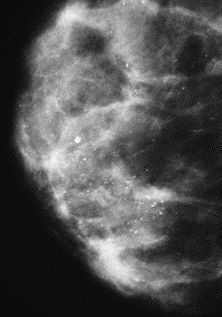
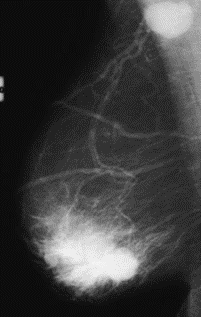
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?
Szczytowy przepływ wydechowy zarejestrowany w trakcie badania maksymalnie natężonego wydechu jest oznaczany skrótem
Do zdjęcia lewobocznego kręgosłupa lędźwiowo-krzyżowego pacjenta należy ułożyć na boku
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

Jaki kolor ma warstwa korowa kości w badaniu MR na obrazie T1- zależnym?
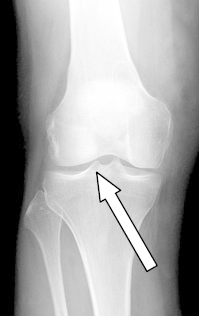
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
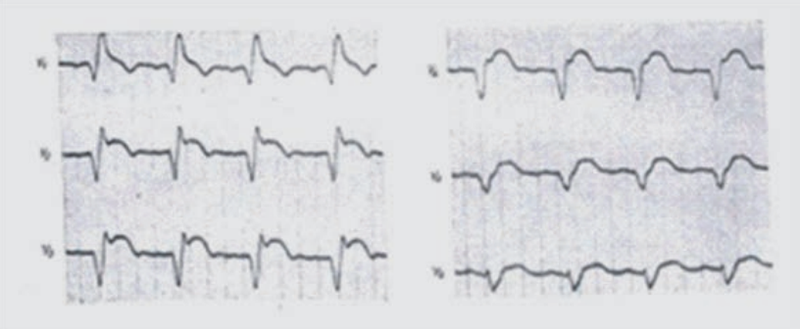
Na elektrokardiogramie zarejestrowano
Podstawowym elementem diagnostycznym aparatury izotopowej wykorzystującej emisyjne metody pomiaru jest
Jak oznacza się w systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej?
Przy ułożeniu do zdjęcia AP czaszki płaszczyzna
Lordoza to fizjologiczna krzywizna kręgosłupa występująca
Na scyntygramie tarczycy został uwidoczniony guzek
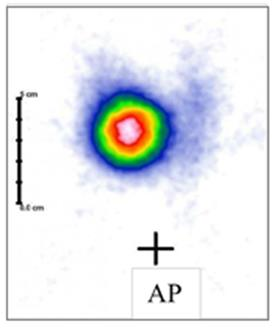
Standardowe badanie urografii polega na podaniu pacjentowi środka kontrastującego
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
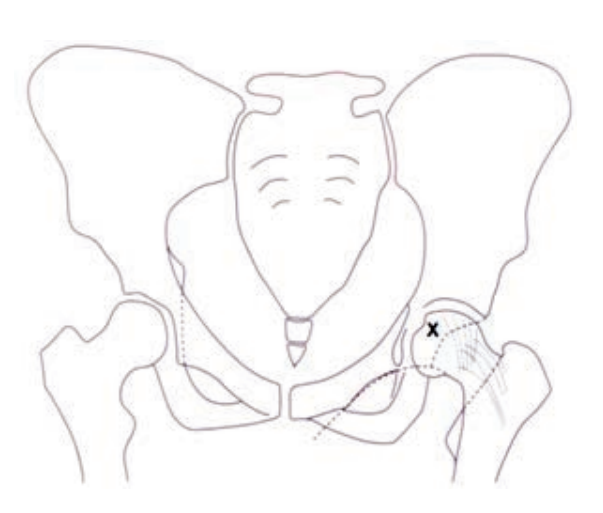
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
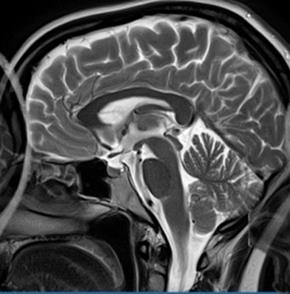
Teleradioterapia 4D na etapie planowania leczenia wykorzystuje obrazy
Którą strukturę anatomiczną zaznaczono strzałką na rentgenogramie?
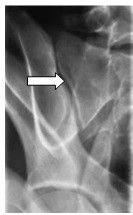
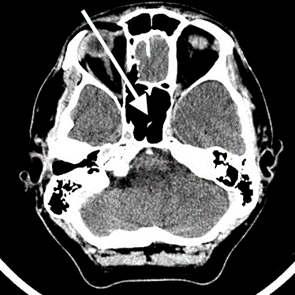
Na przedstawionym radiogramie TK głowy strzałką zaznaczono
W badaniu cystografii wstępującej środek kontrastowy należy podać
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
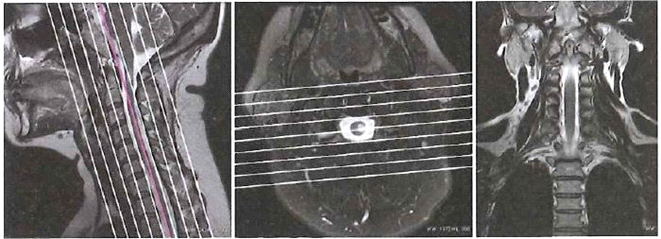
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
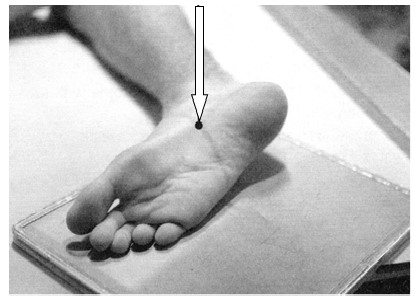
Na ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
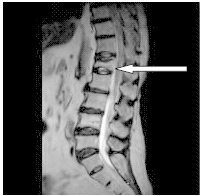
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg
Którą strukturę anatomiczną oznaczono na skanie TK głowy?
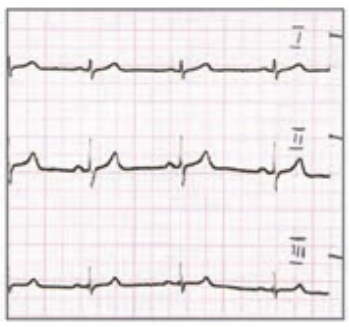
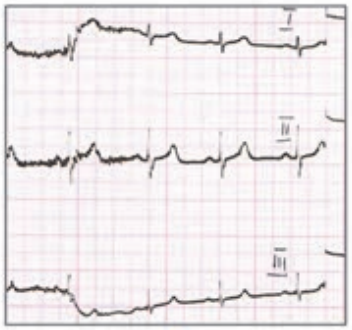
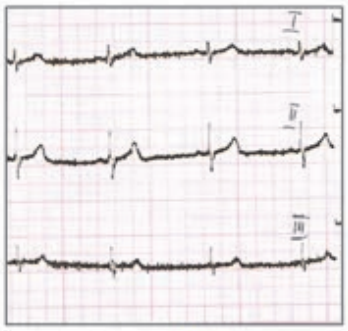
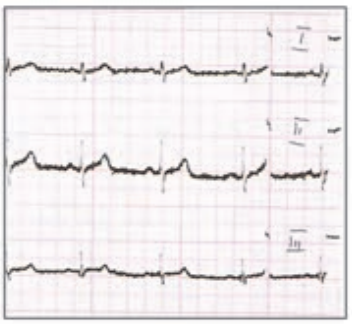
Który elektrokardiogram jest poprawny technicznie?
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
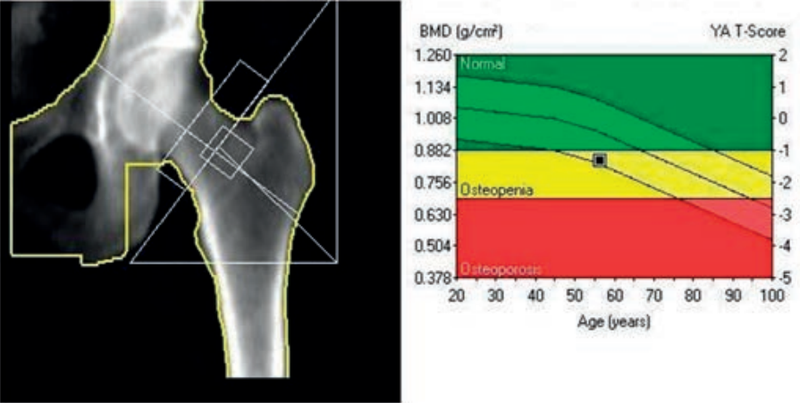
Zamieszczone obrazy związane są z badaniem
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Z kratką przeciwrozproszeniową należy wykonać zdjęcie
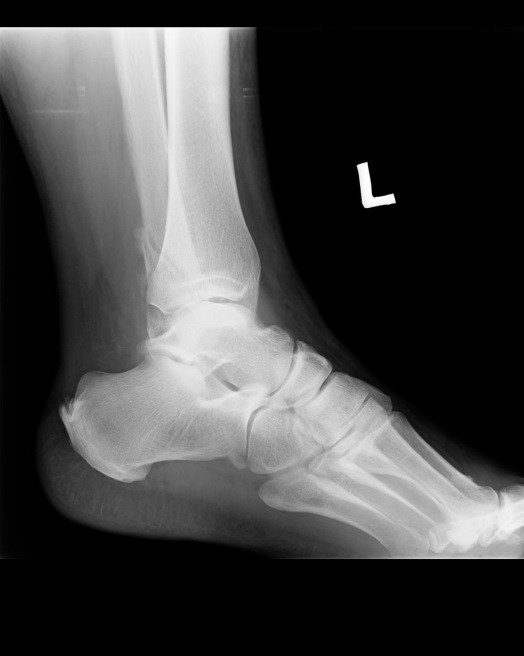
Na obrazie radiologicznym uwidoczniono złamanie kości
Rumień skóry pojawiający się podczas radioterapii jest objawem
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
Nieostrość geometryczna obrazu rentgenowskiego zależy od