Pytanie 1
Na ilustracji przedstawiono przygotowanie pacjenta do badania
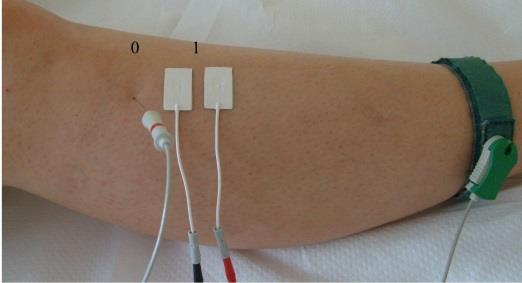
Wynik: 32/40 punktów (80,0%)
Wymagane minimum: 20 punktów (50%)
Na ilustracji przedstawiono przygotowanie pacjenta do badania

Na obrazie RM uwidoczniono odcinek kręgosłupa
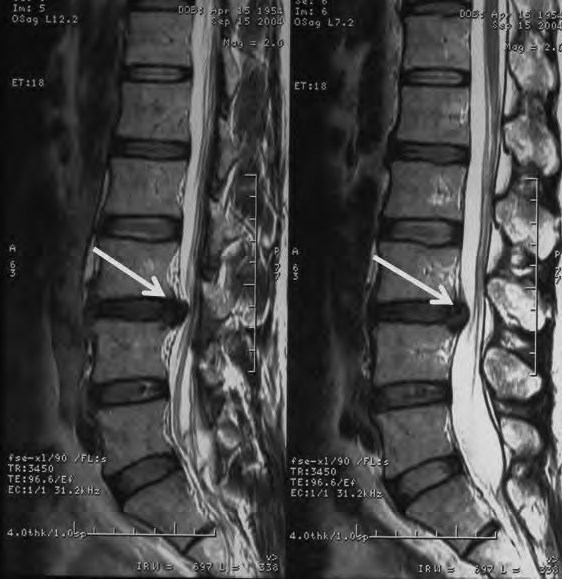
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
Audiogram przedstawia próbę
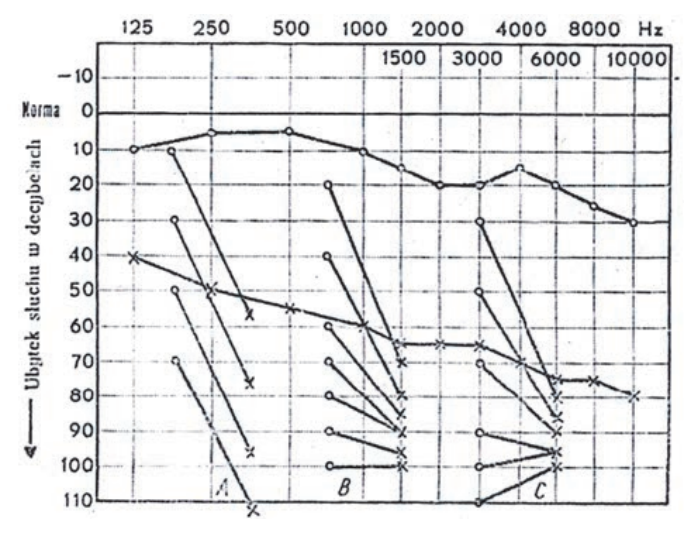
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
Na radiogramie uwidoczniono
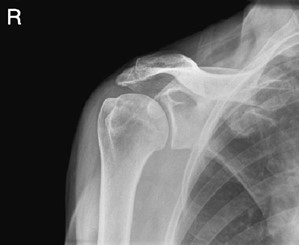
W systemie międzynarodowym ząb pierwszy przedtrzonowy po stronie lewej oznacza się symbolem
W jaki sposób należy oprzeć stroik w audiometrycznym badaniu przewodnictwa kostnego?
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
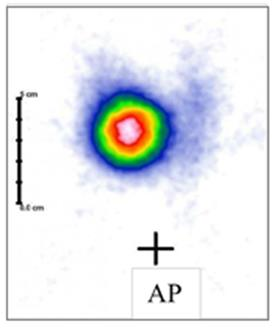
Na scyntygramie tarczycy został uwidoczniony guzek
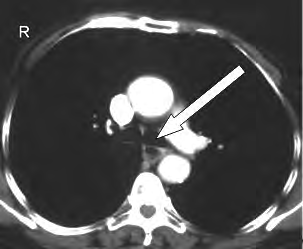
Na obrazie TK klatki piersiowej w przekroju poprzecznym strzałką oznaczono
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
W metodzie RM (rezonansu magnetycznego) po umieszczeniu pacjenta w silnym, stałym polu magnetycznym dochodzi do oddziaływania
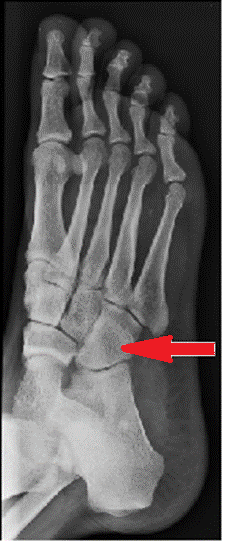
Na radiogramie stopy strzałką wskazano kość
Jaki sposób frakcjonowania dawki jest stosowany w radioterapii konwencjonalnej?
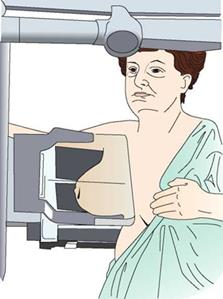
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
Który obszar napromieniania w radioterapii oznacza się skrótem PTV?
Zastosowana w badaniu radiologicznym kratka przeciwrozproszeniowa powoduje
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
W brachyterapii MDR stosowane są dawki promieniowania
Gdzie znajduje się węzeł zatokowo-przedsionkowy wywołujący rytmiczne skurcze mięśnia serca?
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Który radiofarmaceutyk należy podać pacjentowi w scyntygrafii perfuzyjnej mózgu?
Obiektywną metodą badania słuchu jest audiometria
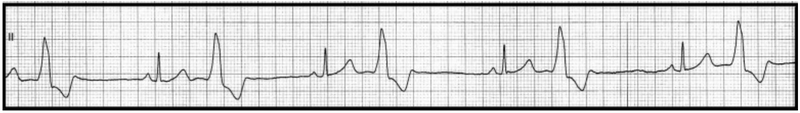
Który stan patologiczny został zarejestrowany podczas wykonywania badania EKG?
Radioizotopowa terapia medycyny nuklearnej polega na wprowadzeniu do tkanek lub narządów radiofarmaceutyku
Czym charakteryzuje się późny odczyn popromienny?
Jak konwencjonalnie frakcjonuje się dawkę w teleradioterapii?
Które znaczniki są wykorzystywane w scyntygrafii tarczycy?
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
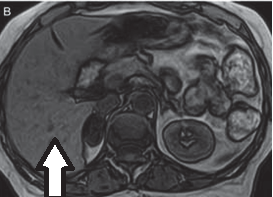
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
W scyntygrafii kośćca „ogniska gorące” oznaczają miejsca
Fala głosowa rozchodzi się