Pytanie 1
Jakie aspekty nie są objęte badaniami organoleptycznymi olejów rafinowanych?
Wynik: 0/40 punktów (0,0%)
Wymagane minimum: 20 punktów (50%)
Jakie aspekty nie są objęte badaniami organoleptycznymi olejów rafinowanych?
Lepkość dynamiczna wody
| Tabela. Gęstość (d) i lepkość dynamiczna wody (η) w danej temperaturze (T). | ||
| T [K] | d [g/cm3] | η [cP] |
| 293 | 0,99823 | 1,0050 |
| 298 | 0,99707 | 0,8937 |
| 303 | 0,99567 | 0,8007 |
| 308 | 0,99406 | 0,7225 |
| 313 | 0,99222 | 0,6560 |
| 318 | 0,99025 | 0,5988 |
| 323 | 0,98807 | 0,5494 |
| 328 | 0,98573 | 0,5064 |
| 333 | 0,98324 | 0,4688 |
Brak odpowiedzi na to pytanie.
Na rysunku pokazano efekt reakcji chemicznej, polegającej na dodaniu do badanego roztworu jonów żelaza (II) w obecności stężonego kwasu siarkowego(VI). Reakcja ta jest stosowana w celu wykrywania jonów

Brak odpowiedzi na to pytanie.
Z uwagi na niską zawartość żelaza w wodzie, najbardziej adekwatną metodą określania całkowitej ilości jonów żelaza(II) oraz (III) w próbkach wody pitnej jest
Brak odpowiedzi na to pytanie.
Ustalenie wartości miana roztworu wodorotlenku sodu na wodoroftalan potasu jest rekomendowane przez IUPAC, ponieważ wodoroftalan potasu jest substancją
Brak odpowiedzi na to pytanie.
W opisie metody analitycznej zapisano:
Który parametr metody analitycznej opisano?
| Różnica w otrzymanych wynikach dwóch oznaczeń wykonanych równocześnie lub w krótkim przedziale czasu na tej samej próbce, przez tego samego analityka, w takich samych warunkach, nie może przekraczać 1,5 g na 100 g oznaczanej próbki. |
Brak odpowiedzi na to pytanie.
Do zmiany objętości próbki roztworu NaOH wykorzystano 10,0 cm3 roztworu HCl o stężeniu 0,1000 mol/dm3. Jaką ilość NaOH (M = 40 g/mol) zawierała próbka?
Brak odpowiedzi na to pytanie.
W celu przeprowadzenia bezpośredniego testu ELISA należy postąpić zgodnie z procedurą

Brak odpowiedzi na to pytanie.
Zjawisko opisane w zamieszczonej informacji to
| Jeżeli w wodzie zostanie rozpuszczona α-D-glukopiranoza, to roztwór tuż po rozpuszczeniu wykazuje skręcalność właściwą [α]D = +112,2°, lecz w miarę upływu czasu skręcalność ta stopniowo spada do wartości charakterystycznej w stanie równowagi, mianowicie [α]D = +52,7° |
Brak odpowiedzi na to pytanie.
Ze względu na zmieniającą się podczas miareczkowania objętość badanego roztworu, należy obliczyć poprawkę p w przypadku miareczkowania
| p = Vpróbki + Vwody + Vtitrantu Vpróbki + Vwody |
Brak odpowiedzi na to pytanie.
Który rodzaj naczynka konduktometrycznego przedstawiono na rysunku?

Brak odpowiedzi na to pytanie.
Określenie punktu końcowego miareczkowania (PK) na podstawie analizy zmian przewodnictwa roztworu miareczkowanego w zależności od objętości wprowadzanego titranta jest podstawą miareczkowania?
Brak odpowiedzi na to pytanie.
Wyznaczanie punktu końcowego (PK) miareczkowania przy użyciu metod: graficznej, pierwszej pochodnej oraz Halina jest stosowane w
Brak odpowiedzi na to pytanie.
| Zawartość chlorowodoru w próbce można obliczyć wg wzoru: mB = CA · VA⁄1000 · pB⁄pA · MB w którym: mB – masa analizowanej substancji [g] CA – stężenie titranta [mol/dm3] VA – objętość titranta [cm3] pA i pB – współczynniki stechiometryczne reakcji, odpowiednio titranta i substancji oznaczanej MB – masa molowa substancji oznaczanej; 36,46 g/mol Do oznaczenia zużyto średnio 20,0 cm3 titranta, którego stężenie wynosiło 0,1000 mol/dm3. Obliczono masę próbki, która wyniosła 0,07292 g. |
| A. | HCl + NaOH → NaCl + H2O |
| B. | 3HCl + Al(OH)3 → AlCl3 + 3H2O |
| C. | 2HCl + Na2CO3 → 2NaCl + H2O + CO2 |
| D. | 2HCl + Na2B4O7 + 5H2O → 4H3BO3 + 2NaCl |
Brak odpowiedzi na to pytanie.
Wartości iloczynów rozpuszczalności związków srebra wynoszą odpowiednio: Osad której soli srebra wytrąci się jako pierwszy podczas dodawania jonów Ag+ do roztworu zawierającego jony I-, Br-, Cl- oraz CN-?
| Związek chemiczny | Iloczyn rozpuszczalności |
|---|---|
| AgCl | 1,8·10-10 |
| AgBr | 5,3·10-13 |
| AgCN | 1,4·10-16 |
| AgI | 8,3·10-17 |
Brak odpowiedzi na to pytanie.
Który zestaw sprzętu jest niezbędny do wykonania oznaczenia kwasowości wody?
| Procedura oznaczania kwasowości wody metodą miareczkowania wobec wskaźników. |
|---|
| Do kolby stożkowej odmierzyć 100 cm3 badanej wody, dodać 3 krople oranżu metylowego i miareczkować roztworem NaOH o stężeniu 0,05 mol/dm3 do pierwszej zmiany barwy z różowej na słomkowożółtą. Następnie dodać 10 kropli fenoloftaleiny i miareczkować roztworem NaOH do wyraźnie różowego zabarwienia utrzymującego się przez 3 minuty. |
Brak odpowiedzi na to pytanie.
Z analizy danych w tabeli rozpuszczalności wynika, że w formie osadu z roztworu wytrąci się
| Na+ | Fe2+ | Pb2+ | Mg2+ | Fe3+ | Ag+ | Zn2+ | |
|---|---|---|---|---|---|---|---|
| SO42- | ↓ | ↓ | |||||
| Br- | ↓ | ↓ | |||||
| Cl- | ↓ | ↓ | |||||
| S2- | ↓ | ↓ | ↓ | ↓ | ↓ | ↓ |
Brak odpowiedzi na to pytanie.
Elektroforeza to technika wykorzystywana głównie do segregacji mieszaniny
Brak odpowiedzi na to pytanie.
Do metod instrumentalnych w analizach jakościowych nie zaliczają się techniki
Brak odpowiedzi na to pytanie.
Część opisu skutków analizy
(...) generuje kation jednowartościowy, a sole powstałe z tym kationem to w przeważającej mierze substancje trudnorozpuszczalne. Większość jego soli jest bezbarwna. Ten bezbarwny jon ma zdolność do tworzenia jonów kompleksowych, na przykład z tiosiarczanem sodowym. Związki tego kationu są wrażliwe na światło (ciemnieją pod jego działaniem), dlatego powinny być przechowywane w pojemnikach z ciemnego szkła (...) Z opisu wynika, że w analizowanym surowcu jakościowo oznaczano kation
Brak odpowiedzi na to pytanie.
Czym jest efekt wspólnego jonu?
Brak odpowiedzi na to pytanie.
Podczas reakcji ksantoproteinowej obecność białka jest potwierdzana przez zmianę koloru na żółty, co wskazuje na obecność w białku
Brak odpowiedzi na to pytanie.
Dział analizy objętościowej, który dotyczy reakcji zobojętniania, to
Brak odpowiedzi na to pytanie.
Reakcja jonu Ag+ z substancją pełniącą rolę odczynnika grupowego, 4g+ + Cl- —> AgCl ↓, jest typowa dla kationów z grupy
Brak odpowiedzi na to pytanie.
Wykresy przedstawiają przebieg krzywych miareczkowania
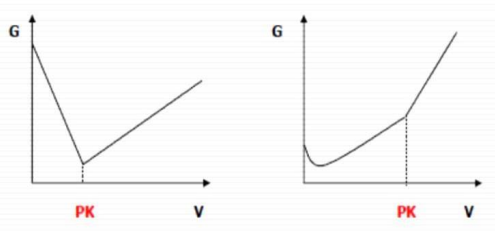
Brak odpowiedzi na to pytanie.
W próbce wody oznaczono zawartość rozpuszczonego tlenu metodą Winklera. Wyniki zestawiono w tabeli. Korzystając z zamieszczonego wzoru, określ zawartość rozpuszczonego tlenu (x) w badanej próbce wody.
$$ x = \frac{V_1 \cdot 0,2 \cdot 1000}{V_p} $$
\( x \) – zawartość tlenu rozpuszczonego; \( \text{mgO}_2/\text{dm}^3 \)
\( V_1 \) – objętość roztworu \( \text{Na}_2\text{S}_2\text{O}_3 \) o stężeniu \( 0,025 \, \text{mol}/\text{dm}^3 \) zużyta do miareczkowania; \( \text{cm}^3 \)
\( V_p \) – objętość próbki wody użytej do miareczkowania; \( \text{cm}^3 \)
\( 0,2 \) – ilość tlenu odpowiadająca \( 1 \, \text{cm}^3 \) roztworu \( \text{Na}_2\text{S}_2\text{O}_3 \) o stężeniu \( 0,025 \, \text{mol}/\text{dm}^3 \); \( \text{mg} \)
| Objętość próbki; \( V_p \) | Objętość roztworu \( \text{Na}_2\text{S}_2\text{O}_3 \) o stężeniu \( 0,025 \, \text{mol}/\text{dm}^3 \) zużyta do miareczkowania; \( V_1 \) |
| \( 100 \, \text{cm}^3 \) | \( 8,4 \, \text{cm}^3 \) |
Brak odpowiedzi na to pytanie.
Badaniom poddano wodę z akwarium przed napowietrzaniem i po napowietrzaniu. Wiadomo, że zawartość tlenu w wodzie powinna wzrosnąć o 20%. Który z wykresów obrazuje wyniki tych badań?
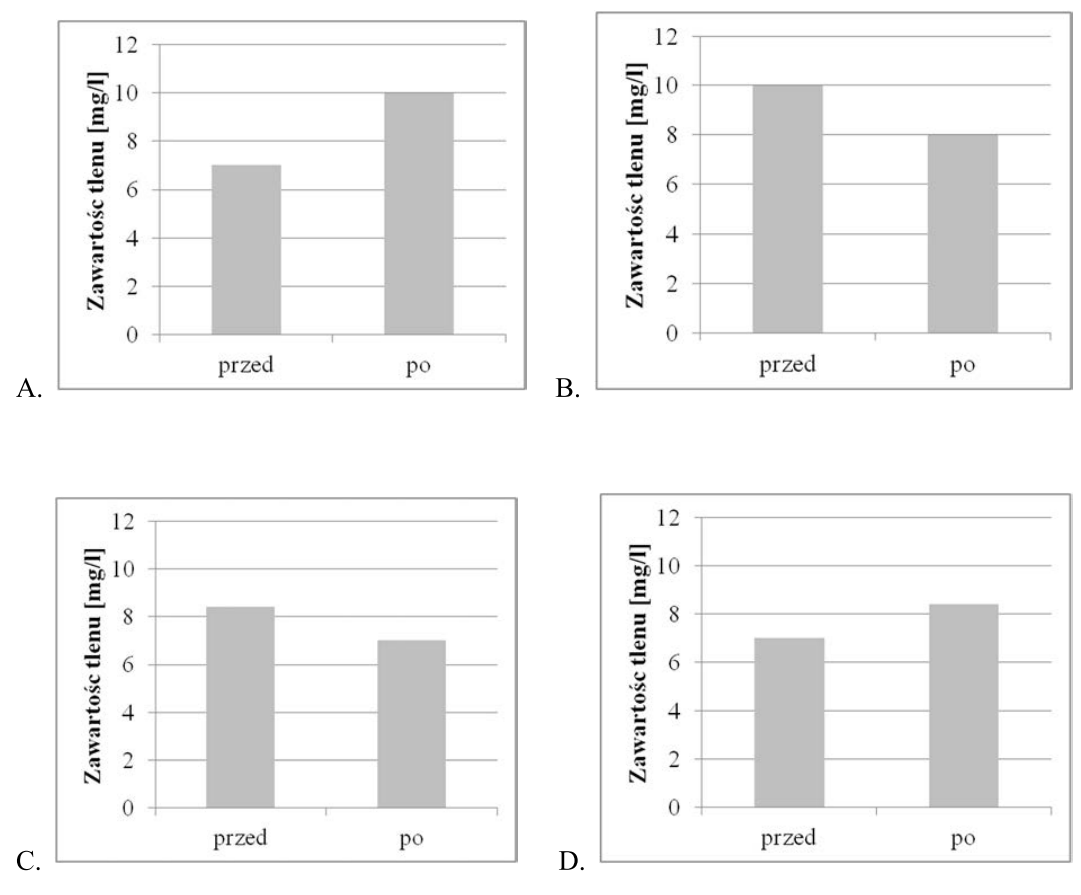
Brak odpowiedzi na to pytanie.
Znając zasadę działania polarymetru i wzór - można oznaczyć stężenie
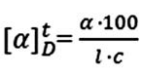
Brak odpowiedzi na to pytanie.
Korzystając z rysunków zamieszczonych w tabeli, wybierz zestaw sprzętu potrzebnego do oznaczania CO2 w wodach powierzchniowych metodą miareczkową.
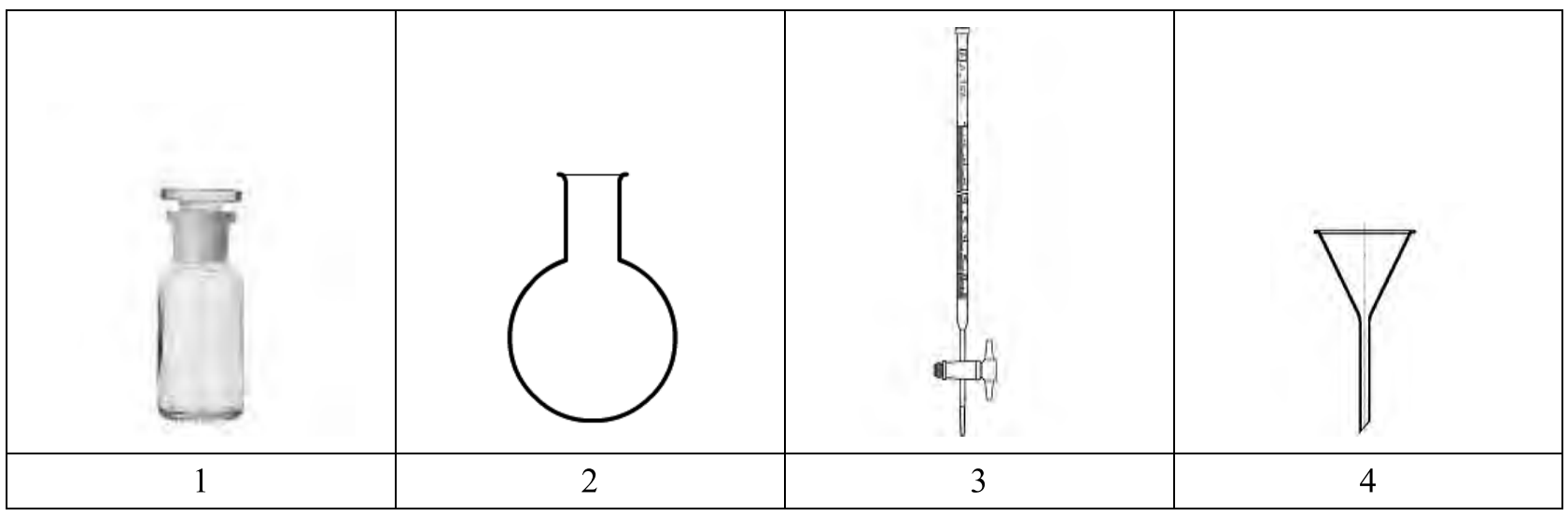
Brak odpowiedzi na to pytanie.
Do oceny kwasowości mleka wykorzystuje się metodę miareczkowania
Brak odpowiedzi na to pytanie.
Ile wynosi refrakcja molowa kwasu octowego o gęstości równej 1,0498 g/cm3, jeżeli współczynnik załamania światła wynosi 1,3874, a masa molowa kwasu octowego jest równa 60,054 g/mol?
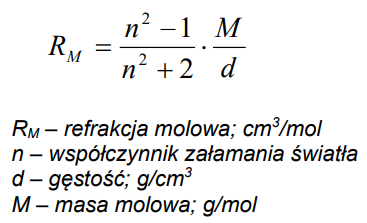
Brak odpowiedzi na to pytanie.
Z rysunku wynika, że analitem jest roztwór
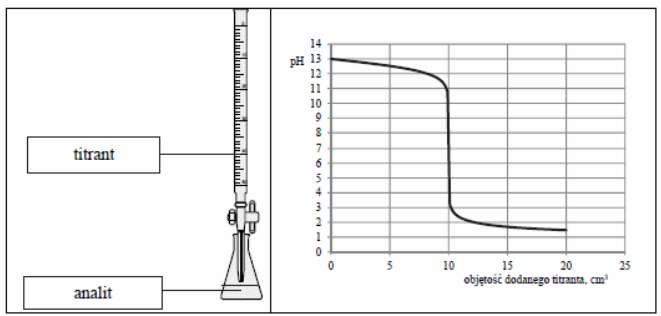
Brak odpowiedzi na to pytanie.
Który zestaw węglowodanów zalicza się do monosacharydów?
| mannoza | maltoza | mannoza | celuloza |
| glukoza | glukoza | glukoza | glukoza |
| sacharoza | fruktoza | fruktoza | ryboza |
| A | B | C | D |
Brak odpowiedzi na to pytanie.
Na schemacie przedstawiono bieg promieni światła w
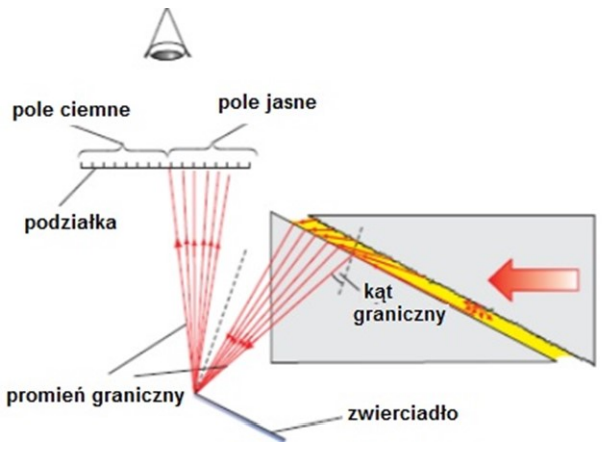
Brak odpowiedzi na to pytanie.
W temperaturze 20°C wyznaczono gęstość i współczynnik załamania światła kwasu butanowego. Wyniki zestawiono w tabeli. Refrakcja molowa kwasu butanowego wynosi
| Gęstość | Współczynnik załamania światła |
|---|---|
| 0,960 g/cm³ | 1,398 |
| RM = n2 - 1 n2 + 2 M d |
| RM – refrakcja molowa, cm3/mol n – współczynnik załamania światła d – gęstość, g/cm3 M – masa molowa, 88 g/mol |
Brak odpowiedzi na to pytanie.
Na rysunku przedstawione jest pole widzenia
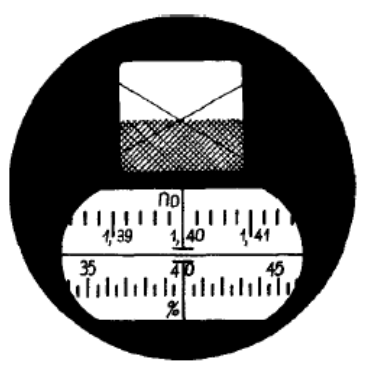
Brak odpowiedzi na to pytanie.
Wykonano identyfikację opisaną w schemacie:
BaCl2 + X — biały osadJaki wzór reprezentuje substrat X?
Brak odpowiedzi na to pytanie.
Do zmiareczkowania 30,0 cm3 roztworu HCl o stężeniu 0,1 mol/dm3 użyto KOH. Jaką masę KOH zawierała ta odważka?
MKOH = 56 g/mol
Brak odpowiedzi na to pytanie.
Wskaź zespół substancji, które przyczyniają się do twardości niewęglanowej wody?
Brak odpowiedzi na to pytanie.
Mangan ulega utlenieniu w reakcji
| A. | Mn2+ + 2OH− → Mn(OH)2 |
| B. | 2Mn(OH)2 + O2 → 2 MnO(OH)2 |
| C. | MnO(OH)2 + 4H+ → Mn4+ + 3H2O |
| D. | Mn4+ + 2I− → Mn2+ + I2 |
Brak odpowiedzi na to pytanie.