Pytanie 1
W których projekcjach wykonuje się standardowe badanie mammograficzne?
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
W których projekcjach wykonuje się standardowe badanie mammograficzne?
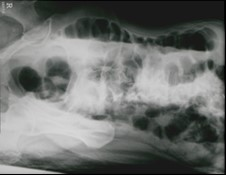
Przedstawiony obraz został zarejestrowany podczas wykonania
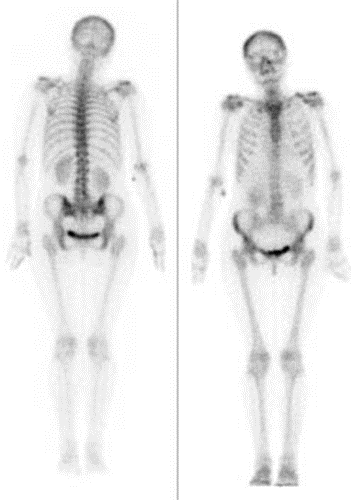
Celiakografia jest badaniem kontrastowym
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Z kratką przeciwrozproszeniową należy wykonać zdjęcie
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
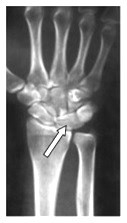
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
Obraz stawu kolanowego otrzymano metodą
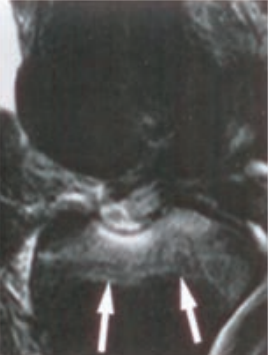
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
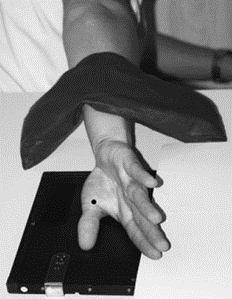
Na ilustracji przedstawiono ułożenie pacjenta do zdjęcia rentgenowskiego
Które badanie zostało zarejestrowane na przedstawionym radiogramie?
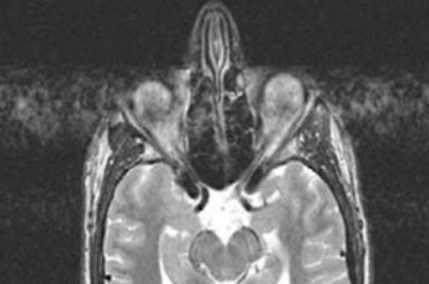
Co jest przyczyną artefaktu widocznego na obrazie MR?
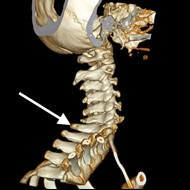
Na obrazie TK kręgosłupa strzałką wskazano wyrostek
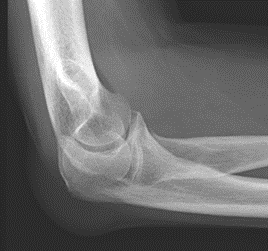
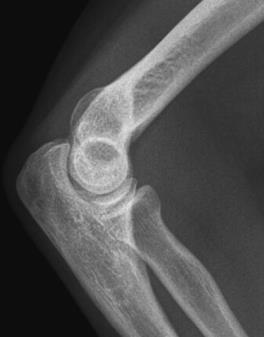
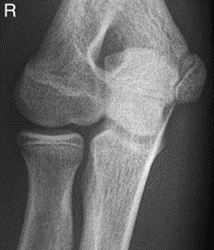
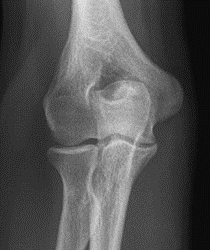
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
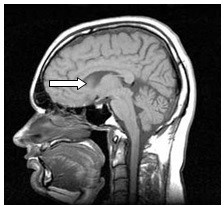
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
Technikę bramkowania oddechowego stosuje się w badaniu MR
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
Rozpoczęcie badania TK nerek po 20-30 sekundach od początku podania środka kontrastowego umożliwia diagnostykę
DSA to cyfrowa
Na obrazie TK nadgarstka uwidocznione jest złamanie kości
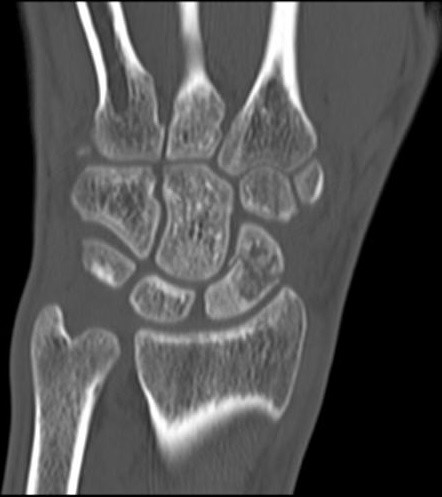
Ligand stosuje się
Testy specjalistyczne aparatów rentgenowskich do zdjęć wewnątrzustnych są przeprowadzane
Jak przebiega promień centralny w projekcji AP czaszki?
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
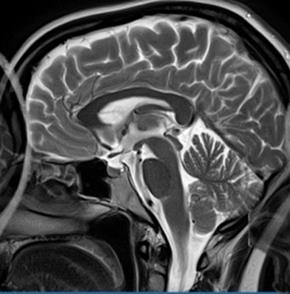
Na radiogramie uwidoczniono złamanie
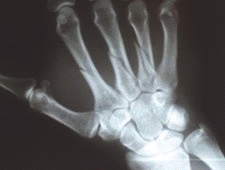
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Badanie metodą Dopplera umożliwia
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
Nieostrość geometryczna obrazu rentgenowskiego zależy od
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Które kolejne sekwencje badania kręgosłupa lędźwiowego uwidoczniono na przedstawionych obrazach?
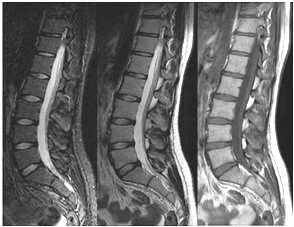
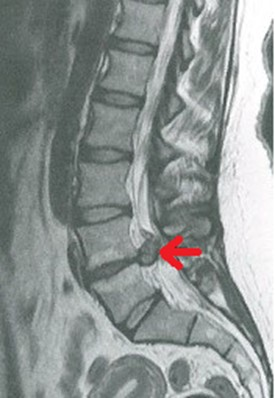
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
W radiologii stomatologicznej ząb o numerze 23 to kieł
Obrazowanie w sekwencjach STIR, FLAIR, SE wykonywane jest w badaniu
Promieniowanie rentgenowskie jest
Na obrazie uwidoczniono
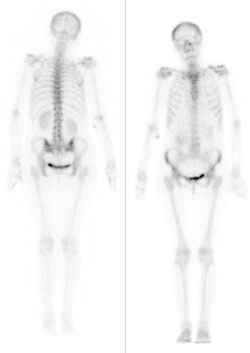
Przedstawiony obraz został zarejestrowany podczas wykonywania
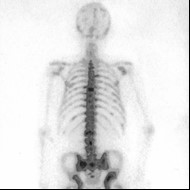
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji