Pytanie 1
Badanie polegające na wprowadzeniu cewnika przez pęcherz moczowy do moczowodu i miedniczki nerkowej i podaniu środka kontrastującego to
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Badanie polegające na wprowadzeniu cewnika przez pęcherz moczowy do moczowodu i miedniczki nerkowej i podaniu środka kontrastującego to
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
Obraz stawu kolanowego otrzymano metodą
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?
W zapisie EKG prawidłowego rytmu zatokowego wszystkie załamki P są
W lampie rentgenowskiej promieniowanie X powstaje w wyniku hamowania
Jaka jest standardowa odległość OF do wykonania rentgenowskich zdjęć kości i stawów kończyny górnej?
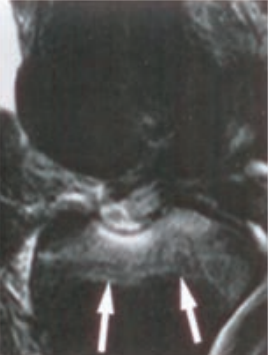
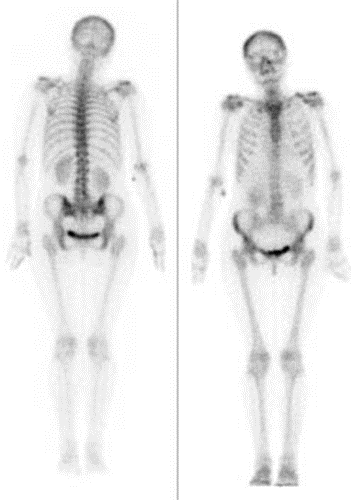
Na scyntygramie strzałką oznaczono
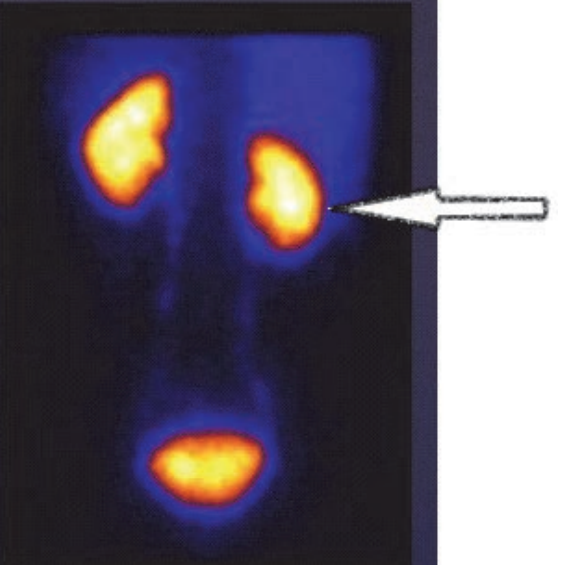
Na scyntygramie kości strzałkami oznaczono ogniska
Które obszary napromieniowania powinien określić lekarz radioterapeuta u pacjenta z nowotworem stercza po wcześniejszej prostatektomii?
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
Nieostrość geometryczna obrazu rentgenowskiego zależy od
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
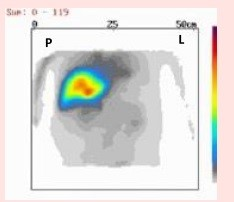
Który narząd został uwidoczniony na przedstawionym obrazie scyntygraficznym?
W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
W obrazowaniu MR wykorzystuje się moment magnetyczny
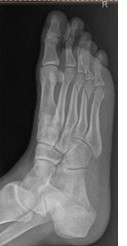
Na rentgenogramie stopy uwidocznione jest złamanie
Gadolin jako dożylny środek kontrastowy stosowany w MR powoduje
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

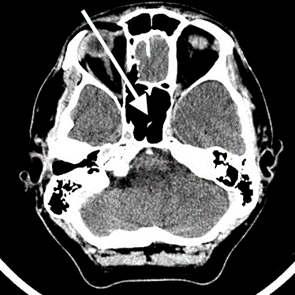
Na przedstawionym radiogramie TK głowy strzałką zaznaczono
W badaniu EKG elektrodę przedsercową V4 należy umocować
Przedstawiony obraz został zarejestrowany podczas wykonania
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem jest
Elementem systemu rejestracji obrazu, w którym fotony promieniowania X są bezpośrednio konwertowane na sygnał elektryczny, jest
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
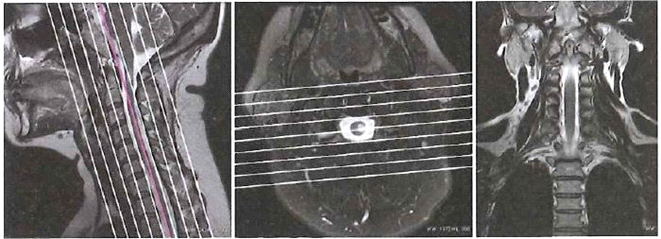
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
Na scyntygramie tarczycy uwidoczniono guzek
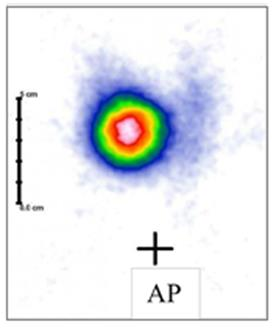
Planowany obszar napromieniania PTV obejmuje
Jakie są wielkości mocy dawki stosowanej w brachyterapii HDR?
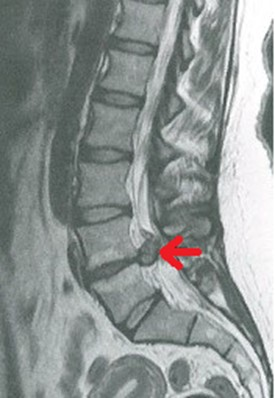
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
Obrazowanie w sekwencjach STIR, FLAIR, SE wykonywane jest w badaniu
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
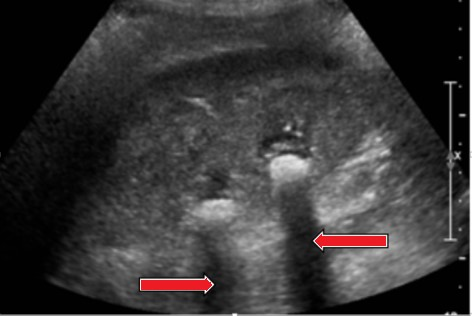
Który artefakt wskazano strzałkami na obrazie USG nerki?
Który środek ochrony radiologicznej pacjenta należy zastosować podczas wykonywania zdjęcia bocznego kręgosłupa szyjnego?
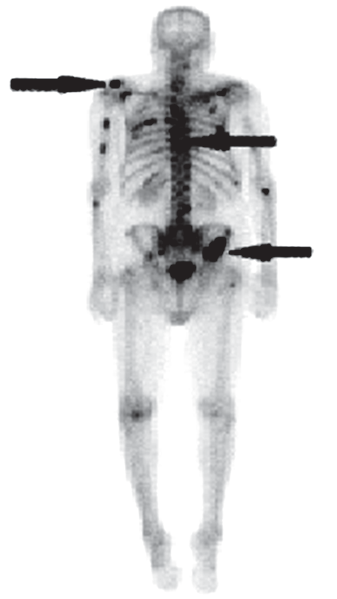
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki