Pytanie 1
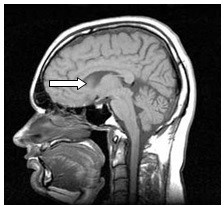
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
Wynik: 15/40 punktów (37,5%)
Wymagane minimum: 20 punktów (50%)
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to

Do pomiaru dawek indywidualnych u osób narażonych zawodowo na promieniowanie rentgenowskie są stosowane
Technika stereotaktyczna polega na napromienianiu nowotworu
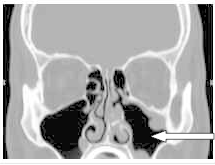
Na obrazie TK zaznaczono zatokę
Ultrasonograficzne środki kontrastowe to
Cholangiografia to badanie radiologiczne
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
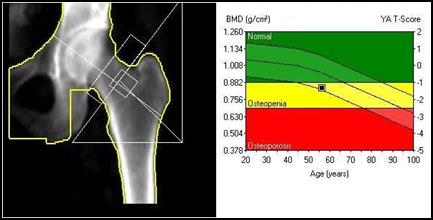
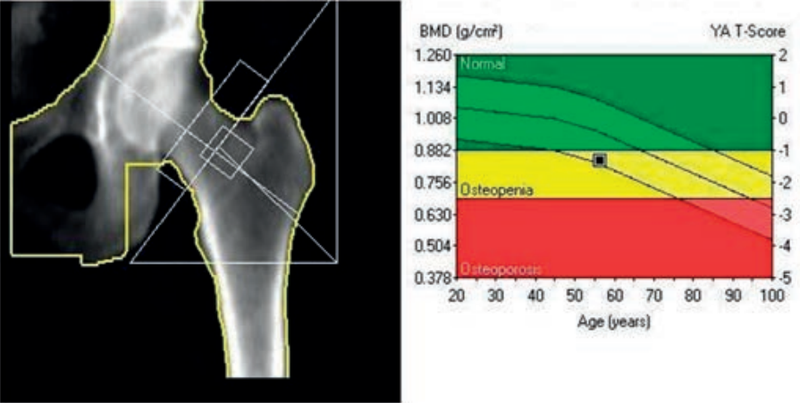
Która metoda diagnostyczna służy do określenia gęstości minerału kostnego w ujęciu objętościowym g/cm³?
Która składowa prawidłowej krzywej EKG odpowiada powolnej repolaryzacji komór mięśnia sercowego?
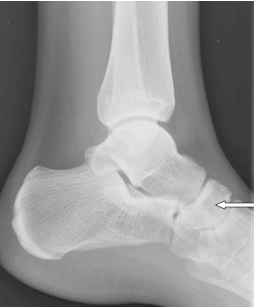
Na radiogramie strzałką oznaczono
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Który zestaw zdjęć narządów klatki piersiowej należy wykonać u pacjenta z podejrzeniem lewostronnego zapalenia płuc?
W ułożeniu do rentgenografii AP stawu kolanowego promień główny pada
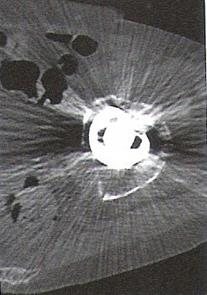
Zarejestrowany na obrazie TK artefakt jest spowodowany
Który radioizotop jest emiterem promieniowania alfa?
Zamieszczone na ilustracji obrazy dotyczą badania
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Wyniosłość międzykłykciowa znajduje się na nasadzie
Który załamek w zapisie EKG odpowiada zjawisku depolaryzacji przedsionków mięśnia sercowego?
Na radiogramie strzałką oznaczono
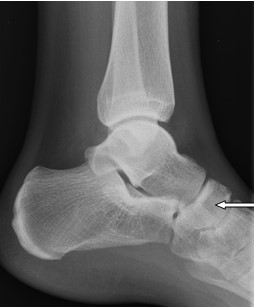
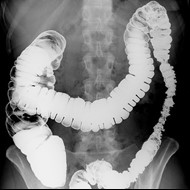
Przedstawiony obraz radiologiczny został zarejestrowany podczas badania jelita
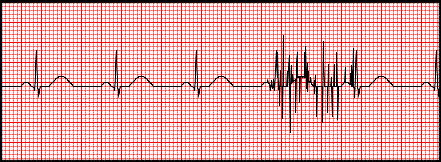
Artefakty zarejestrowane na elektrokardiogramie zostały wywołane przez
W scyntygrafii perfuzyjnej płuc pacjentowi podawany jest radioizotop
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
Objawem późnego odczynu popromiennego po teleradioterapii jest
Zamieszczone obrazy związane są z badaniem
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji
Zdjęcie rentgenowskie nadgarstka w przywiedzeniu dołokciowym jest wykonywane w celu uwidocznienia kości
Przy ułożeniu do zdjęcia AP czaszki płaszczyzna
Jak oznacza się w systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej?
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
Który radioizotop jest stosowany w diagnostyce i terapii raka tarczycy?
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
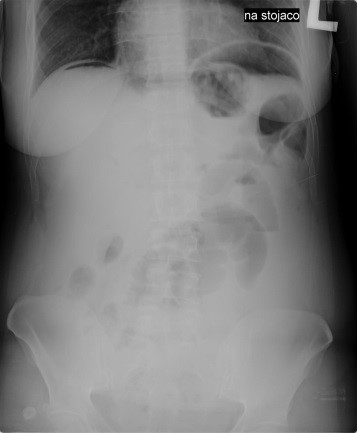
Radiogram jamy brzusznej uwidacznia
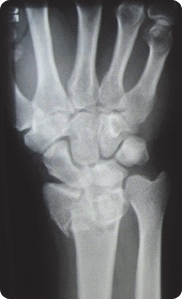
Na radiogramie uwidoczniono złamanie nasady
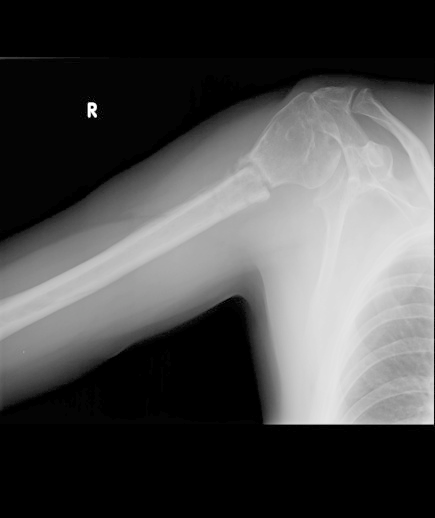
Na radiogramie uwidoczniono złamanie
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy