Pytanie 1
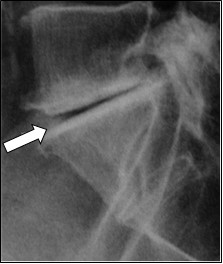
Na obrazie uwidoczniono złamanie kompresyjne kręgu
Wynik: 26/40 punktów (65,0%)
Wymagane minimum: 20 punktów (50%)
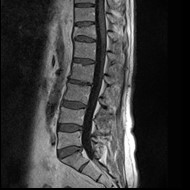
Na obrazie uwidoczniono złamanie kompresyjne kręgu

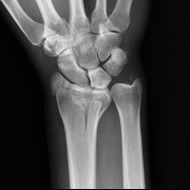
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
Zwiększenie napięcia na lampie rentgenowskiej powoduje
W której pozycji wykonuje się zdjęcie jamy brzusznej u pacjenta z podejrzeniem perforacji żołądka?
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Ligand stosuje się
Który z nowotworów jest hormonozależny?
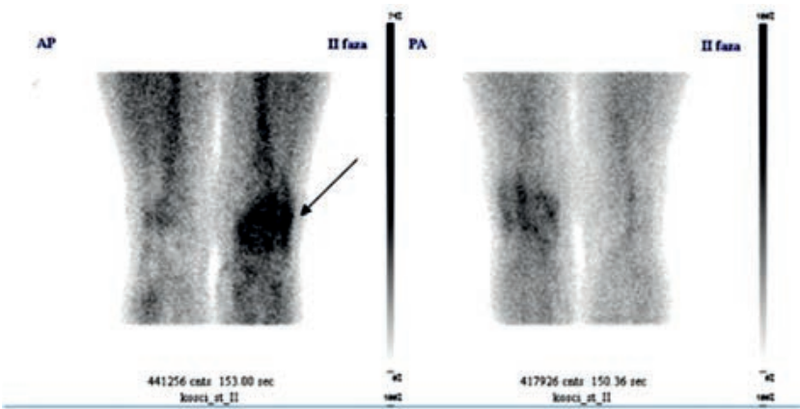
Na przedstawionym scyntygramie ukazano duży obszar
W pracowni radioterapii wyświetlenie na ekranie monitora aparatu komunikatu „ROTATION” oznacza prowadzoną terapię
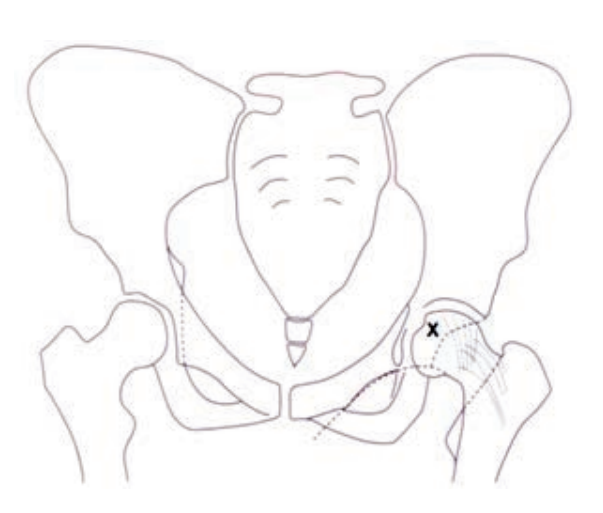
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
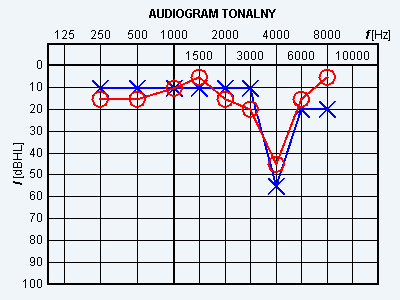
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
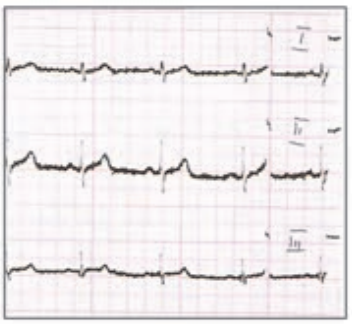
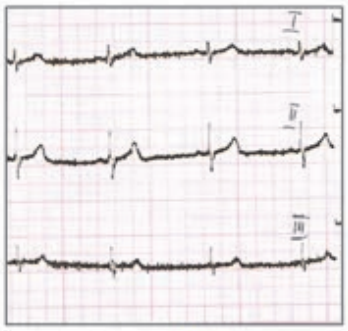
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Wskazaniem do wykonania badania spirometrycznego jest
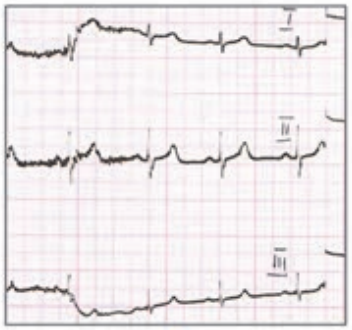
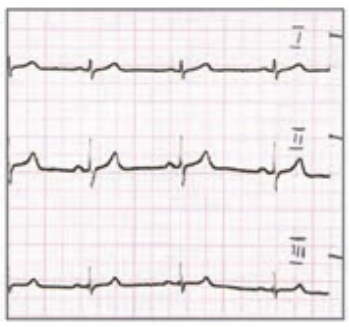
Który elektrokardiogram jest poprawny technicznie?
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
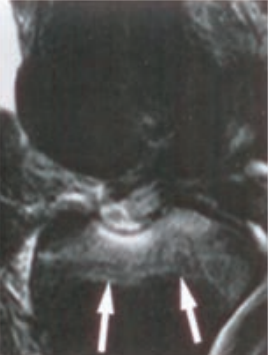
Obraz stawu kolanowego otrzymano metodą
Promieniowanie rentgenowskie jest
W pracowni ultrasonograficznej technik elektroradiolog nie korzysta z przepisów dotyczących
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?
Celiakografia jest badaniem kontrastowym
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Którym skrótem w badaniu spirometrycznym oznaczana jest pojemność życiowa płuc?
Teleradioterapia 4D na etapie planowania leczenia wykorzystuje obrazy
Rak drobnokomórkowy i rak niedrobnokomórkowy to postacie organiczne nowotworów złośliwych
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
W której projekcji należy wykonać badanie radiologiczne kręgosłupa lędźwiowego, by na otrzymanym zdjęciu wyrostki kręgów lędźwiowych układały się w charakterystyczny kształt piesków (teriera szkockiego)?
W radiografii mianem SID określa się
Objawem późnego odczynu popromiennego po teleradioterapii jest
Brachyterapia polega na napromieniowaniu pacjenta promieniowaniem
W celu unieruchomienia okolicy badanej podczas wykonywania zdjęcia nadgarstka u osoby dorosłej należy zastosować
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
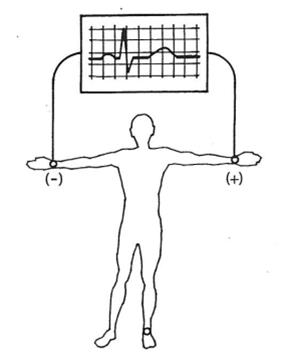
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
Hałas podczas badania tomografii rezonansu magnetycznego jest efektem ubocznym pracy
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
Brak odpowiedzi na to pytanie.
Na rentgenogramie strzałką zaznaczono