Pytanie 1
Reagenty o czystości na poziomie 99,999% — 99,9999% to reagenty
Wynik: 38/40 punktów (95,0%)
Wymagane minimum: 20 punktów (50%)
Reagenty o czystości na poziomie 99,999% — 99,9999% to reagenty
Materiały wykorzystywane w laboratoriach, mogące prowadzić do powstawania mieszanin wybuchowych, powinny być przechowywane
Do narzędzi pomiarowych zalicza się
Który z procesów jest endotermiczny?
W probówce połączono roztwory CuSO4 oraz NaOH. Powstał niebieski osad, który po podgrzaniu zmienił kolor na czarny. Czarnym osadem jest
W wyniku reakcji 20 g tlenku magnezu z wodą uzyskano 20 g wodorotlenku magnezu. Oblicz efektywność reakcji.
MMg = 24 g/mol, MO = 16 g/mol, MH = 1 g/mol?
Rozpuszczalnik stosowany w procesie krystalizacji powinien
Jakie procesy towarzyszy efekt egzotermiczny?
Jakie zestawienie sprzętu laboratoryjnego wykorzystuje się do filtracji osadów?
Próbka wzorcowa to próbka
W trzech probówkach umieszczono roztwory: wodorotlenku sodu, chlorku sodu i kwasu octowego. W celu identyfikacji zbadano ich odczyn za pomocą uniwersalnego papierka wskaźnikowego, a następnie fenoloftaleiny. Barwy wskaźników w badanych roztworach przedstawiono w tabeli:
| Wskaźnik | Barwa wskaźnika | ||
|---|---|---|---|
| próbówka nr 1 | próbówka nr 2 | próbówka nr 3 | |
| uniwersalny papierek wskaźnikowy | żółty | czerwony | niebieski |
| fenoloftaleina | bezbarwny | bezbarwny | malinowa |
W celu uzyskania 500 g mieszaniny oziębiającej o temperaturze -18oC należy zmieszać
| Tabela. Mieszaniny oziębiające | ||
|---|---|---|
| Temperatura mieszaniny [°C] | Skład mieszaniny | Stosunek masowy |
| -2 | Woda + chlorek amonu | 10 : 3 |
| -15 | Woda + rodanek amonu | 10 : 13 |
| -18 | Lód + chlorek amonu | 10 : 3 |
| -21 | Lód + chlorek sodu | 3 : 1 |
| -22 | Lód + chlorek amonu + azotan(V) amonu | 25 : 5 : 11 |
| -25 | Lód + azotan(V) amonu | 1 : 1 |
Jaką objętość w warunkach standardowych zajmie 1,7 g amoniaku (masa molowa amoniaku wynosi 17 g/mol)?
Transportuje się pobrane próbki wody do analiz fizykochemicznych
Skuteczny środek do osuszania
Rozpuszczalniki organiczne powinny być składowane
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Nie należy podgrzewać cieczy w szczelnie zamkniętych pojemnikach, ponieważ
W trakcie reakcji estryfikacji opisanej równaniem CH3COOH + C2H5OH ↔ CH3COOC2H5 + H2O użyto molowego stosunku alkoholu do kwasu wynoszącego 1:10. W rezultacie tego
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Aby odcedzić galaretowaty osad, konieczne jest użycie sączka
Reagent, który reaguje wyłącznie z jednym konkretnym jonem lub związkiem, nazywamy reagente
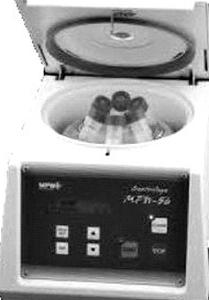
Na ilustracji zobrazowano urządzenie do
Na zdjęciu przedstawiono urządzenie służące do
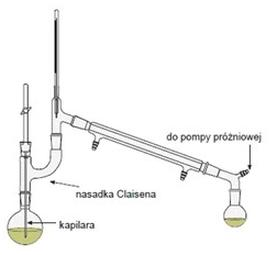
W trakcie destylacji cieczy wykorzystuje się tzw. kamienie wrzenne, ponieważ
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Ile gramów cukru trzeba dodać do 200 gramów wody o temperaturze 20°C, aby uzyskać roztwór nasycony?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Kalibracja pH-metru nie jest potrzebna po
Do systemu odprowadzania ścieków, w formie rozcieńczonego roztworu wodnego o maksymalnej masie 100 g na raz, można wprowadzić
Która część małej partii materiału jest najczęściej pobierana w celu przygotowania próbki ogólnej?
Przedstawiony na rysunku zestaw służy do destylacji
Sód metaliczny powinien być przechowywany w laboratorium
Jakie narzędzie w laboratorium jest wykorzystywane do rozdrabniania małych ilości substancji stałych?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na opakowaniu którego odczynnika powinien znaleźć się piktogram przedstawiony na ilustracji?
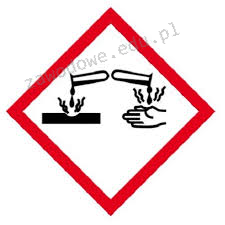
Naczynia miarowe, skalibrowane "na wlew" (IN) to:
Podczas pipetowania menisk górny określa się dla roztworów