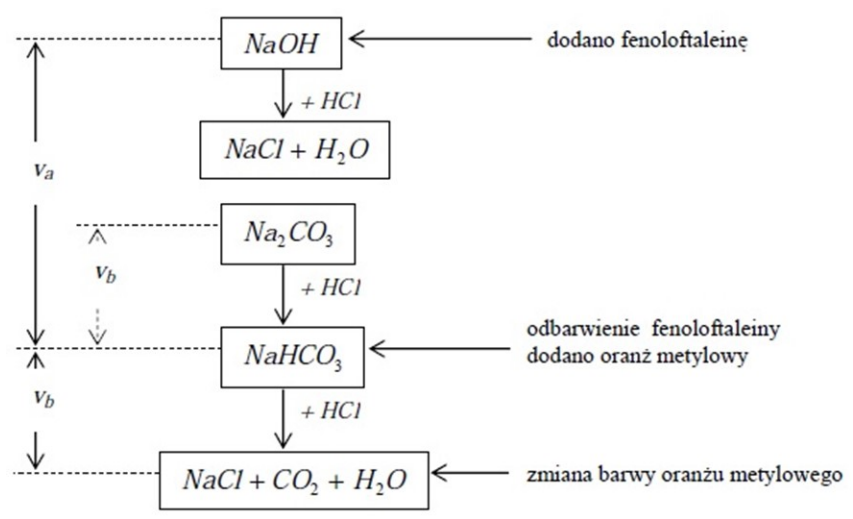
Odpowiedź jest poprawna, ponieważ wskazuje na dwa składniki, które mogą być użyte w procesie titracji. NaOH, jako silna zasada, reaguje z HCl, tworząc NaCl i wodę, co ilustruje pierwszy etap schematu. W dalszej kolejności Na2CO3 może reagować z HCl, przekształcając się najpierw w NaHCO3, a następnie w NaCl, CO2 i H2O. Reakcje te są zgodne z zasadami teorii kwasów i zasad oraz procesami analizy chemicznej. Fenoloftaleina, jako wskaźnik, zmienia kolor w obecności zasadowych roztworów, co jest kluczowe dla wizualizacji postępu titracji. W praktyce, takie analizy są stosowane w laboratoriach chemicznych, szczególnie w determinacji stężenia kwasów i zasad w różnych próbkach, co jest istotne w przemyśle farmaceutycznym, spożywczym oraz w badaniach środowiskowych.
Wybór innych składników, takich jak NaOH z NaCl, NaOH z HCl lub HCl z Na2CO3, nie odzwierciedla charakterystyki opisanej w schemacie procesu titracji. NaOH z NaCl nie stanowi odpowiedniej pary, ponieważ NaCl jest solą już powstałą w wyniku reakcji NaOH z HCl. Taki wybór wskazuje na brak zrozumienia, że NaCl nie może być ani reagentem, ani wskaźnikiem w kontekście titracji. W przypadku NaOH i HCl, chociaż oba te reagenty są używane w titracji, nie uwzględniają one drugiego etapu, w którym Na2CO3 musi być zaangażowany, co jest kluczowe dla pełnego zrozumienia procesów zachodzących w schemacie. Natomiast połączenie HCl z Na2CO3 jest błędne, gdyż nie bierze pod uwagę, że HCl jest już kwasem, który reaguje z zasadami. Tego rodzaju błędy często wynikają z niewłaściwego zrozumienia procesów chemicznych oraz roli, jaką różne związki chemiczne odgrywają w reakcjach. Aby poprawnie podejść do analizy, warto przestudiować mechanizmy reakcji chemicznych oraz zasady titracji, co jest kluczowe w naukach chemicznych oraz zastosowaniach przemysłowych.