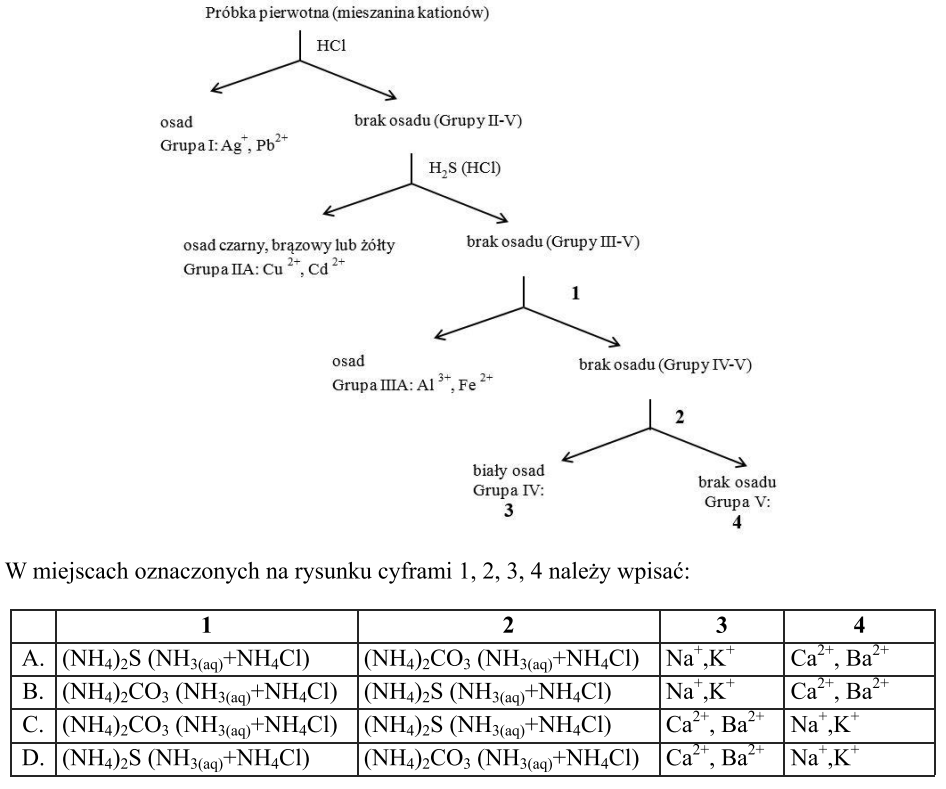
Odpowiedź D to strzał w dziesiątkę, bo świetnie opisuje, jak rozdzielamy te mieszaniny kationów. W punkcie 1 nie ma osadu dla grup III-V, co trochę pokazuje, że mamy do czynienia z jonami amonowymi (NH4)2CO3 oraz NH3(aq)+NH4Cl – no, to jest ważne w chemii analitycznej. W miejscu 2 też brak osadu dla grupy IV-V, a to znowu potwierdza obecność NH42CO3. To naprawdę ma swoją wagę w analizach chemicznych. Jeśli chodzi o miejsce 3, tam pojawia się biały osad, co z kolei sugeruje jony Na+ i K+ – typowe dla grupy IV. A w miejscu 4 znowu nie ma osadu, co mówi nam, że są tam kationy Ca2+ i Ba2+, które są kluczowe w chemii analitycznej. Wiadomo, rozdzielanie kationów to podstawa, bo pomaga nam w identyfikacji i pomiarze składników w różnych mieszaninach. Zrozumienie tego procesu jest mega ważne dla chemików w laboratoriach, gdzie dokładność odgrywa ogromną rolę w analizach jakościowych i ilościowych.
Wydaje mi się, że wybierając odpowiedzi A, B lub C, zrozumiałeś trochę inaczej, jak działa ten proces analizy chemicznej. Duży błąd polega na tym, że można było lepiej zrozumieć, jak jony reagują, kiedy mówimy o ich osadzaniu. Na przykład, w odpowiedzi A brak osadu w punkcie 1 oraz to, co jest w punkcie 2, pokazuje, że nie zauważyłeś roli kationów amonowych, co jest istotne dla grup III-V. A w odpowiedziach B i C pewnie poszło coś nie tak z interpretacją schematu, co doprowadziło do błędnych wniosków o tym, czy osady są obecne lub nie. Z moich obserwacji, często ludzie zbytnio upraszczają te procesy, nie biorąc pod uwagę, jak skomplikowane są te reakcje chemiczne i jak warunki wpływają na osadzanie. W chemii analitycznej detale naprawdę się liczą, bo różne kationy mogą mieć różne właściwości w zależności od pH czy temperatury. Znalezienie właściwego zrozumienia tego procesu jest kluczowe, żeby uzyskać rzetelne wyniki, co jest zgodne z najlepszymi praktykami w chemii.