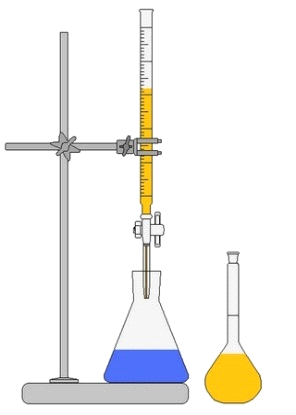
Zestaw pokazany na rysunku to klasyczne stanowisko do miareczkowania, czyli metody objętościowej analizy chemicznej. Kluczowym elementem jest biureta zamocowana na statywie, z kranikiem pozwalającym bardzo precyzyjnie dozować roztwór mianowany (titrujący). Pod biuretą stoi kolba stożkowa (Erlenmeyera), w której znajduje się roztwór badany z dodatkiem wskaźnika (stąd zwykle wyraźne zabarwienie). Obok widzimy kolbę miarową, w której typowo przygotowuje się roztwór o dokładnym stężeniu. Taki układ nie służy do ogrzewania ani rozdzielania mieszanin, tylko do bardzo dokładnego odmierzania objętości i obserwacji punktu końcowego reakcji. W analizie i kontroli jakości żywności miareczkowanie wykorzystuje się non stop: do oznaczania kwasowości miareczkowej w sokach i winach, zawartości soli kuchennej w peklówkach, liczby zmydlania i liczby kwasowej tłuszczów, zawartości wapnia czy magnezu w wodzie technologicznej. Moim zdaniem jest to jedna z podstawowych umiejętności laboratoryjnych w technikum – coś jak czytanie ze zrozumieniem w języku polskim. Dobre praktyki mówią, żeby zawsze: dokładnie przepłukać biuretę roztworem mianowanym, usunąć pęcherzyki powietrza spod kranika, ustawić poziom menisku na zerze na wysokości oczu, prowadzić miareczkowanie powoli w pobliżu punktu końcowego i cały czas mieszać zawartość kolby. W profesjonalnych laboratoriach kontrolnych każda seria miareczkowa jest dodatkowo weryfikowana próbką kontrolną i zapisem w dokumentacji zgodnie z zasadami GLP i systemami jakości typu ISO 17025. Wszystko po to, żeby wynik był wiarygodny i powtarzalny, a nie „na oko”.
Na rysunku widać układ z biuretą na statywie oraz kolbą stożkową pod nią, co jednoznacznie wskazuje na stanowisko do miareczkowania, a nie na aparaturę do innych operacji laboratoryjnych. Łatwo tu o skojarzenie z destylacją, bo w destylacji też mamy statyw, szkło i czasem kolby, ale w destylacji kluczowe są: kolba destylacyjna ogrzewana (np. na łaźni lub grzałce), chłodnica Liebiga lub inna chłodnica, odbieralnik oraz termometr do kontroli temperatury wrzenia. W destylacji zawsze występuje element kondensacji pary i układ chłodzący wodą – tego na rysunku w ogóle nie ma, nie ma też źródła ciepła ani połączeń szlifowych. To pokazuje, że nie chodzi o rozdzielanie składników na podstawie temperatury wrzenia. Z elektroforezą bywa podobny problem skojarzeniowy, bo uczniowie widzą barwne roztwory i myślą o rozdziale składników. Elektroforeza jednak wymaga zupełnie innego sprzętu: kuwety żelowe, zasilacz wysokiego napięcia, elektrody, ośrodki buforowe oraz najczęściej żel agarozowy lub poliakrylamidowy. Szkło laboratoryjne jak biureta czy kolba stożkowa nie jest typowym wyposażeniem stanowiska do elektroforezy, poza przygotowaniem buforów. Brak jakichkolwiek przewodów, elektrod i źródła napięcia jasno wskazuje, że to nie ta technika. Frakcjonowanie też może mylić, bo kojarzy się z podziałem na frakcje, ale w chemii laboratoryjnej frakcjonowanie zwykle oznacza albo destylację frakcyjną, albo rozdział zawiesin i roztworów przez sączenie, wirowanie czy ekstrakcję. W każdym z tych przypadków potrzebne są inne zestawy: kolumna frakcyjna, chłodnice, lejek sączkowy, wirówka itp. Tutaj mamy wyłącznie aparaturę do dokładnego odmierzania objętości roztworu i obserwacji zmiany barwy wskaźnika, co jest typową cechą miareczkowania w analizie wolumetrycznej. Z mojego doświadczenia typowy błąd myślowy polega na tym, że jeśli jest kolorowy roztwór i kilka elementów szkła, to uczniowie automatycznie myślą „jakaś zaawansowana separacja”. Tymczasem cały urok tego zestawu tkwi w prostocie: biureta, kolba stożkowa i roztwór mianowany służą nie do rozdzielania, tylko do bardzo dokładnego wyznaczania ilości substancji na podstawie reakcji chemicznej i zużytej objętości titranta. W realnym laboratorium kontroli jakości właśnie taki zestaw jest codziennym narzędziem pracy analityka.