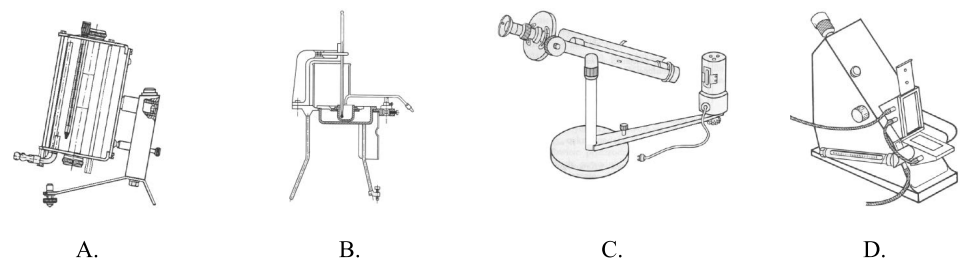
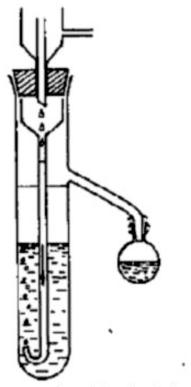
Który sprzęt laboratoryjny przedstawiono na ilustracji?


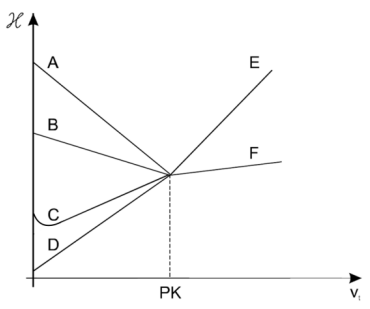
Cl2 + 2 I- → I2 + 2 Cl-Na podstawie podanych reakcji można stwierdzić, że w pierwszej kolejności woda chlorowa
I2 + 5 Cl2 + 6 H2O → 2 IO3- + 10 Cl- + 12 H+
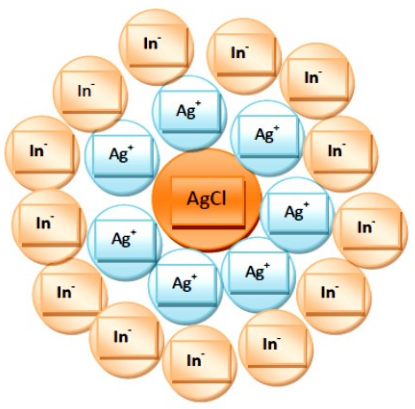
| Powierzchnię - suchą próbkę rozetrzeć w moździerzu, przesiać przez sito o średnicy oczek 1,25 mm i odważyć z niej 10 g w zlewce poj. 50 cm3. Do zlewki z próbką dodać 25 cm3 1-molowego roztworu KCl i energicznie mieszać, aż całość przejdzie w zawiesinę. Włączyć pH-metr, zanurzyć elektrody w zawiesinie i odczytać wartość na skali urządzenia. Pomiaru dokonać 3-krotnie, po każdym pomiarze przepłukując elektrody wodą destylowaną. Za wynik uznać średnią z trzech pomiarów obliczoną z dokładnością 0,05 pH. |
| Wskaźnik | Przedział pH |
| Błękit tymolowy | 1,2–2,8 |
| 8,0–9,6 | |
| Oranż metylowy | 3,1–4,4 |
| Czerwień metylowa | 4,2–6,2 |
| Błękit bromotymolowy | 6,7–7,6 |
| Fenoloftaleina | 8,0–9,8 |
| Tymoloftaleina | 9,3–10,5 |
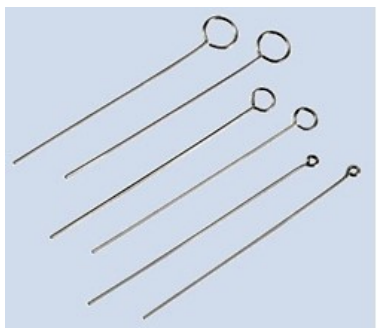
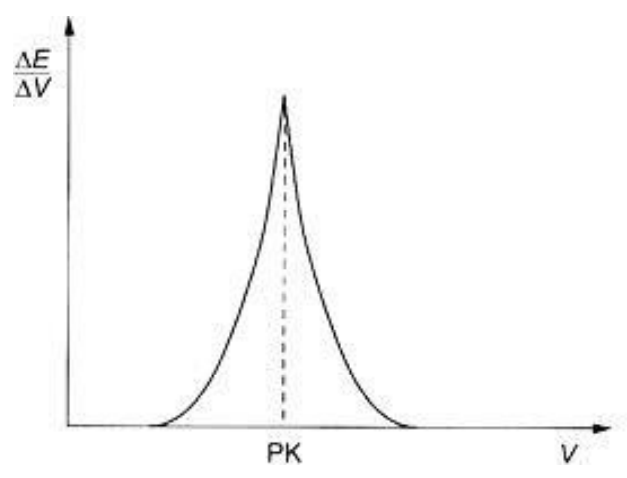
| Typ miareczkowania | Titrant | Wskaźnik | Barwa w PK miareczkowania | |
|---|---|---|---|---|
| A. | pośrednie | 0,5-molowy roztwór H2SO4 | czerwień metylowa z błękitem metylowym w etanolu | fioletowo-czerwona |
| B. | bezpośrednie | 0,5-molowy roztwór H2SO4 | czerwień metylowa z błękitem metylowym w etanolu | zielona |
| C. | pośrednie | 0,5-molowy roztwór NaOH | czerwień metylowa z błękitem metylowym w etanolu | fioletowo-czerwona |
| D. | bezpośrednie | 0,5-molowy roztwór NaOH | czerwień metylowa z błękitem metylowym w etanolu | fioletowo-czerwona |
| Odczynnik strącający | Reakcje analityczne | |||
|---|---|---|---|---|
| Ag+ | Hg22+ | Pb2+ | ||
| A. | HCl | biały osad AgCl rozpuszczalny w NH3·H2O | biały osad Hg2Cl2 | biały osad PbCl2 rozpuszczalny w gorącej wodzie |
| B. | H2SO4 | biały Ag2SO4 (ze stężonych roztworów), rozpuszczalny w gorącej wodzie | biały osad Hg2SO4 rozpuszczalny w wodzie królewskiej | biały osad PbSO4 rozpuszczalny w roztworze NaOH |
| C. | NaOH | brunatny osad Ag2O rozpuszczalny w NH3·H2O | czarny osad HgO i Hg | biały osad Pb(OH)2 rozpuszczalny w roztworze NaOH |
| D. | NH3aq | brunatny jon kompleksowy Ag(NH3)2+ | biały osad soli amidortęciowej rozpuszczalny w stężonym HNO3 | żółty osad Pb(OH)2 rozpuszczalny w gorącej wodzie |
| Gęstość | Współczynnik załamania światła |
|---|---|
| 0,960 g/cm³ | 1,398 |
| RM = n2 - 1 n2 + 2 M d |
| RM – refrakcja molowa, cm3/mol n – współczynnik załamania światła d – gęstość, g/cm3 M – masa molowa, 88 g/mol |
System HACCP – System Analizy Zagrożeń i Krytycznych Punktów Kontroli, stanowi zbiór wzajemnie powiązanych ze sobą procedur, które w całości tworzą system zarządzania bezpieczeństwem żywności.
| Odczynnik | Obserwacje |
|---|---|
| woda bromowa | odbarwienie wody bromowej |