Filtrowanie pytań
Wykonywanie badań analityczny…
A. czysta do badań.
B. produkt o charakterze technicznym.
C. czysta.
D. chemicznie czysta.
Wykonywanie badań analityczny…
W próbce wody pitnej o objętości 100 cm3 oznaczono zawartość azotanów 4 mg, chlorków 23 mg, manganu 0,006 mg i żelaza 0,01 mg. Korzystając z danych zawartych w tabeli, można stwierdzić, że badana woda
| Tabela. Wybrane parametry, jakim powinna odpowiadać woda do picia | ||
|---|---|---|
| Wskaźnik jakości wody | Jednostka | Najwyższe dopuszczalne stężenie lub zakres |
| Barwa | mgPt/l | 15 |
| Mętność | NTU | 1 |
| Zapach | - | akceptowalny |
| Odczyn | pH | 6,5 – 9,5 |
| Przewodność | μS/cm w 20°C | 2500 |
| Azotany | mg/l | 50 |
| Chlorki | mg/l | 250 |
| Chlor – wolny | mg/l | 0,1 – 0,3 |
| Mangan | mg/l | 0,05 |
| Twardość ogólna | mg CaCO₃/l | 60 - 500 |
| Twardość niewęglanowa | mval/l | - |
| Utlenialność | mgO₂/l | 5 |
| Żelazo | mg/l | 0,2 |
A. nie spełnia wymagań ze względu na zawartość manganu.
B. nie spełnia wymagań ze względu na zawartość azotanów.
C. nie spełnia wymagań ze względu na zawartość żelaza.
D. spełnia wymagania dla badanych parametrów.
Wykonywanie badań analityczny…
Podczas reakcji ksantoproteinowej obecność białka jest potwierdzana przez zmianę koloru na żółty, co wskazuje na obecność w białku
A. aminokwasów zawierających siarkę
B. wiązań peptydowych
C. wiązań wodorowych
D. aminokwasów zawierających pierścień aromatyczny
Wykonywanie badań analityczny…
Przedstawione reakcje zachodzą w produktach żywnościowych podczas fermentacji
| C12H22O11 + H2O → C6H12O6 + C6H12O6 |
| C6H12O6 → 2 CH3 −CH(OH) −COOH |
A. masłowej.
B. mlekowej.
C. alkoholowej.
D. octowej.
Wykonywanie badań analityczny…
BZT5 to umowny wskaźnik wskazujący na biochemiczne zapotrzebowanie na
A. potas
B. tlen
C. fosfor
D. azot
Wykonywanie badań analityczny…
Która z podanych metod pozwala na oznaczenie stężenia kwasu solnego (HCl)?
A. Spektrofotometria UV-Vis
B. Fluorymetria
C. Chromatografia HPLC
D. Miareczkowanie potencjometryczne
Wykonywanie badań analityczny…
W wodzie poddawanej procesowi dezynfekcji mierzy się zawartość chloru wolnego. Co oznacza ten parametr?
A. sumą stężenia ClO2-, ClO3-
B. stężeniem chloramin
C. sumą stężenia Cl2, HClO, ClO-
D. sumą stężenia chloramin oraz chloranów
Wykonywanie badań analityczny…
Określenie stężenia jonów Fe3+ w wodzie pitnej powinno być zrealizowane przy użyciu metody
A. chromatograficznej
B. absorpcjometrycznej
C. polarymetrycznej
D. refraktometrycznej
Wykonywanie badań analityczny…
W celu oceny jakości masła wykonano oznaczenie liczby kwasowej LK, liczby zmydlania LZ i liczby nadtlenkowej LOO. Wyniki zapisano w tabeli.
Wartość liczby estrowej LE w badanym maśle wynosi
| Liczba | Wartość zmierzona |
|---|---|
| LZ | 196,8 mg KOH/1g |
| LK | 1,2 mg KOH/1g |
| LE | ? |
| LOO | 4,25 milirównoważnika aktywnego tlenu/ kg |
A. 198,0 mg KOH/1g
B. 234,7 mg KOH/1g
C. 195,6 mg KOH/1g
D. 164,0 mg KOH/1g
Wykonywanie badań analityczny…
Do barwienia preparatów metodą Grama w badaniach mikrobiologicznych używa się płynu Lugola, który jest
A. roztworem jodku potasu w wodzie
B. wodnym roztworem jodu w jodku potasu
C. rozpuszczonym w alkoholu jodkiem potasu
D. rozpuszczonym w alkoholu jodem
Wykonywanie badań analityczny…
Która z przedstawionych na wykresie długości fali widma absorpcyjnego jonów MnO4- powinna być stosowana jako długość analityczna?
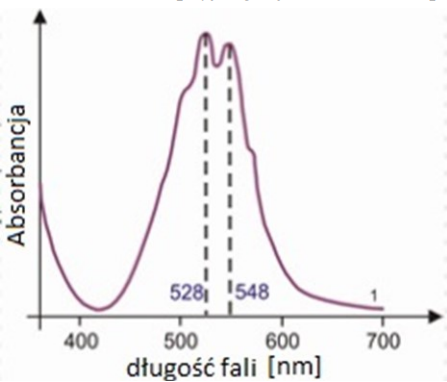
A. 700 nm
B. 548 nm
C. 420 nm
D. 528 nm
Wykonywanie badań analityczny…
W trakcie oznaczania ChZT wody, określanego jako utlenialność, substancją utleniającą jest
A. KMnO4
B. K2Cr2O7
C. H2O2
D. Cl2
Wykonywanie badań analityczny…
Określenie punktu końcowego miareczkowania (PK) na podstawie analizy zmian przewodnictwa roztworu miareczkowanego w zależności od objętości wprowadzanego titranta jest podstawą miareczkowania?
A. konduktometrycznego
B. spektrofotometrycznego
C. amperometrycznego
D. potencjometrycznego
Wykonywanie badań analityczny…
Związek chemiczny, który posiada skrót Gly-Ala-Leu-Ala-Tyr i został zidentyfikowany w trakcie badań analitycznych, to
A. pentapeptyd
B. tetrapeptyd
C. tripeptyd
D. dipeptyd
Wykonywanie badań analityczny…
Próbkę tłuszczu poddano analizie, której wyniki zapisano w tabeli. Która substancja była zawarta w próbce?
| Odczynnik | Obserwacje |
|---|---|
| woda bromowa | odbarwienie wody bromowej |
A. Masło.
B. Słonina.
C. Olej.
D. Smalec.
Wykonywanie badań analityczny…
Na podstawie informacji zamieszczonych w tabeli wskaż nazwę badanego związku.
| Dodany odczynnik | Obserwacje |
|---|---|
| Cu(OH)₂ | Zawiesina Cu(OH)₂ rozpuściła się, a roztwór przyjął szafirową barwę |
| Cu(OH)₂ | Po ogrzaniu probówki pojawił się ceglastoczerwony osad |
| [Ag(NH₃)₂]⁺ | Na ściankach probówki pojawiło się srebro metaliczne |
A. Glicerol.
B. Kwas metanowy.
C. Butanon.
D. Glukoza.
Wykonywanie badań analityczny…
W oznaczeniach kompleksonometrycznych dużej grupy kationów metali jako titrant stosowany jest związek chemiczny o ogólnym wzorze Na2H2Y. Przebieg oznaczenia przedstawia schematyczny zapis równania reakcji. Który z jonów metali nie jest oznaczany tą metodą?
| Me(H2O)xn+ + H2Y2- ↔ MeYn-4 + 2H3O+ + (x-2) H2O |
A. Zn2+
B. Ca2+
C. Al3+
D. Na+
Wykonywanie badań analityczny…
Badanie obecności pałeczek Salmonella w produktach spożywczych klasyfikuje się jako analiza
A. fizykochemicznych
B. mikrobiologicznych
C. fizycznych
D. chemicznych
Wykonywanie badań analityczny…
Na podstawie zamieszczonego fragmentu opisu wykonania ćwiczenia ustal, który wskaźnik jakości wody jest określany.
| Oznaczenie polega na określeniu ilości tlenu zużywanej do utleniania substancji organicznych w badanej próbce w ciągu n dób inkubacji w temperaturze 20°C. Ilość tę, w przeliczeniu na 1 dm³ wody, oblicza się jako różnicę zawartości tlenu przed i po inkubacji próbki. |
A. CHZT
B. Fosfor ogólny
C. BZT5
D. Azot azotanowy
Wykonywanie badań analityczny…
Jaką metodą dokonuje się oceny intensywności koloru karmelu?
A. jodometryczną
B. potencjometryczną
C. chromatografii bibułowej
D. spektrofotometryczną
Wykonywanie badań analityczny…
W zamieszczonej informacji przedstawiono równania reakcji zachodzące podczas oznaczania chlorków metodą
| Ag+ + Cl- → AgCl ↓ Ag+ + SCN- → AgSCN ↓ Fe3+ + SCN- → Fe(SCN)2+ |
A. strąceniową Mohra.
B. strąceniową Volharda.
C. grawimetryczną.
D. kompleksometryczną.
Wykonywanie badań analityczny…
Przeprowadzano analizę jakościową próbki według schematu:
Badana próbka zawierała kation
| badany roztwór zawierający jony X2+ | |
| + roztwór HCl | |
| XCl2↓ biały osad | |
| + H2O: ogrzać | |
| roztwór X2+: podzielić na 2 części | |
| + roztwór KI | oziębić |
| XI2 żółty osad | XCl2↓ biały osad |
A. Cd2+
B. Pb2+
C. Ag+
D. Hg2+
Wykonywanie badań analityczny…
Na rysunku przedstawiono schemat doświadczenia pozwalającego na zbadanie właściwości
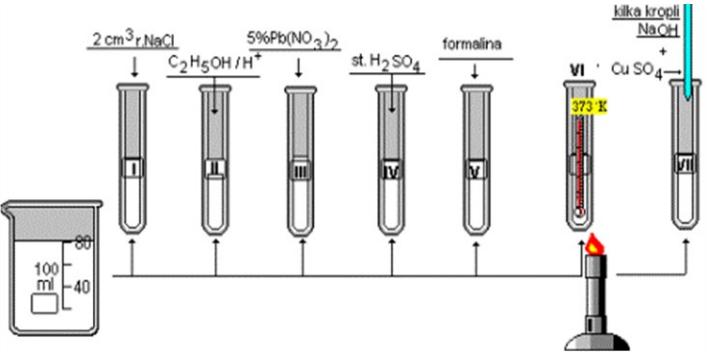
A. tłuszczów.
B. alkoholi.
C. cukrów.
D. białek.
Wykonywanie badań analityczny…
Reakcja: MnO4- + 8H+ + 5e- → Mn2+ + 4H2O jest wykorzystywana w metodzie analizy jakościowej, określanej jako
A. redoksometria
B. kompleksometria
C. alkalimetra
D. acydymetria
Wykonywanie badań analityczny…
Podczas miareczkowania kwasu octowego mianowanym roztworem wodorotlenku sodu należy użyć wskaźnika oznaczonego w tabeli literą
| Wskaźnik | Zakres pH zmiany barwy | |
|---|---|---|
| A. | Błękit tymolowy | 1,2-2,8 |
| B. | Oranż metylowy | 3,1-4,2 |
| C. | Czerwień metylowa | 4,2-6,3 |
| D. | Fenoloftaleina | 8,3-10,0 |
A. C.
B. B.
C. A.
D. D.
Wykonywanie badań analityczny…
Czym charakteryzuje się barwa roztworu zawierającego jony Cr2O72-?
A. pomarańczowa
B. zielona
C. żółta
D. niebieska
Wykonywanie badań analityczny…
W ramce przedstawiono równania reakcji zachodzące podczas oznaczania chlorków metodą
| Ag+ + Cl- → AgCl ↓ |
| Ag+ + SCN- → AgSCN ↓ |
| Fe3+ + SCN- → Fe(SCN)2+ |
A. grawimetryczną.
B. kompleksometryczną.
C. strąceniową Volharda.
D. strąceniową Mohra.
Wykonywanie badań analityczny…
Wykonano badanie, działając świeżo strąconym wodorotlenkiem miedzi(II) na wodny roztwór badanej próbki. Obserwacje zamieszczono w tabeli. Z obserwacji zawartych w tabeli wynika, że badaniu poddano
| Odczynnik | Obserwacje |
|---|---|
| Cu(OH)2 na gorąco | ceglastoczerwony osad |
| Cu(OH)2 na zimno | klarowny, szafirowy roztwór |
A. glukozę.
B. glicerol.
C. etanol.
D. etanal.
Wykonywanie badań analityczny…
Jakie kationy wchodzą w skład II grupy analitycznej?
A. Sn2+, Hg2+, Ag+
B. Cd2+, Sn2+, Al3+
C. Zn2+, Cu2+, Cd2+
D. Cu2+, Cd2+, Hg2+
Wykonywanie badań analityczny…
Ile wynosi mnożnik analityczny żelaza oznaczanego wagowo w postaci Fe2O3?
| MFe = 55,845 g/mol | MFe2O3 = 159,687 g/mol |
A. 1,4297
B. 2,8595
C. 0,3491
D. 0,6994
Wykonywanie badań analityczny…
Na etykiecie odczynnika chemicznego zawarte są następujące informacje. Z informacji wynika, że odczynnik ten może być zastosowany do sporządzenia roztworu o stężeniu około 0,1 mol/dm3 z dokładnością do
| NH4SCN amonu tiocyjanian | 0,1 mol/l |
| Stężenie po rozcieńczeniu do 1000 ml w 20°C | 0,1 mol/l ± 0,2 % |
A. 0,0002 mol/dm3
B. 0,2 mol/dm3
C. 0,002 mol/dm3
D. 0,02 mol/dm3
Wykonywanie badań analityczny…
Na podstawie danych w tabeli określ, który odczynnik należy dobrać, aby wykryć fenyloalaninę metodą chromatografii bibułowej i cienkowarstwowej.
| Substancje wykrywane | Odczynnik | Skład | Efekt barwny |
|---|---|---|---|
| Kwasy karboksylowe | Zieleń bromokrezolowa | 3% roztwór w metanolu z dodatkiem NaOH | Żółte plamy na zielonym tle |
| Aminokwasy | Ninhydryna | 1-2% roztwór w acetonie | Ogrzanie do temp. 110°C charakterystyczne zabarwienie |
| Lipidy | Błękit bromotymolowy | 0,04% roztwór w NaOH o stęż. 0,01 mol/dm3 | Żółte plamy na zielonym tle |
| Barbiturany | Azotan(V) rtęci(II) | 1% roztwór wodny | Czarne lub białe plamy na szarym tle |
A. Błękit bromotymolowy.
B. Ninhydryna.
C. Azotan(V) rtęci(II).
D. Zieleń bromokrezolowa.
Wykonywanie badań analityczny…
W trakcie analizy przeprowadzonej metodą fotometrii płomieniowej próbkę nawozu o wadze 0,1000 g rozpuszczono w 250 cm3 wody destylowanej. Po wykonaniu badań uzyskano zawartość potasu równą 0,0830 mg/cm3. Jaką wartość procentową K2O ma badany nawóz i czy mieści się ona w normie, jeśli współczynnik przeliczeniowy K na K2O wynosi 1,205, a zawartość procentowa K2O w nawozie powinna być w zakresie 40-50%?
A. 45% i jest zgodna z normą
B. 40% i jest zgodna z normą
C. 2,5% i nie jest zgodna z normą
D. 25% i nie jest zgodna z normą
Wykonywanie badań analityczny…
Prawidłowy przebieg reakcji redukcji jonu MnO4- w środowisku kwaśnym przedstawia równanie
| A. | MnO4- + H+ + e- → MnO42- + H+ |
| B. | MnO4- + 8H+ + 5e- → Mn2+ + 4H2O |
| C. | MnO4- + 4H+ + 3e- → MnO2 + 2H2O |
| D. | 2MnO4- + 10H+ + 8e- → Mn2O3 + 5H2O |
A. D.
B. A.
C. B.
D. C.
Wykonywanie badań analityczny…
Podczas elektrolizy wodnego roztworu kwasu solnego na katodzie zachodzi reakcja opisana równaniem
| A. | 2 H2O + 2e− → H2 + 2 OH− |
| B. | 2 H2O + 4e− → 4H+ + O2 |
| C. | 2 Cl− → Cl2 + 2e− |
| D. | 2 H+ + 2e− → H2 |
A. D.
B. B.
C. C.
D. A.
Wykonywanie badań analityczny…
Równanie przedstawia reakcję zachodzącą podczas oznaczania żelaza metodą miareczkowania
| 5Fe2+ + MnO4- + 8H+ ⇆ 5Fe3+ + Mn2+ + 4H2O |
A. redoksymetrycznego, gdzie wskaźnikiem jest roztwór skrobi.
B. redoksymetrycznego, gdzie wskaźnikiem jest fenoloftaleina.
C. redoksymetrycznego, gdzie wskaźnikiem jest titrant.
D. alkacymetrycznego, gdzie wskaźnikiem jest titrant.
Wykonywanie badań analityczny…
Wartości iloczynów rozpuszczalności związków srebra wynoszą odpowiednio: Osad której soli srebra wytrąci się jako pierwszy podczas dodawania jonów Ag+ do roztworu zawierającego jony I-, Br-, Cl- oraz CN-?
| Związek chemiczny | Iloczyn rozpuszczalności |
|---|---|
| AgCl | 1,8·10-10 |
| AgBr | 5,3·10-13 |
| AgCN | 1,4·10-16 |
| AgI | 8,3·10-17 |
A. Chlorku.
B. Bromku.
C. Cyjanku.
D. Jodku.
Wykonywanie badań analityczny…
Roztwór zawierający aniony I grupy analitycznej poddano identyfikacji metodą chromatografii cienkowarstwowej. Na chromatogramie uwidoczniono dwie plamki w odległości 5,6 cm i 3,5 cm od linii startu. Odległość czoła eluenta od linii startu wyniosła 10,1 cm, a wartości wskaźników Rf wzorców anionów wynoszą odpowiednio: Które z anionów zawierała badana próbka?
| Anion | Cl- | Br- | I- | SCN- |
| Wskaźnik Rf | 0,243 | 0,352 | 0,554 | 0,648 |
A. I- i SCN-
B. Cl- i SCN-
C. I"-i Br-
D. Cl- i Br-
Wykonywanie badań analityczny…
Wśród wskaźników stosowanych w analizach kompleksometrycznych znajdują się
A. skrobia
B. czerwień metylowa
C. kalces
D. błękit bromotymolowy
Wykonywanie badań analityczny…
Roztwór K2CrO4 jest używany jako wskaźnik przy oznaczaniu chlorków w metodzie Mohra. Powoduje on zmianę koloru mieszaniny reakcyjnej, co jest skutkiem
A. powstawania brunatnoczerwonego osadu Ag2CrO4 w obecności nadwyżki titrantu
B. utleniania chlorków, co prowadzi do powstania zielonożółtego chloru
C. adsorpcji żółtego roztworu wskaźnika na białym serowatym osadzie AgCl
D. przekształcania się żółtego K2CrO4 w pomarańczowy K2Cr2O7