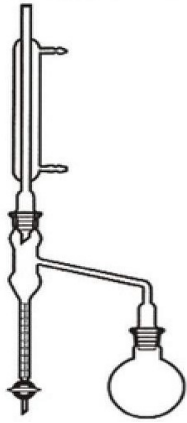
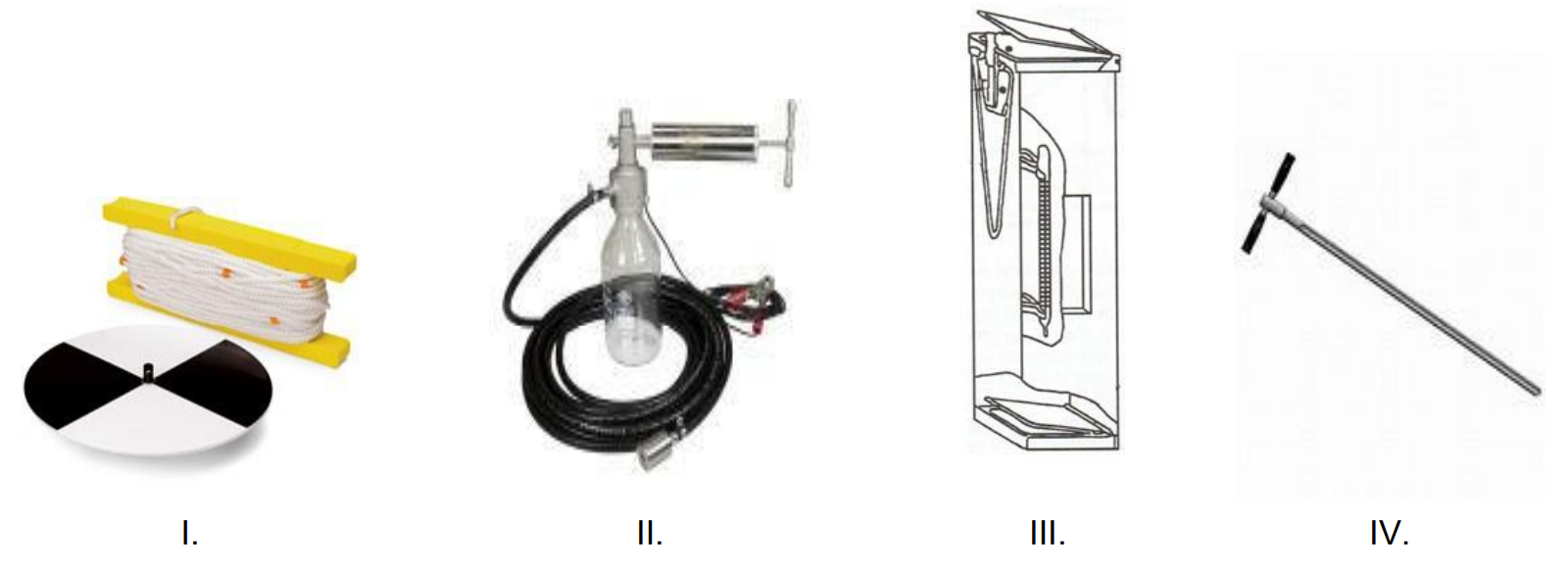
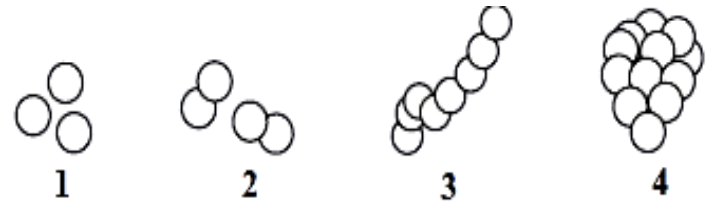
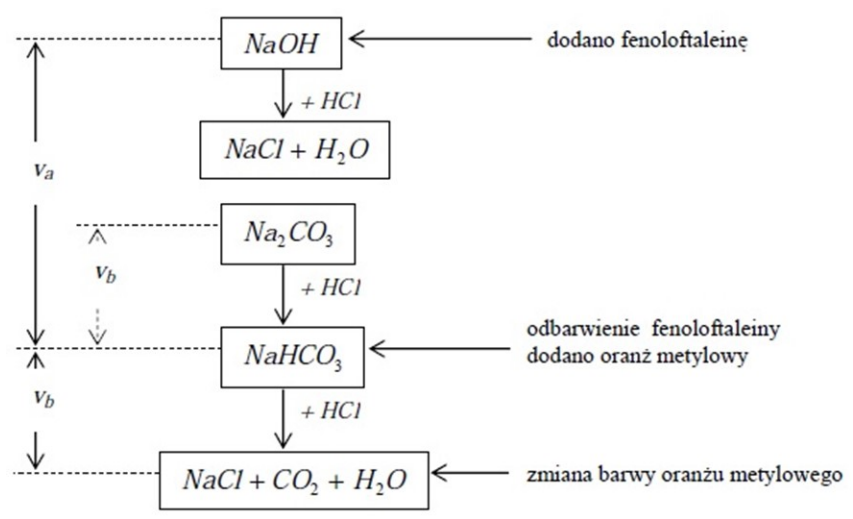
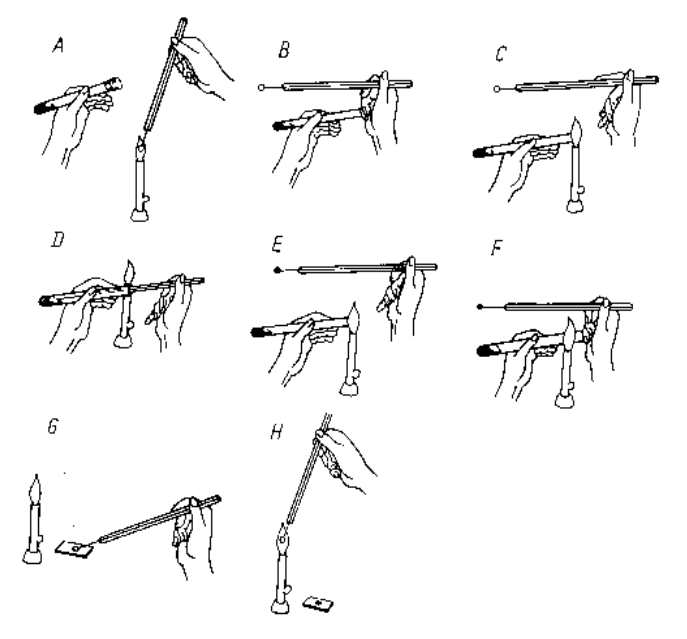
Jaką metodę poboru próbek przedstawiono na rysunku?


Odważka analityczna azotan(V) srebra(I) AgNO3 0,1 mol/dm3 |
| Próbkę roztworu naproksenu przenieść ilościowo do kolby miarowej o pojemności 100 cm3 i uzupełnić roztworem woda + metanol (1:3, v/v) do kreski. Odpipetować 25 cm3 tak przygotowanego roztworu do kolby stożkowej o pojemności 250 cm3 i po dodaniu 5 kropli fenoloftaleiny miareczkować mianowanym roztworem NaOH do uzyskania lekko różowego zabarwienia. |
| Obliczyć zawartość naproksenu w próbce według wzoru: |
| X = C · V · M · W |
| C - stężenie molowe roztworu NaOH, mol/dm3 V - objętość roztworu NaOH zużyta do miareczkowania, dm3 M - masa molowa naproksenu, g/mol W – współmierność kolby i pipety |
| NH4SCN amonu tiocyjanian | 0,1 mol/l |
| Stężenie po rozcieńczeniu do 1000 ml w 20°C | 0,1 mol/l ± 0,2 % |

| 16S Siarka 32 | 29Cu Miedź 63,55 |
| Tabela. Jednostki twardości wody | |||||
| Jednostka twardości | mmol/l | mval/l | mg CaCO3/l | °f stopień francuski | °n stopień niemiecki |
|---|---|---|---|---|---|
| 1 mmol/l | 1 | 2 | 100 | 10 | 5,6 |
| 1 mval/l | 0,5 | 1 | 50 | 5,0 | 2,8 |
| 1 mg CaCO3/l | 0,01 | 0,02 | 1 | 0,1 | 0,056 |
| 1 stopień francuski (°f) | 0,1 | 0,2 | 10 | 1 | 0,56 |
| 1 stopień niemiecki (°n) | 0,178 | 0,357 | 17,8 | 1,78 | 1 |
| Numer wzorca | 1. | 2. | 3. | 4. | 5. |
| Odmierzona ilość roztworu wzorcowego [cm3] | 0 | 1 | 2 | 3 | 4 |
| Barwa w stopniach mg Pt/dm3 | 0 | 5 | 10 | 15 | 20 |
| Objętość badanej próbki wody [cm3] | 100 |
| Wzorzec | 2. |
gdzie:
a – odczytana ze skali wzorców barwa próbki, mg Pt/dm³
V – objętość próbki, cm³
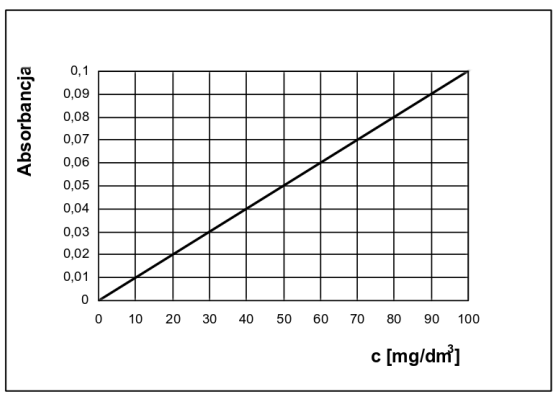
| A = ε · l · c |
| gdzie: |
| A – wartość absorbancji |
| ε – molowy współczynnik absorpcji; dm3/mol · cm |
| c – stężenie molowe roztworu; mol/dm3 |
| l – grubość kuwety; cm |
| A. | Mn2+ + 2OH− → Mn(OH)2 |
| B. | 2Mn(OH)2 + O2 → 2 MnO(OH)2 |
| C. | MnO(OH)2 + 4H+ → Mn4+ + 3H2O |
| D. | Mn4+ + 2I− → Mn2+ + I2 |
| Procedura Współoznaczanie wapnia i magnezu w wodach naturalnych polega na przeprowadzeniu dwóch miareczkowań mianowanym 0,0100 mol/dm3 roztworem EDTA. Pierwsze miareczkowanie przeprowadza się w środowisku buforu amoniakalnego pH = 10 wobec czerni eriochromowej T, jako wskaźnika. Objętość zużytego titranta odpowiada sumie zawartości jonów wapnia i magnezu. Drugie miareczkowanie przeprowadza się w środowisku silnie zasadowym pH=12-13 wobec mureksydu. Objętość użytego titranta zależy od ilości jonów wapnia. Podczas wykonywania oznaczenia zużyto na pierwsze miareczkowanie wobec czerni eriochromowej średnio V1= 20,3 cm3 roztworu EDTA, na drugie oznaczenie wobec mureksydu zużyto średnio V2= 5,4 cm3 tego samego roztworu EDTA. |
| Pb2+ | Hg22+ | Ag+ |
| + rozc. HCl | ||
| PbCl2↓ | Hg2Cl2↓ | AgCl↓ |
| Dodać kilka kropli H2O, ogrzać na łaźni, odsączyć na gorąco | ||
| Pb2+ | Hg2Cl2↓ | AgCl↓ |
| + K2CrO4 | + NH3 aq | +stęż. NH3 aq |
Ca – 40 g/mol; O – 16 g/mol; C – 12 g/mol; H – 1 g/mol