Filtrowanie pytań
Wykonywanie badań analityczny…
A. za pomocą areometru Trallesa
B. za pomocą areometru Ballinga
C. przy pomocy wagi hydrostatycznej
D. przy pomocy wiskozymetru Hópplera
Przygotowywanie sprzętu, odcz…
Podaj nazwę reagentu chemicznego, który w specyficznych warunkach reaguje tylko z jednym jonem, pierwiastkiem lub związkiem chemicznym?
A. Specyficzny
B. Wzorcowy
C. Selektywny
D. Grupowy
Wykonywanie badań analityczny…
Na etykiecie odczynnika chemicznego zawarte są następujące informacje. Z informacji wynika, że odczynnik ten może być zastosowany do sporządzenia roztworu o stężeniu około 0,1 mol/dm3 z dokładnością do
| NH4SCN amonu tiocyjanian | 0,1 mol/l |
| Stężenie po rozcieńczeniu do 1000 ml w 20°C | 0,1 mol/l ± 0,2 % |
A. 0,2 mol/dm3
B. 0,0002 mol/dm3
C. 0,02 mol/dm3
D. 0,002 mol/dm3
Przygotowywanie sprzętu, odcz…
Przy przygotowywaniu 100 cm3 roztworu o określonym stężeniu procentowym (m/V) konieczne jest odważenie wyliczonej ilości substancji, a następnie przeniesienie jej do
A. kolby miarowej, dodać 100 cm3 rozpuszczalnika, wymieszać, opisać
B. zlewki, rozpuścić w 100 cm3 rozpuszczalnika, opisać, wymieszać bagietką
C. kolby miarowej, rozpuścić, uzupełnić kolbę rozpuszczalnikiem do kreski, wymieszać, opisać
D. zlewki, rozpuścić w 100 cm3 rozpuszczalnika, przenieść do kolby miarowej, opisać
Wykonywanie badań analityczny…
Na zamieszczonym schemacie biosensora literą A oznaczono
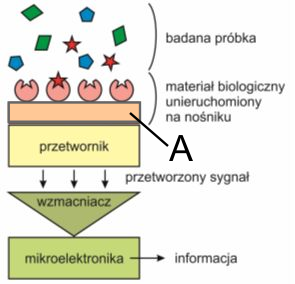
A. wzmacniacz sygnału.
B. biosensor.
C. element czuły.
D. transformator.
Wykonywanie badań analityczny…
Zamieszczone w tabeli dane techniczne dotyczą
| Specyfikacja urządzenia | |
|---|---|
| zakres pH | od -2,00 do 16,00pH |
| zakres temperatury | od -9,9 do 120,0 C |
| rozdzielczość: pH | 0,01pH |
| rozdzielczość temperatury | 0,1°C |
| kalibracja | automatyczna 1 lub 2 punktowa z 5 buforami |
| elektroda | szklana HI 1131B, elektrolitowa, kabel 1m |
| wymiary | 240*182*74mm |
| waga | 1,1kg |
A. tlenomierza.
B. pH-metru.
C. wagi analitycznej.
D. konduktometru.
Przygotowywanie sprzętu, odcz…
Naważkę NaOH o masie 0,0400 g rozpuścić w małej ilości wody, a następnie przelać ten roztwór do kolby miarowej o pojemności 500 cm3 i uzupełnić kolbę miarową wodą do tzw. kreski. Masa molowa NaOH wynosi 40,0 g/mol. Jakie jest stężenie molowe przygotowanego roztworu?
A. 2,000 mol/dm3
B. 0,002 mol/dm3
C. 0,200 mol/dm3
D. 0,020 mol/dm3
Wykonywanie badań analityczny…
Metoda analityczna, która polega na wyznaczaniu masy osadzonej substancji z roztworu z wykorzystaniem azotanu(V) srebra, to
A. jodometria
B. alkacymetria
C. kompleksometria
D. argentometria
Wykonywanie badań analityczny…
W celu oznaczenia zawartości kwasu azotowego(V) w technicznym kwasie przeprowadzono jego analizę według procedury:
Odważyć około 2 g badanego kwasu w naczyniu wagowym. Do zlewki o pojemności 250 cm³ wlać 50 cm³ wody destylowanej i dokładnie odmierzyć pipetą 50 cm³ 0,5-molowego roztworu NaOH oraz 2–4 kropli roztworu wskaźnika mieszanego (czerwieni metylowej z błękitem metylowym w etanolu)
Następnie zamurzyć naczynko z próbką kwasu w zlewce i po wymieszaniu roztworu odmiareczkowac nadmiar NaOH roztworem kwasu siarkowego(VI) o stężeniu 0,5 mol/dm³ do zmiany barwy z zielonej na fioletowo-czerwoną.
Określ podstawowe parametry oznaczenia.
| Typ miareczkowania | Titrant | Wskaźnik | Barwa w PK miareczkowania | |
|---|---|---|---|---|
| A. | pośrednie | 0,5-molowy roztwór H2SO4 | czerwień metylowa z błękitem metylowym w etanolu | fioletowo-czerwona |
| B. | bezpośrednie | 0,5-molowy roztwór H2SO4 | czerwień metylowa z błękitem metylowym w etanolu | zielona |
| C. | pośrednie | 0,5-molowy roztwór NaOH | czerwień metylowa z błękitem metylowym w etanolu | fioletowo-czerwona |
| D. | bezpośrednie | 0,5-molowy roztwór NaOH | czerwień metylowa z błękitem metylowym w etanolu | fioletowo-czerwona |
A. C.
B. B.
C. D.
D. A.
Wykonywanie badań analityczny…
Na podstawie zamieszczonego opisu wskaż, którą metodę stosuje się do oznaczania zawartości kwasu acetylosalicylowego.
| Oznaczenie zawartości kwasu acetylosalicylowego w preparacie farmaceutycznym |
| Oznaczenie polega na hydrolizie tego kwasu na gorąco, za pomocą mianowanego roztworu wodorotlenku sodu o stężeniu 0,1 mol/dm3, do salicylanu i octanu sodu. Nadmiar NaOH odmiareczkowuje się mianowanym roztworem kwasu siarkowego(VI) wobec fenoloftaleiny jako wskaźnika. |
A. Kompleksometryczną.
B. Argentometryczną.
C. Jodometryczną.
D. Alkacymetryczną.
Wykonywanie badań analityczny…
W tabeli przedstawiono skalę wzorców do oznaczania barwy wody.
Wyznacz barwę badanej próbki wody, korzystając ze wzoru:
| Numer wzorca | 1. | 2. | 3. | 4. | 5. |
| Odmierzona ilość roztworu wzorcowego [cm3] | 0 | 1 | 2 | 3 | 4 |
| Barwa w stopniach mg Pt/dm3 | 0 | 5 | 10 | 15 | 20 |
| Objętość badanej próbki wody [cm3] | 100 |
| Wzorzec | 2. |
X = a · 100 V
gdzie:
a – odczytana ze skali wzorców barwa próbki, mg Pt/dm³
V – objętość próbki, cm³
A. 0 mgPt/dm3
B. 10 mgPt/dm3
C. 15 mgPt/dm3
D. 5 mgPt/dm3
Przygotowywanie sprzętu, odcz…
Którą z poniższych czynności należy wykonać, aby zapewnić wysoką dokładność pomiaru masy substancji podczas przygotowywania próbki do analizy chemicznej?
A. Użyć linijki do określenia objętości substancji.
B. Zastosować wagę analityczną o dokładności do 0,1 mg.
C. Pominąć etap ważenia przy sporządzaniu roztworu.
D. Wystarczy ważyć substancję na zwykłej wadze kuchennej.
Przygotowywanie sprzętu, odcz…
W trzech probówkach umieszczono roztwory: wodorotlenku sodu, chlorku sodu i kwasu octowego. W celu identyfikacji zbadano ich odczyn za pomocą uniwersalnego papierka wskaźnikowego, a następnie fenoloftaleiny. Barwy wskaźników w badanych roztworach przedstawiono w tabeli:
| Wskaźnik | Barwa wskaźnika | ||
|---|---|---|---|
| próbówka nr 1 | próbówka nr 2 | próbówka nr 3 | |
| uniwersalny papierek wskaźnikowy | żółty | czerwony | niebieski |
| fenoloftaleina | bezbarwny | bezbarwny | malinowa |
A. W probówce nr 2 znajdował się roztwór o pH powyżej 9.
B. Po zastosowaniu tylko fenoloftaleiny można stwierdzić, że w probówce nr 1 był roztwór chlorku sodu.
C. Po zastosowaniu tylko uniwersalnego papierka wskaźnikowego można stwierdzić, że w probówce nr 3 był roztwór wodorotlenku sodu.
D. W probówce nr 1 znajdował się roztwór o odczynie zasadowym.
Przygotowywanie sprzętu, odcz…
Proces usuwania substancji z cieczy lub wydobywania składnika z mieszanin cieczy, oparty na równowadze fazowej ciecz-gaz, nazywa się
A. filtracja
B. dekantacja
C. destylacja
D. krystalizacja
Przygotowywanie sprzętu, odcz…
Odczynnik, który nie został wykorzystany, należy zutylizować zgodnie z informacjami zawartymi na etykiecie
A. w kwietniu 2017 roku
B. 13 maja 2017 roku
C. w czerwcu 2017 roku
D. 5 maja 2017 roku
Wykonywanie badań analityczny…
Na rysunku przedstawiono wykres zależności absorbancji od stężenia fosforu. Ile wynosi stężenie fosforu w próbce, jeśli absorbancja dla badanej próbki wynosi A = 0,628?
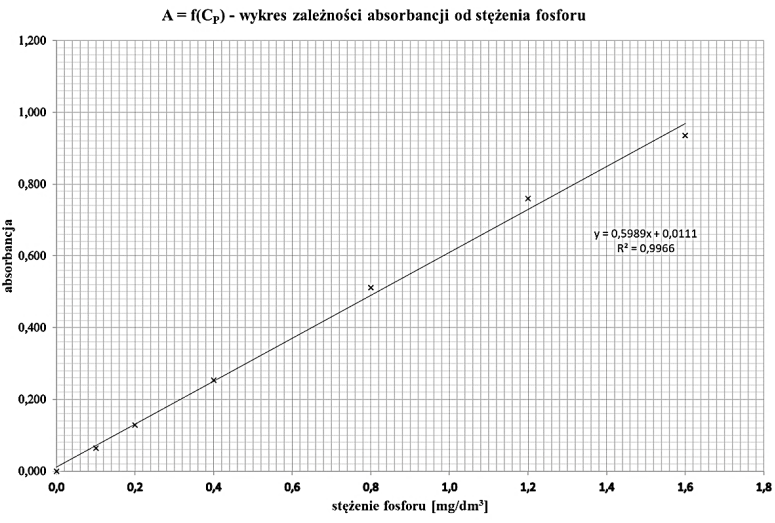
A. 1,088 mg/dm3
B. 1,010 mg/dm3
C. 1,055 mg/dm3
D. 1,030 mg/dm3
Wykonywanie badań analityczny…
Przeprowadzono orientacyjną ocenę jakości mikrobiologicznej mleka w tak zwanej próbie azotanowej, która zabarwiła się na kolor bladoróżowy, co znaczy, że jakość mleka wziętego do analizy była
| Zabarwienie próbki mleka | Ocena jakości próbki Mleko: |
|---|---|
| bez zmiany barwy | bardzo dobre i dobre |
| lekko lub wyraźnie różowa | średniej jakości |
| intensywnie różowa, czerwona lub brunatna | złej jakości |
A. dobra.
B. zła.
C. bardzo dobra.
D. średnia.
Wykonywanie badań analityczny…
Zjawisko, w którym obce jony są mechanicznie zatrzymywane przez szybko rosnący kryształ, określane jest mianem
A. współstrącania
B. okluzji
C. adsorpcji powierzchniowej
D. efektu solnego
Wykonywanie badań analityczny…
Podział anionów na grupy analityczne według Bunsena obejmuje ile grup?
A. dziesięć grup analitycznych
B. siedem grup analitycznych
C. pięć grup analitycznych
D. cztery grupy analityczne
Wykonywanie badań analityczny…
Dawka substancji, która powoduje pierwsze widoczne zmiany w organizmie, nazywana jest
A. toksyczna
B. lecznicza
C. progowa
D. letalna
Wykonywanie badań analityczny…
Który z reagentów można wykorzystać do wykrywania skrobi?
A. Br2(aq)
B. CuSO4(aq)
C. NaCl(aq)
D. I2 w KI(aq)
Przygotowywanie sprzętu, odcz…
Podczas oznaczania kwasu siarkowego zachodzi reakcja:
H2SO4 + 2NaOH → Na2SO4 + 2H2O
Zgodnie z zamieszczoną instrukcją, roztwór poreakcyjny należy
| Fragmenty instrukcji zbierania, utylizacji i eliminacji odpadów chemicznych | |
|---|---|
| Lista substancji, które mogą być usunięte z odpadami komunalnymi w postaci stałej, lub wprowadzone do systemu kanalizacyjnego w postaci rozcieńczonych roztworów wodnych, o ile ich ilość nie przekracza jednorazowo 100 g. | |
| Związki nieorganiczne Siarczany sodu, potasu, magnezu, wapnia, amonu | |
| Kwasy nieorganiczne Stężone kwasy ostrożnie rozcieńczyć przez wkroplenie z równoczesnym mieszaniem do wody z lodem, a następnie zneutralizować roztworem wodorotlenku sodowego. Po neutralizacji doprowadzić pH roztworu do zakresu 6-8 przelać do pojemnika S. Małe ilości kwasów takich jak siarkowy, solny, azotowy czy fosforowy (nie więcej niż 10 g) po rozcieńczeniu wodą i neutralizacji roztworem wodorotlenku sodowego oraz doprowadzeniu pH takiego roztworu do zakresu 6-8 można wylać do zlewu i obficie spłukać wodą. | |
| Sole nieorganiczne Stałe sole nieorganiczne – pojemnik N. Obojętne roztwory soli nieorganicznych pojemnik S. Sole metali ciężkich, sole o właściwościach toksycznych – pojemnik TN. |
A. zobojętnić i usunąć z odpadami komunalnymi.
B. wylać do zlewu i spłukać bieżącą wodą.
C. umieścić w pojemniku TN.
D. umieścić w pojemniku S.
Wykonywanie badań analityczny…
Czym jest efekt wspólnego jonu?
A. osadzanie się na powierzchni osadu jonów ujemnych oraz dodatnich, które nie są częścią składu osadu.
B. zmniejszenie rozpuszczalności osadu spowodowane obecnością jonu wspólnego z osadem.
C. osadzanie się na powierzchni osadu jonów ujemnych, które nie są częścią składu osadu.
D. wzrost rozpuszczalności osadu spowodowany obecnością jonu wspólnego z osadem.
Wykonywanie badań analityczny…
W tabeli przedstawiono wartości iloczynów rozpuszczalności wybranych siarczanów(VI).
| CaSO4 | 6,1·10-5 |
| SrSO4 | 2,8·10-7 |
| BaSO4 | 1,1·10-10 |
| PbSO4 | 2,2·10-8 |
Po dodaniu roztworu kwasu siarkowego(VI) do roztworu zawierającego Ca2+, Sr2+, Ba2+, Pb2+ jako pierwszy wytrąci się osad
A. CaSO4
B. BaSO4
C. SrSO4
D. PbSO4
Wykonywanie badań analityczny…
Określ typ pożywki, która składa się z agarów zwykłych (1000 ml) oraz 5% baraniej krwi (50-100 ml)?
A. Specjalistyczna.
B. Selektywna.
C. Prosta.
D. Wzbogacona.
Wykonywanie badań analityczny…
Jakim urządzeniem określa się temperaturę zapłonu oleju opałowego?
A. urządzeniem Marcussona
B. kriometrem
C. bombą kalorymetryczną
D. urządzeniem Orsata
Przygotowywanie sprzętu, odcz…
W jakiej standardowej temperaturze są kalibrowane szklane naczynia pomiarowe?
A. 20°C
B. 21°C
C. 25°C
D. 19°C
Przygotowywanie sprzętu, odcz…
Jakie roztwory chemiczne powinny być stanowczo pobierane przy włączonym dygestorium?
A. glicerolu o stężeniu 36%
B. etanolu o stężeniu 36%
C. kwasu cytrynowego o stężeniu 36%
D. kwasu solnego o stężeniu 36%
Wykonywanie badań analityczny…
Z uwagi na niską zawartość żelaza w wodzie, najbardziej adekwatną metodą określania całkowitej ilości jonów żelaza(II) oraz (III) w próbkach wody pitnej jest
A. manganometryczne wykrywanie jonów żelaza(II)
B. spektrfotometryczne wykrywanie jonów żelaza(III) z użyciem metody rodankowej
C. argentometryczne wykrywanie jonów żelaza(III) przy zastosowaniu metody Mohra
D. polarograficzne oznaczanie jonów żelaza(III) z użyciem rodanku potasu
Wykonywanie badań analityczny…
Opis w ramce przedstawia procedurę ilościowego oznaczania
| Do kolby miarowej o pojemności 250 cm3 odpipetować 25 cm3 3% wody utlenionej i dopełnić wodą do kreski. Do kolby stożkowej o pojemności 250 cm3 odpipetować 20 cm3 próbki rozcieńczonej wody utlenionej, dodać 25 cm3 kwasu siarkowego(VI) (1+4) i miareczkować roztworem manganianu(VII) potasu o stężeniu 0,02 mol/dm3 do pojawienia się trwałego różowego zabarwienia. |
A. nadtlenku wodoru metodą manganometryczną.
B. wody utlenionej metodą alkacymetryczną.
C. manganianu(VII) potasu metodą miareczkową.
D. kwasu siarkowego(VI) metodą manganometryczną.
Przygotowywanie sprzętu, odcz…
Odlanie cieczy z nad osadu to
A. sedymentacja
B. filtracja
C. dekantacja
D. destylacja
Wykonywanie badań analityczny…
Na rysunku przedstawiono wyznaczanie punktu końcowego miareczkowania metodą
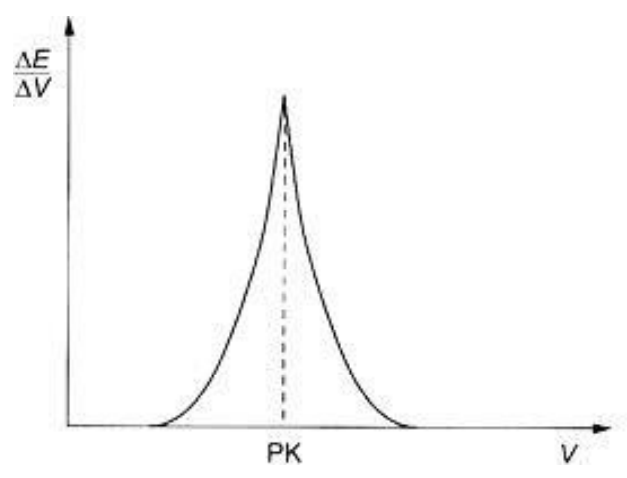
A. pierwszej pochodnej.
B. drugiej pochodnej.
C. połówkową.
D. grawimetryczną.
Przygotowywanie sprzętu, odcz…
Maksymalna średnica ziaren w partii substancji stałej wynosi 0,5 cm. Zgodnie z danymi zawartymi w tabeli próbka pierwotna tej substancji powinna mieć masę minimum
| Tabela. Masa próbki pierwotnej w zależności od wielkości ziaren lub kawałków | ||||
| Średnica ziaren lub kawałków [mm] | do 1 | 1 - 10 | 11 - 50 | ponad 50 |
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
A. 100 g
B. 1000 g
C. 200 g
D. 2500 g
Przygotowywanie sprzętu, odcz…
Oblicz stężenie molowe 250 cm3 roztworu NaOH, w którym znajduje się 0,5 g substancji. Masa molowa NaOH wynosi 40 g/mol
A. 0,01 mol/dm3
B. 0,05 mol/dm3
C. 0,50 mol/dm3
D. 0,10 mol/dm3
Przygotowywanie sprzętu, odcz…
Ekstrakcję w trybie ciągłym przeprowadza się
A. w aparacie Soxhleta
B. w rozdzielaczu z korkiem
C. w zestawie do ogrzewania
D. w kolbie płaskodennej
Wykonywanie badań analityczny…
Toksyczność względną zanieczyszczeń opisuje wzór:
Korzystając z danych z tabeli, oblicz toksyczność względną węglowodorów.
| Zanieczyszczenia emitowane do ekosystemu powietrza | NDS [ppm] |
|---|---|
| CO | 40,0 |
| CxHy | 19,3 |
| SO2 | 1,4 |
| NOx | 0,5 |

A. 1
B. 80
C. 2
D. 28
Przygotowywanie sprzętu, odcz…
Niemetal o kolorze fioletowoczarnym, który łatwo przechodzi w stan gazowy, to
A. brom
B. chlor
C. jod
D. fosfor
Wykonywanie badań analityczny…
Skalę wzorców do oznaczenia zawartości ołowiu przygotowano w cylindrach Nesslera o pojemności 100 cm3. Zawartość ołowiu oznaczona w tabeli jako X wynosi
| Ilość wzorcowego roztworu roboczego ołowiu w cm3 | 0,0 | 0,5 | 1,0 | 2,0 | 3,0 |
| Zawartość ołowiu w mg | 0,0 | 0,005 | X | 0,020 | 0,030 |
A. 0,100 mg
B. 0,001 mg
C. 0,010 mg
D. 0,0001 mg
Wykonywanie badań analityczny…
Maksymalne dzienne przyjęcie (ADI) benzoesanu sodu wynosi 0,5 mg/kg wagi ciała. Ile maksymalnie benzoesanu sodu może dziennie spożywać osoba ważąca 70 kg?
A. 175 mg
B. 450 mg
C. 70 mg
D. 350 mg
Wykonywanie badań analityczny…
Reakcja: MnO4- + 8H+ + 5e- → Mn2+ + 4H2O jest wykorzystywana w metodzie analizy jakościowej, określanej jako
A. kompleksometria
B. acydymetria
C. alkalimetra
D. redoksometria