Filtrowanie pytań
W naczyniu rozdzielającym umieszczono wodę oraz eter etylowy (d20 = 0,7138 g/cm3) i dokładnie je wymieszano.
Metody graficzne, pierwsza pochodna oraz Hahna znajdują zastosowanie w wyznaczaniu punktu końcowego miareczkowania?
W procedurze analitycznej zapisano. Ile wynosi zawartość procentowa Na2B4O7 • H2O w badanej próbce boraksu, jeżeli na zmiareczkowanie 0,3 g próbki zużyto 15,4 cm3 roztworu NaOH?
| 1 cm3 roztworu NaOH o stężeniu 0,1 mol/dm3 odpowiada 19,07 mg tetraboranu sodu Na2B4O7·H2O |
Który z parametrów jakości wody jest nieprawidłowo opisany?
| Mętność | 0,19 NTU | |
| Barwa | Akceptowalna - 10 mg Pt/dm3 | |
| Jon amonowy | 0,15 mg NH4+/dm3 | |
| Twardość | Węglanowa | Stopnie niemieckie |
| 8,01°dH | 140 mg/dm3 | |
Jaka jest wartość stałej Michaelisa, przy której enzym ma największe powinowactwo do substratu?
Zgodnie z zamieszczonym fragmentem metodyki postępowania analitycznego mineralizację próbki paszy należy przeprowadzić w kolbie
| Fragment metodyki postępowania analitycznego: |
| (...) Metoda służy do oznaczania zawartości białka w paszach na podstawie zawartości oznaczonego azotu. Próbka jest mineralizowana kwasem siarkowym(VI) w obecności katalizatora. Kwaśny roztwór jest alkalizowany za pomocą wodorotlenku sodu. Amoniak oddestylowany z zasadowego roztworu jest zbierany w znanej ilości roztworu kwasu siarkowego(VI), którego nadmiar jest z kolei miareczkowany roztworem wodorotlenku sodu. (...) |
Wśród substancji konserwujących stosowanych w żywności występują CH3COONH4 (E 264) oraz C6H5COONa (E 211). Związki te można określić jako
Do roztworu zawierającego jony Ca2+ i Ni2+ o równym stężeniu dodawano kroplami roztwór węglanu sodu. Iloczyn rozpuszczalności węglanu wapnia wynosi 4,8x10-9, natomiast węglanu niklu 1,7x10-7. Który węglan wytrąci się jako pierwszy?
W trakcie zmiareczkowania próbki roztworu NaOH zużyto 15,0 cm3 roztworu HCl o stężeniu 0,1 mol/dm3. Ilość NaOH (M = 40 g/mol) w analizowanej próbce wyniosła
Podstawowe kryteria oceny jakości nafty to:
Oznaczono zawartość cynku w stopie metodą kompleksometryczną. W tym celu odważono 0,50 g stopu i przeprowadzono do roztworu. Próbkę do badań przygotowano w kolbie miarowej o pojemności 250 cm3. Następnie do trzech kolb stożkowych odpipetowano po 50 cm3 roztworu z przygotowanej próbki do badań. Próbki miareczkowano roztworem EDTA o stężeniu 0,01 mmol/cm3. Zużyta średnia objętość roztworu EDTA wyniosła 32,5 cm3. Korzystając z zamieszczonego wzoru, oblicz procentową zawartość cynku w stopie.
| mZn = V · CEDTA · 65,37 · W |
| mZn – masa cynku; mg V – objętość zużytego roztworu EDTA w trakcie miareczkowania; cm3 CEDTA – stężenie molowe roztworu EDTA; mmol/cm3 65,37 – masa molowa cynku; mg/mmol W – współmierność kolby miarowej i pipety; 5 |
W analizowanej próbce oznaczono obecność baru, wytrącając go jako BaSO4. Otrzymano osad o masie 200 mg. Jaka była zawartość baru w próbce, jeśli mnożnik analityczny wynosi 0,5885?
W jakiej proporcji molowej EDTA reaguje z jonami Zn2+?
Wykonano analizę mikrobiologiczną próbki wody wodociągowej o objętości 100 ml i uzyskano wyniki:
Wymagania mikrobiologiczne, jakim powinna odpowiadać woda wodociągowa wprowadzana | |||
|---|---|---|---|
| Lp. | Parametr | Wartość parametryczna | |
| liczba mikroorganizmów [jtk lub NPL] | objętość próbki [ml] | ||
| 1. | Escherichia coli | 0 | 250 |
| 2. | Enterokoki | 0 | 250 |
| 3. | Pałeczka ropy błękitnej (Pseudomonas aeruginosa) | 0 | 250 |
| 4. | Ogólna liczba mikroorganizmów w 36±2°C | 20 | 1 |
| 5. | Ogólna liczba mikroorganizmów w 22±2°C | 100 | 1 |
| Escherichia coli | nieobecne |
| Enterokoki | nieobecne |
| Pałeczki ropy błękitnej | nieobecne |
| Ogólna liczba mikroorganizmów w 37°C | 1200 |
| Ogólna liczba mikroorganizmów w 22°C | 11000 |
Lepkość dynamiczna wody
| Tabela. Gęstość (d) i lepkość dynamiczna wody (η) w danej temperaturze (T). | ||
| T [K] | d [g/cm3] | η [cP] |
| 293 | 0,99823 | 1,0050 |
| 298 | 0,99707 | 0,8937 |
| 303 | 0,99567 | 0,8007 |
| 308 | 0,99406 | 0,7225 |
| 313 | 0,99222 | 0,6560 |
| 318 | 0,99025 | 0,5988 |
| 323 | 0,98807 | 0,5494 |
| 328 | 0,98573 | 0,5064 |
| 333 | 0,98324 | 0,4688 |
Wykonano jodometryczne oznaczenie zawartości kwasu askorbinowego dla 4 próbek tabletek witaminy C, uzyskując wyniki. Na podstawie informacji zawartych w opisie i wyników analizy można stwierdzić, że zawartość witaminy C
| Opis Na opakowaniach tabletek witaminy C producenci deklarują zawartość 200 mg kwasu askorbinowego. Zgodnie z normą odchylenia od deklarowanej zawartości substancji leczniczej nie mogą przekraczać ±10% dla tabletek o zawartości poniżej 100 mg i ±5% dla tabletek o deklarowanej zawartości 100 mg i więcej. | ||||
| Próbka | 1 | 2 | 3 | 4 |
| Zawartość kwasu askorbinowego | 198,5 mg | 211 mg | 201 mg | 205 mg |
Jakie jest stężenie analitu wyrażone w procentach, gdy próbka analityczna zawiera 250 ppm analitu?
Dokładność metody definiowana jest na podstawie ustalonej wartości
Błąd miareczkowania w oznaczeniach objętościowych nie występuje, gdy
Jakie aspekty nie są objęte badaniami organoleptycznymi olejów rafinowanych?
Analiza wody opadowej, obejmująca pomiar: temperatury, koloru, klarowności oraz zapachu, zalicza się do badań
Po przeprowadzeniu analizy wagowej uzyskano 253 mg Mg2P2O7. Jaką ilość gramów magnezu zawierała zbadana próbka, jeśli współczynnik analityczny wynosi 0,2185?
Błąd pomiarowy, który stanowi różnicę pomiędzy średnim wynikiem pomiaru a wartością rzeczywistą, określa się mianem
Oznaczona twardość ogólna wody wynosi 2 mval/dm3. Wartość ta przeliczona na stopnie niemieckie, zgodnie z zamieszczonym przelicznikiem jednostek, wynosi
| 1 mval/dm3 – 2,8°dH (stopni niemieckich) |
W trakcie oznaczania węglanu sodu przy użyciu wodorotlenku sodu metodą Wardera warto miareczkować próbkę od razu przy umiarkowanym mieszaniu, ponieważ mogą się rozpuszczać cząsteczki CO2 z atmosfery, co skutkuje
Na podstawie danych zamieszczonych w tabeli określ zależność lepkości cieczy od temperatury.
| Ciecz | Lepkość [Pa×s×10-3] | |||
|---|---|---|---|---|
| 0°C | 10°C | 30°C | 60°C | |
| Aceton | 0,397 | 0,361 | 0,296 | 0,228 |
| Toluen | 0,700 | 0,667 | 0,517 | 0,381 |
| Woda | 1,792 | 1,308 | 0,801 | 0,469 |
W temperaturze 20°C wyznaczono gęstość i współczynnik załamania światła kwasu butanowego. Wyniki zestawiono w tabeli:
| Gęstość | Współczynnik załamania światła |
|---|---|
| 0,960 g/cm³ | 1,398 |
RM = (n² − 1) · M
(n² + 2) · d
RM – refrakcja molowa, cm³/mol
n – współczynnik załamania światła
d – gęstość, g/cm³
M – masa molowa, 88 g/mol
Sporządzono wykres potencjometrycznego miareczkowania alkacymetrycznego. W jaki sposób należy opisać oś Y?
| A. | ΔpH/ΔVtitranta |
| B. | ΔSEM/ΔVtitranta |
| C. | pH/ΔVtitranta |
| D. | SEM/ΔVtitranta |
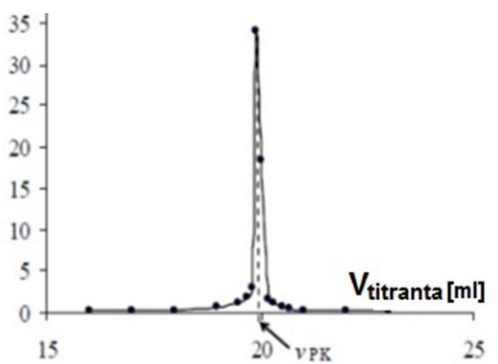
Oblicz ilość amoniaku w badanej próbce, jeśli do jej zmiareczkowania wykorzystano 20,0 cm3 roztworu HCl o stężeniu 0,1 mol/dm3.
Z jaką precyzją należy zważyć próbkę o masie 20 mg, aby błąd względny nie wynosił więcej niż 0,05%?
Czym są lipidy złożone?
W równaniu dotyczącym iloczynu rozpuszczalności siarczanu(VI) baru: Kso = [Ba2+][SO42-], jonowe stężenia Ba2+ oraz SO42- są przedstawione jako
Ogólna twardość próbki wody stosowanej w technologiach wynosi 16,5°n, a twardość węglanowa osiąga 7,2°n. Jaką wartość ma twardość stała?
Absorbancja barwnego roztworu o stężeniu 0,0004 mol/dm3, zmierzona w kuwecie o grubości 1 cm wynosi 0,30. Korzystając z zamieszczonego wzoru, oblicz wartość molowego współczynnika absorpcji £.
| A = ε · l · c |
| gdzie: |
| A – wartość absorbancji |
| ε – molowy współczynnik absorpcji; dm3/mol · cm |
| c – stężenie molowe roztworu; mol/dm3 |
| l – grubość kuwety; cm |
Z analizy danych zawartych w tabeli wynika, że
| Tabela. Rodzaj paliwa stałego, zawartość węgla pierwiastkowego i wartość opałowa | ||||
|---|---|---|---|---|
| Rodzaj paliwa | Torf | Węgiel brunatny | Węgiel kamienny | Antracyt |
| Zawartość C, % | 55 – 63 | 63 – 76 | 80 – 90 | 93 – 98 |
| Wartość opałowa, MJ/kg | 21 – 24 | 26 – 32 | 30 – 35 | 36 |
W makroanalizie wykorzystuje się próbki o ciężarze
W zamieszczonym opisie przedstawiono fragment instrukcji obsługi
| Umieść probówki w adapterach. Zawsze umieszczaj probówki symetrycznie celem prawidłowego wyważenia rotora. W przypadku użycia tylko jednej probówki niezbędne jest umieszczenie przeciwwagi po stronie przeciwnej. Po zamknięciu pokrywy zostaje ona automatycznie zablokowana ... |
W wyniku oznaczenia wagowego otrzymano 0,2451 g tlenku żelaza(III). Ile gramów żelaza zawierała analizowana próbka?
| MFe = 55,845 g/mol, MO = 15,999 g/mol |
Woda obecna w cząsteczce Ca(OH)2 określana jest jako woda
Roztwór zawierający aniony I grupy analitycznej poddano identyfikacji metodą chromatografii cienkowarstwowej. Na chromatogramie uwidoczniono dwie plamki w odległości 5,6 cm i 3,5 cm od linii startu. Odległość czoła eluenta od linii startu wyniosła 10,1 cm, a wartości wskaźników Rf wzorców anionów wynoszą jak w tabeli. Które z anionów zawierała badana próbka?
| Anion | Cl- | Br- | I- | SCN- |
|---|---|---|---|---|
| Wskaźnik Rf | 0,243 | 0,352 | 0,554 | 0,648 |